
【題目】利用元素的化合價推測物質的性質是化學研究的重要手段。如圖是硫元素的常見化合價與部分物質類別的對應關系:
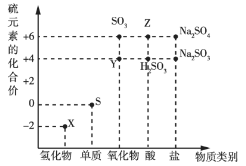
(1)從硫元素化合價變化的角度分析,圖中既有氧化性又有還原性的化合物有______(填化學式)。
(2)將![]() 與
與![]() 混合,可生成黃色固體,該反應中氧化劑與還原劑的物質的量之比為______。
混合,可生成黃色固體,該反應中氧化劑與還原劑的物質的量之比為______。
(3)![]() 是重要的化工原料。從氧化還原反應的角度分析,下列制備
是重要的化工原料。從氧化還原反應的角度分析,下列制備![]() 的方案理論上可行的是______(填序號)。
的方案理論上可行的是______(填序號)。
a.![]() b.
b.![]()
c.![]() d.
d.![]()
(4)已知![]() 能被
能被![]() 氧化為
氧化為![]() ,則
,則![]() 的
的![]() 溶液與
溶液與![]() 的
的![]() 溶液恰好反應時,
溶液恰好反應時,![]() 元素在還原產物中的化合價為______。
元素在還原產物中的化合價為______。
【答案】![]() 、
、![]() 、
、![]()
![]() b
b ![]()
【解析】
(1)根據氧化還原反應中的價態規律,處于中間價態的既具有氧化性又具有還原性;
(2)X為氫化物,且S顯-2價,即X為H2S,表現還原性,Y為氧化物,且S顯+4價,即Y為SO2,與H2S反應生成S單質;
(3)Na2S2O3中S的價態為+2價,根據氧化還原反應的規律進行分析;
(4)利用得失電子數目守恒進行分析計算;
(1)含有中間價態元素的物質既有還原性又有氧化性,![]() 元素常有
元素常有![]() 價、0價、
價、0價、![]() 價、
價、![]() 價,0價的硫單質和
價,0價的硫單質和![]() 價
價![]() 的化合物既有還原性又有氧化性,由題圖知
的化合物既有還原性又有氧化性,由題圖知![]() 為
為![]() ,
,![]() 為
為![]() ;
;
(2) X為氫化物,且S顯-2價,即X為H2S,表現還原性,Y為氧化物,且S顯+4價,即Y為SO2,將![]() 與
與![]() 混合,可生成黃色固體,反應的化學方程式為
混合,可生成黃色固體,反應的化學方程式為![]() ,反應中
,反應中![]() 作還原劑,
作還原劑,![]() 作氧化劑,則該反應中氧化劑與還原劑的物質的量之比為
作氧化劑,則該反應中氧化劑與還原劑的物質的量之比為![]() ;
;
(3)![]() 中
中![]() 元素的化合價為
元素的化合價為![]() ,從氧化還原的角度分析,反應物中
,從氧化還原的角度分析,反應物中![]() 元素的化合價必有一種大于
元素的化合價必有一種大于![]() ,另一種小于
,另一種小于![]() ,
,
a. ![]() 元素的化合價都小于
元素的化合價都小于![]() ,故a不符合;
,故a不符合;
b. Na2SO3中S顯+4價,S單質為0價,符合上述分析,故b符合;
c. SO2中S的化合價為+4,Na2SO4中S的價態為+6價,故c不符合;
d. Na2SO3中S價態為+4價,Na2SO4中S的價態為+6價,故d不符合;
(4)假設![]() 元素在生成物中的化合價為+a,根據得失電子守恒,得
元素在生成物中的化合價為+a,根據得失電子守恒,得![]() ,解得a=3。
,解得a=3。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】下列有關文獻記載中涉及的化學知識表述不正確的是( )
A.“以曾青涂鐵,鐵赤色如銅”說明我國古代就掌握了“濕法冶金”技術
B.“墻塌壓糖,去土而糖白”中的脫色過程發生了化學變化
C.“丹砂燒之成水銀,積變又還成丹砂”講的是單質與化合物之間的互變
D.《本草綱目》中記載:“燒酒非古法也,……,用濃酒和糟入甑,蒸令氣上,用器承取滴露。”涉及的操作方法是蒸餾
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,鹽酸與氫氧化鈉溶液相互滴定的滴定曲線如下圖,下列敘述不正確的是
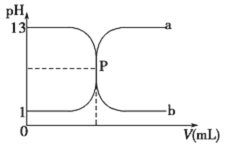
A. 滴定過程的任何時刻都存在:c(H+)+ c(Na+)=c(OH-)+c(Cl-)
B. 曲線b是用氫氧化鈉溶液滴定鹽酸溶液的滴定曲線
C. 氫氧化鈉溶液的物質的量濃度為0.1molL-1
D. P點時恰好完全中和,溶液呈中性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一絕熱(不與外界發生熱交換)的恒容容器中,發生反應:2A(g)+B(s)![]() C(g)+D(g),下列描述中不能表明該反應已達到平衡狀態的是
C(g)+D(g),下列描述中不能表明該反應已達到平衡狀態的是
A.混合氣體的密度不變B.單位時間內生成nmolD,同時生成nmolC
C.容器中的溫度不再變化D.C(g)的物質的量濃度不變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】向某密閉容器中加入 0.3 mol A、0.1 mol C 和一定量的 B 三種氣體, 一定條件下發生如下反應:3A(g) ![]() B(g)+2C(g),各物質的濃度隨時間變化如圖所示[t0~t1 階段的 c(B)變化未畫出]。下列說法中正確的是
B(g)+2C(g),各物質的濃度隨時間變化如圖所示[t0~t1 階段的 c(B)變化未畫出]。下列說法中正確的是

A. 若t1=15s, A 的濃度變化表示 t0~t1階段的平均反應速率為 0.09 mol·L-1·s-1
B. t0~t1階段,此過程中容器放出a kJ熱量,該反應的熱化學方程式為:3A(g)![]() B(g)+2C(g) ΔH=-50a kJ·mol-1
B(g)+2C(g) ΔH=-50a kJ·mol-1
C. 該容器的容積為2 L,B的起始的物質的量為0.03 mol
D. t1時該反應達到平衡且A 的轉化率為60%
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知硫粉跟亞硫酸鈉溶液共熱可制得硫代硫酸鈉![]() 。現以硫化亞鐵
。現以硫化亞鐵![]() 為主要原料,按如圖所示流程制取硫代硫酸鈉。已知
為主要原料,按如圖所示流程制取硫代硫酸鈉。已知![]() 能與
能與![]() 反應生成
反應生成![]() 和
和![]() 。圖中
。圖中![]() 、
、![]() 、
、![]() 、
、![]() 是硫單質或硫的化合物,其他不含硫的反應產物已被略去,各步反應可以添加必要的試劑。
是硫單質或硫的化合物,其他不含硫的反應產物已被略去,各步反應可以添加必要的試劑。
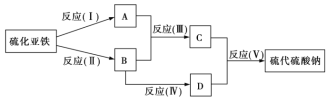
請回答下列問題:
(1)反應(I)的離子方程式為______。
(2)物質![]() 的化學式為______
的化學式為______
(3)物質![]() 的化學式為______
的化學式為______
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在400℃、101 kPa時,NO2(g) +CO(g) ![]() NO(g) + CO2(g) 反應過程的能量變化如下圖所示。
NO(g) + CO2(g) 反應過程的能量變化如下圖所示。
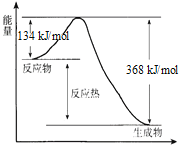
反應過程
(1)該反應是_____________(填“吸熱”或“放熱”)反應。
(2)該反應的熱化學方程式為_____________。
(3)改變下列條件都可使該反應的反應速率改變,其中通過降低活化能加快反應速率的是_____________。
a.濃度 b.壓強 c.溫度 d.催化劑
(4)反應體系中加入催化劑對反應熱是否有影響?____(填“是”或“否”),原因是____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一固定容積的密閉容器中進行著如下反應:CO2(g)+H2(g)![]() CO(g)+H2O(g),其平衡常數K和溫度t的關系:
CO(g)+H2O(g),其平衡常數K和溫度t的關系:
t℃ | 700 | 800 | 850 | 1000 | 1200 |
K | 2.6 | 1.7 | 1.0 | 0.9 | 0.6 |
(1)K的表達式為:_________;
(2)該反應的正反應為_________反應(“吸熱”或“放熱”);
(3)下列選項中可作為該反應在850℃時已經達到化學平衡狀態的標志的是:_________。
A.容器中壓強不再變化 B.混合氣體中CO濃度不再變化
C.混合氣體的密度不再變化 D.c(CO2)=c(CO)=c(H2)=c(H2O)
(4)當溫度為850℃,某時刻測得該溫度下的密閉容器中各物質的物質的量見表:
CO | H2O | CO2 | H2 |
0.5mol | 8.5mol | 2.0mol | 2.0mol |
此時上述的反應中正、逆反應速率的關系式是_________(填代號)。
A.v(正)>v(逆) B.v(正)<v(逆) C.v(正)=v(逆) D.無法判斷
(5)在700℃通過壓縮體積增大氣體壓強,則該反應中H2(g)的轉化率_________(“增大”、“減小”或“不變”);工業生產中,通過此方法使容器內氣體壓強增大以加快反應,卻意外發現H2(g)的轉化率也顯著提高,請你從平衡原理解釋其可能原因是__________________________________________。
Ⅱ.設在容積可變的密閉容器中充入10molN2(g)和10molH2(g),反應在一定條件下達到平衡時,NH3的體積分數為0.25。
(6)求該條件下反應N2(g)+3H2(g)![]() 2NH3(g)的平衡常數__________。(設該條件下,每1mol氣體所占的體積為VL)上述反應的平衡時,再充入10mol的N2,根據計算,平衡應向什么方向移動?[需按格式寫計算過程,否則答案對也不給分]__________。
2NH3(g)的平衡常數__________。(設該條件下,每1mol氣體所占的體積為VL)上述反應的平衡時,再充入10mol的N2,根據計算,平衡應向什么方向移動?[需按格式寫計算過程,否則答案對也不給分]__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有關物質的轉化關系如下圖所示(部分物質和條件已略去)。A、C是常見的強酸,B是黃色非金屬單質;E是紫紅色金屬單質,G是最常見的無色液體;D、F、I是常見的氣體,D為紅棕色,D與I組成元素相同,且相對分子質量相差16。
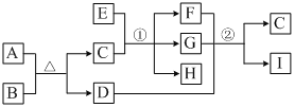
請回答下列問題:
(1)G的化學式為________。
(2)反應①的化學方程式為_____________________________。
(3)E與A的濃溶液反應的離子方程式為_________________________________。
(4)反應②的化學方程式為_____________________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com