
【題目】下列敘述不正確的是 ( )
A.金剛石的一個晶胞中含有6個碳原子。
B.12 g石墨中六元環的數目為0.5NA。
C.1個干冰晶胞的質量為![]() ×44 g。
×44 g。
D.以面心立方最密堆積形成的晶胞中金屬含有4個金屬原子。
 數學奧賽暑假天天練南京大學出版社系列答案
數學奧賽暑假天天練南京大學出版社系列答案科目:高中化學 來源: 題型:
【題目】下圖是某品牌飲用礦泉水標簽的部分內容。下列說法正確的是

A. 標簽上離子的濃度是物質的量濃度
B. 由礦泉水制蒸餾水必需使用的玻璃儀器有:圓底燒瓶、酒精燈、溫度計、冷凝管、牛角管和錐形瓶
C. 該品牌飲用礦泉水中c(Mg2+)最大值為2×10-4mol/L
D. 一瓶該品牌飲用礦泉水中SO42-的物質的量不超過l×10-5mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某蓄電池放電、充電時反應為:Fe + Ni2O3 +3H2O![]() Fe(OH)2 +2Ni(OH)2 ,下列推斷不正確的是( )
Fe(OH)2 +2Ni(OH)2 ,下列推斷不正確的是( )
A.放電時,負極上的電極反應式是:Fe+2OH--2e-=Fe (OH)2
B.放電時,每轉移2 mol 電子,正極上有1 mol Ni2O3 被氧化
C.充電時,陽極上的電極反應式是:2Ni(OH)2 -2e-+ 2OH- = Ni2O3 +3H2O
D.該蓄電池的電極必須是浸在某種堿性電解質溶液中
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】圖a是1 mol NO2和1 mol CO恰好反應生成CO2和NO過程中的能量變化示意圖;現往體積固定的密閉容器中通入等物質的量的NO2 和CO,反應中的CO和NO的濃度隨時間變化的示意圖如b圖。根據圖意回答下列問題:
a 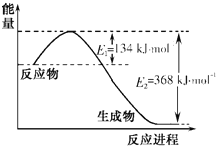 b
b
(1)寫出NO2和CO反應的熱化學方程式_____________________________________。
(2)從反應開始到平衡,用NO2濃度變化表示平均反應速率v(NO2)=_____________。
(3)此溫度下該反應的平衡常數K=___________。
(4)830K時,在密閉容器中發生下列可逆反應:CO(g)+H2O(g)![]() CO2(g)+H2(g)△H<0。試回答下列問題:
CO2(g)+H2(g)△H<0。試回答下列問題:
①若起始時c(CO)=2mol·L-1,c(H2O)=3mol·L-1,達到平衡時CO的轉化率為60%,則在該溫度下,該反應的平衡常數K=____________。
②在相同溫度下,若起始時c(CO)=1mol·L-1,c(H2O)=2mol·L-1,反應進行一段時間后,測得H2的濃度為0.5mol·L-1,則此時該反應是否達到平衡狀態______(填“是”與“否”),此時v(正)____v(逆)(填“大于”“小于”或“等于”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗裝置能達到相應實驗目的的是
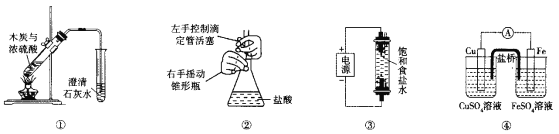
A.裝置①用于驗證反應是否有CO2生成
B.裝置②用于用標準NaOH溶液測定鹽酸濃度
C.裝置③用于制備少量含NaClO的消毒液
D.裝置④用于比較銅、鐵活潑性強弱
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關氣體體積的敘述正確的是( )
A.一定溫度和壓強下,各種氣態物質體積的大小,由構成氣體的分子大小決定
B.一定溫度和壓強下,各種氣態物質體積的大小,由構成氣體的分子數決定
C.不同的氣體,若體積不同,則它們所含的分子數也不同
D.氣體摩爾體積指1mol任何氣體所占的體積約為22.4L
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為驗證鹵素單質氧化性的相對強弱,某小組用下圖所示裝置進行實驗(夾持儀器已略去,氣密性已檢查)。
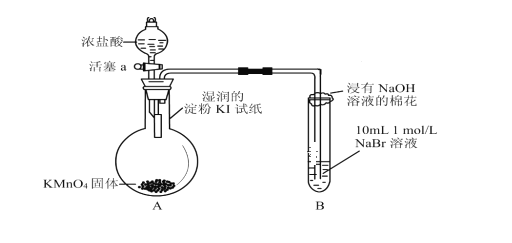
實驗時打開彈簧夾,打開活塞a,滴加濃鹽酸,使濃鹽酸與酸性KMnO4反應。
(1)驗證氯氣的氧化性強于碘的實驗現象是___________________。
(2)B中溶液發生反應的離子方程式是___________。
(3)反應完全后,可往B中加入CCl4來分離提純,該實驗過程名稱為________。
(4)實驗室制氯氣通常使用濃鹽酸與二氧化錳在加熱的條件下反應,試寫出該反應的化學方程式____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25 ℃時,將1.0 L w mol·L-1的CH3COOH溶液與0.1 mol的NaOH固體混合,充分反應后向混合液中通(加)入HCl氣體或NaOH固體。溶液pH隨通(加)入HCl或NaOH的物質的量的變化如下圖。下列敘述正確的是 ( )
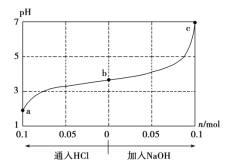
A.a、b、c對應的混合液中,水的電離程度由大到小的順序是a>b>c
B.若忽略體積變化,則25 ℃時,CH3COOH的電離平衡常數K=![]() ×10-7 mol·L-1
×10-7 mol·L-1
C.加入NaOH過程中,![]() 逐漸減小
逐漸減小
D.加入NaOH過程中,c(Na+)·c(CH3COO-)逐漸減小
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鐵和鋁是兩種重要的金屬,它們的單質及化合物有著各自的性質。在一定溫度下,氧化鐵可以與一氧化碳發生下列反應:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)
(1)該溫度下,在2 L盛有Fe2O3粉末的密閉容器中通入CO氣體,10 min后,生成了單質鐵11.2 g。則10 min內CO的平均反應速率為_________。
(2)請用上述反應中某種氣體的有關物理量來說明該反應已達到平衡狀態:
①____________________________________________________;
②_____________________________________________________。
(3)某些金屬氧化物粉末和鋁粉在鎂條的引燃下可以發生鋁熱反應。下列反應速率(v)和溫度(T)的關系示意圖中與鋁熱反應最接近的是___________________。
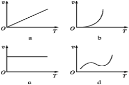
(4)寫出氫氧化鋁在水中發生堿式電離的電離方程式:___________________欲使上述體系中鋁離子濃度增加,可加入的物質是_____________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com