
| A. | 摩爾質量為17 g•mol-1 | |
| B. | 所含的分子數目約為9.03×1023 | |
| C. | 在標準狀況下體積約為33.6L | |
| D. | 溶于水制成0.5L溶液時物質的量濃度為1.5mol•L-1 |
分析 A.氨氣的相對分子質量為17,其摩爾質量為17g/mol;
B.根據N=nNA計算出含有的分子數;
C.根據V=nVm計算出氨氣在標準狀況下的體積;
D.根據c=$\frac{n}{V}$計算出所得溶液的濃度.
解答 解:A.NH3的摩爾質量與物質的量大小無關,其摩爾質量為17 g•mol-1,故A正確;
B.1.5mol NH3所含的分子數目約為:6.02×1023mol-1×1.5mol=9.03×1023,故B正確;
C.在標準狀況下體積約為:22.4L/mol×1.5mol=33.6L,故C正確;
D.溶于水制成0.5L溶液時物質的量濃度為:$\frac{1.5mol}{0.5L}$=3mol•L-1,故D錯誤;
故選D.
點評 本題考查了物質的量的計算,題目難度不大,明確物質的量與氣體摩爾體積、摩爾質量、物質的量濃度等物理量之間的關系即可解答,試題培養了學生的分析能力及化學計算能力.


科目:高中化學 來源: 題型:實驗題
| MnO2 | 觸摸試管情況 | 觀察結果 | 反應完成所需的時間 |
| 粉末狀 | 很燙 | 劇烈反應,帶火星的木條復燃 | 3.5min |
| 塊狀 | 微熱 | 反應較慢,火星紅亮但木條未復燃 | 30min |
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | O2的摩爾質量是32g | B. | 氯化鈉的相對原子質量是58.5g | ||
| C. | 1molH2O的質量是18g | D. | 1molH2O含有氫原子的個數2個 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 使用催化劑,可加快反應速率,目的是提高生產效率 | |
| B. | 使用冰箱保存食物,是利用了化學反應速率理論 | |
| C. | 化學反應速率理論是研究怎樣提高原料轉化率 | |
| D. | 化學平衡理論是研究怎樣使用有限原料多出產品 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
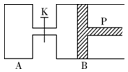 圖中,P為一可自由滑動的活塞,關閉K,分別向容器A、B中各充入1mol X、1mol Y,起始時,VA=a L,VB=0.8a L(連通管的體積忽略不計),在相同溫度和有催化劑存在的條件下,兩容器中各自發生下述反應:3X(g)+3Y(g)?2Z(g)+2W(g),達平衡時,VB=0.6a L.回答下列問題:
圖中,P為一可自由滑動的活塞,關閉K,分別向容器A、B中各充入1mol X、1mol Y,起始時,VA=a L,VB=0.8a L(連通管的體積忽略不計),在相同溫度和有催化劑存在的條件下,兩容器中各自發生下述反應:3X(g)+3Y(g)?2Z(g)+2W(g),達平衡時,VB=0.6a L.回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com