
分析 (1)根據碳單質的性質結合碳單質和硅單質性質的相似性來回答;
(2)根據蓋斯定律來計算化學反應的焓變,并書寫熱化學方程式;
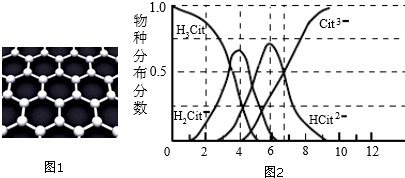
(3)①根據圖示信息確定制取NH4H2Cit的pH范圍;
②根據圖示信息知道:檸檬酸和一定量氨水反應所得溶液的pH約為6.7時,溶液中存在HCit2-、Cit3-等離子;
(4)呈中性則c(H+)=c(OH-)=10-7mol/L,c(Na+)=c(CH3COO-)=cmol/L,CH3COOH?CH3COO-+H+電離常數Ka=$\frac{c(CH{\;}_{3}COO{\;}^{-})c(H{\;}^{+})}{c(CH{\;}_{3}COOH)}$以此計算.
解答 解:(1)根據碳單質的性質可以和氧氣在點燃下反應,可以和濃硝酸加熱下反應,碳單質可以和氟氣之間反應,故答案為:ABC;
(2)已知:①CH4(g)+H2O(g)═CO(g)+3H2(g)△H=a kJ•mol-1;
②CH3OH(g)═CO(g)+2H2(g)△H=bkJ•mol-1;
根據蓋斯定律,反應CH4(g)+H2O(g)=CH3OH(g)+H2(g),可以是①-②得到,所以該反應的△H=(a-b)kJ/mol,
故答案為:CH4(g)+H2O(g)=CH3OH(g)+H2(g)△H=(a-b)kJ/mol;
(3)①根據圖示信息知道,H2Cit-存在的pH范圍大約在4左右,故答案為:3.8~4.2;
②根據圖示信息知道:檸檬酸和一定量氨水反應所得溶液的pH約為6.7時,溶液中存在HCit2-、Cit3-等離子,所以反應的離子方程式為2H3Cit+5NH3•H2O=HCit2-+Cit3-+5NH4++5H2O,故答案為:2H3Cit+5NH3•H2O=HCit2-+Cit3-+5NH4++5H2O;
(4)呈中性則c(H+)=c(OH-)=10-7mol/L,c(Na+)=c(CH3COO-)=cmol/L,所以CH3COOH?CH3COO-+H+用含b、c的代數式表示CH3COOH的電離常數Ka=$\frac{c(CH{\;}_{3}COO{\;}^{-})c(H{\;}^{+})}{c(CH{\;}_{3}COOH)}$=$\frac{10{\;}^{-7}×c}{b-c}$,
故答案為:$\frac{10{\;}^{-7}×c}{b-c}$.
點評 本題涉及碳單質的性質、電化學、熱化學等方面的知識的考查,注意知識的歸納和梳理是關鍵,難度中等.


科目:高中化學 來源: 題型:填空題
 ;
;
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
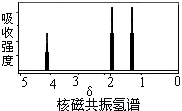
| A. | CH3COOCH2CH3 | B. | CH3CH=CHCH3 | C. | CH3CH2CH3 | D. | CH3CHOHCH3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
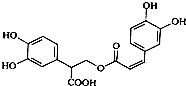
| A. | 迷迭香酸屬于芳香烴 | |
| B. | 1mol迷迭香酸最多能和含6mol H2發生加成反應 | |
| C. | 迷迭香酸可以發生水解反應、消去反應和酯化反應 | |
| D. | 1mol迷迭香酸最多能和含6mol NaOH的水溶液完全反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
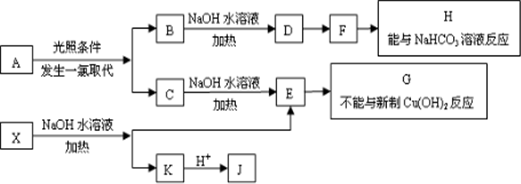
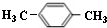 .
.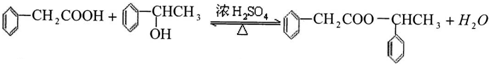 ;該反應類型是酯化反應(或取代反應).
;該反應類型是酯化反應(或取代反應).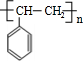 .
.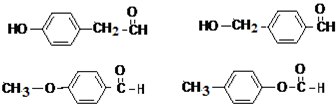 任意一種.
任意一種.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
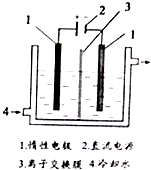 碘被稱為“智力元素”,科學合理地補充碘可防止碘缺乏病.碘酸鉀(KIO3)是國家規定的食鹽加碘劑,它的晶體為白色,可溶于水.碘酸鉀在酸性介質中與過氧化氫或碘化物作用均生成單質碘.以碘為原料,通過電解制備碘酸鉀的實驗裝置如圖所示.請回答下列問題:
碘被稱為“智力元素”,科學合理地補充碘可防止碘缺乏病.碘酸鉀(KIO3)是國家規定的食鹽加碘劑,它的晶體為白色,可溶于水.碘酸鉀在酸性介質中與過氧化氫或碘化物作用均生成單質碘.以碘為原料,通過電解制備碘酸鉀的實驗裝置如圖所示.請回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:填空題
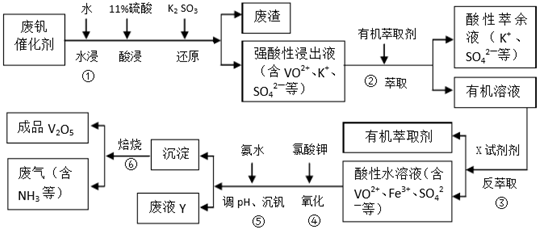
| pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| 釩沉淀率/% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.6 | 96.4 | 93.1 | 89.3 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
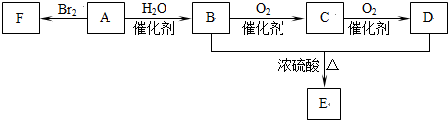
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com