
接觸法制硫酸的流程可表示如下:![]()
![]()
![]()
![]()
![]()

![]()
![]()
 zxxk.com
zxxk.com
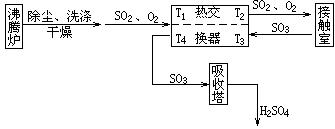
問:(1)熱交換器在制硫酸的過程中有何重要作用?
(2)若以T1、T2、T3、T4分別表示進出熱交換器的氣體溫度,且T1=80℃,T3=600℃、T4=250℃,求進入接觸室后的SO2、O2混合氣體的溫度T2(設進、出熱交換器的氣體的平均比熱均為0.8kJ/(kg??℃))。
(3)假定每天進入接觸室的混合氣體為20t,問與不用熱交換器相比較每年至少可節省多少噸含碳80%的優質煤?(已知煤的供熱效率為20%,C(s)+O2(g)=CO2(g);ΔH=-393kJ/mol)
(1)增效節能 (2)T2=430℃ (3)389.3t![]()
![]()
![]()
![]()
![]()
![]()
![]()
 zxxk
zxxk
(1)由沸騰爐導出的SO2、O2等氣體的溫度經除塵、去雜、洗滌等工藝處理后已大幅度下降,通過熱交換器后氣體的溫度又得以提高,這有利于后續反應(即由SO2合成SO3)的進行。SO2的氧化反應是放熱反應,從接觸室導出的SO3等氣體的溫度已高達600℃以上,難以被濃硫酸吸收。通過熱交換器后SO3的溫度下降了,這有利于提高濃硫酸對它的吸收效率。總而言之,熱交換器在制H2SO4的過程中具有增效節能的作用。
(2)經過熱交換器后,SO2、O2吸收的熱量=cm1(T2-80℃),SO3放出的熱量=cm2(600℃-250℃)。根據物理學原理及質量守恒定律可知,Q(吸)=Q(放),m1=m2,故cm1(T2-80℃)=cm2(600℃-250℃),即T2=430℃。
(3)若不使用熱交換器,欲使80℃的SO2、O2預熱到430℃,每年需提供的熱量為20×103kg×365×0.8kJ/(kg??℃)×(430℃-80℃)=2.04×109kJ,每千克優質煤供給的有效熱量為5240kJ/kg,使用熱交換器后每年可節約優質煤的質量為:2.04×109kJ/(5240kJ/kg)=389.3t。


 陽光課堂課時作業系列答案
陽光課堂課時作業系列答案科目:高中化學 來源:2006年五月理科綜合模擬化學部分、(第一套) 題型:022
| |||||||||||||||||||
查看答案和解析>>
科目:高中化學 來源: 題型:
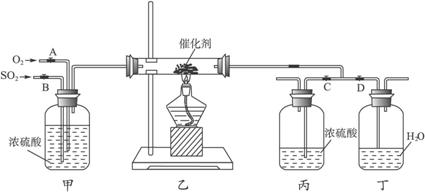
請回答下列問題:
(1)寫出FeS2與氧氣反應的化學方程式:_______________。
(2)從乙裝置中出來的氣體有_______________。
(3)寫出上圖丙裝置的作用______________________________。
(4)在裝置乙的反應器內要求氧氣的量要比二氧化硫的量多一倍左右,實驗時你是如何控制與估計的?_______________。
(5)接觸法制硫酸過程中,若反應熱都未被利用,則每生產1 ![]() 2SO3(g);ΔH=-98.3 kJ·mol-1的熱量能在生產過程中得到充分利用(其他反應熱不計),則每生產1
2SO3(g);ΔH=-98.3 kJ·mol-1的熱量能在生產過程中得到充分利用(其他反應熱不計),則每生產1
(6)本實驗增加丁裝置的目的是為了探究______________________________。
(7)本實驗設計還存在的較明顯缺陷是______________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
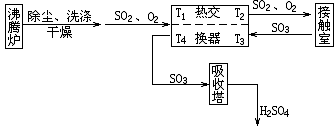
接觸法制硫酸的流程可表示如下:
】
問:(1)熱交換器在制硫酸的過程中有何重要作用?
(2)若以T1、T2、T3、T4分別表示進出熱交換器的氣體溫度,且T1=80℃,T3=600℃、T4=250℃,求進入接觸室后的SO2、O2混合氣體的溫度T2(設進、出熱交換器的氣體的平均比熱均為0.8kJ/(kg??℃))。
(3)假定每天進入接觸室的混合氣體為20t,問與不用熱交換器相比較每年至少可節省多少噸含碳80%的優質煤?(已知煤的供熱效率為20%,C(s)+O2(g)=CO2(g);ΔH=-393kJ/mol)
查看答案和解析>>
科目:高中化學 來源:2015屆重慶市高二上學期期中考試化學試卷(解析版) 題型:填空題
由于催化劑可以為化學工業生產帶來巨大的經濟效益,催化劑研究和尋找一直是受到重視的高科技領域。
(1)V2O5是接觸法制硫酸的催化劑。下圖為硫酸生產過程中2SO2
(g) + O2(g)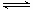 2SO3(g)
ΔH=-196.6 kJ·mol-1反應過程的能量變化示意圖。
2SO3(g)
ΔH=-196.6 kJ·mol-1反應過程的能量變化示意圖。
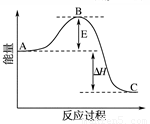
①V2O5的使用會使圖中B點 (填“升高”、“降低”)。
②一定條件下,SO2與空氣反應tmin后,SO2和SO3物質的量濃度分別為a mol/L和b mol/L,則SO2起始物質的量濃度為 mol/L;生成SO3的化學反應速率為 mol/(L·min)。
(2)下圖是一種以銅、稀硫酸為原料生產藍礬的生產流程示意圖。
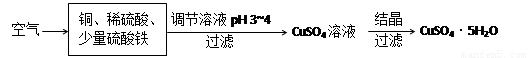
①生成CuSO4的總反應為2Cu+O2+2H2SO4=2 CuSO4+2H2O,少量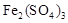 起催化作用,使反應按以下兩步完成:
起催化作用,使反應按以下兩步完成:
第一步:Cu+2Fe3+=2Fe2++Cu2+
第二步: 。(用離子方程式表示)
②調節溶液pH為3~4的目的是 ,調節時加入的試劑可以為 。(選填序號)
a.NaOH溶液 b.CuO粉末 c.Cu2(OH)2CO3 d.氨水
(3)納米TiO2是優良的光敏催化劑。工業上用鈦鐵礦制得粗TiO2;再轉化為TiCl4(l);由TiCl4(l)制取納米TiO2的方法之一是將TiCl4氣體導入氫氧火焰中(700~1000℃)進行水解。
已知:TiO2(s)+2Cl2(g)=TiCl4(l)+O2(g) ΔH=+140 kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH=-221 kJ·mol-1
①寫出TiO2和焦炭、氯氣反應生成TiCl4和CO的熱化學方程式: 。
②寫出上述TiCl4(l)制取納米TiO2的化學方程式: 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com