
在某一種分散系中慢慢滴加后一種試劑,能觀察到先沉淀后變澄清的是( )
①氯化鋁溶液中滴加氫氧化鈉溶液;②偏鋁酸鈉溶液中加鹽酸;
③氫氧化鈉溶液中滴加氯化鋁溶液;④蛋白質溶液中滴入硫酸銅溶液;
⑤氯化鋁溶液中滴加氨水;⑥硝酸銀溶液中滴加氨水;
⑦氫氧化鐵膠體滴加稀硫酸.
A. ①②⑥⑦ B. ②③⑤⑦ C. ①②④⑥ D. ③④⑤⑥
 快樂小博士鞏固與提高系列答案
快樂小博士鞏固與提高系列答案科目:高中化學 來源:廣東省2016-2017學年高二上學期期末考試化學(文)試卷 題型:選擇題
將40℃的飽和NH4Cl溶液冷卻至10℃,有NH4Cl固體析出。該過程中保持不變的是
A. 溶劑的質量 B. 溶質的質量分數
C. NH4Cl的溶解度 D. 溶液中NH4+的數目
查看答案和解析>>
科目:高中化學 來源:2017屆浙江省溫州市高三第二次選考模擬考試(2月)化學試卷(解析版) 題型:選擇題
W、X、Y、Z四種元素在周期表中的位置如圖所示,下列說法不正確的是
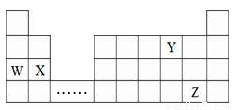
A. W、X、Y三種元素的原子半徑依次減少
B. W元素的最高價氧化物的水化物的堿性比X的強
C. 可在省略號對應的族區域尋找各種優良的催化劑
D. Z元素與水反應得到HZO,HZO只有氧化性
查看答案和解析>>
科目:高中化學 來源:2016-2017學年遼寧省六校協作體高二下學期期初化學試卷 題型:簡答題
硫酸的工業制備是一個重要的化工生產過程,但在生產過程中會產生大量污染,需要在生產工藝中考慮到綠色工藝.以硫酸工業產生的二氧化硫尾氣、氨水、石灰石、焦炭、碳酸氫銨為原料可以合成硫化鈣、硫酸銨、亞硫酸銨等物質.合成路線如下:
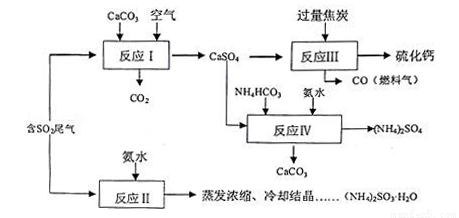
(1)寫出反應Ⅰ的化學方程式________________________.
(2)反應Ⅲ中每生成lmol硫化鈣理論上轉移電子數________;為充分利用副產品CO,有人提出以熔融的K2C03為電解質,設計燃料電池,請寫出此電池的負極反應_____________.
(3)為檢驗反應Ⅱ得到的產品是否因部分被氧化而變質,需選擇的化學試劑有__________________.
(4)根據合成流程,可以循環利用的是____________.
(5)(NH4)2SO3溶液可用于電廠產生的煙道氣的脫氮,將氮氧化物轉化為氮氣,同時生成一種氮肥,形成共生系統.寫出二氧化氮與亞硫酸銨反應的離子方程式___________________.
查看答案和解析>>
科目:高中化學 來源:2016-2017學年遼寧省六校協作體高二下學期期初化學試卷 題型:選擇題
可以鑒別乙酸溶液、葡萄糖溶液、蔗糖溶液的試劑是( )
A. 新制氫氧化銅懸濁液 B. 銀氨溶液 C. 石蕊試液 D. 碳酸鈉溶液
查看答案和解析>>
科目:高中化學 來源:2016-2017學年遼寧省六校協作體高二下學期期初化學試卷 題型:選擇題
某有機物的結構為,這種有機物不可能具有的性質是( )
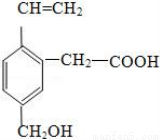
A. 能跟NaOH溶液反應 B. 能使酸性KMnO4溶液褪色
C. 能發生酯化反應 D. 能發生水解反應
查看答案和解析>>
科目:高中化學 來源:2017屆陜西省寶雞市高三教學質量檢測(一)理綜化學試卷(解析版) 題型:簡答題
(1)寫出醋酸在水溶液中的電離方程式 。若某溫度下,CH3COOH(aq)與NaOH(aq)反應的△H=" -" 46.8kJ·mol-1,HCl(aq)與NaOH(aq)反應的△H=" -" 55.6 kJ·mol-1,則CH3COOH在水溶液中電離的△H= kJ·mol-1。
(2)某溫度下,實驗測得0.1mol·L-1醋酸電離度約為1.5%,則該溫度下0.1mol·L-1CH3COOH的電離平衡常數K=________(列出計算式,已知電離度 )
)
(3)近年來化學家研究開發出用乙烯和乙酸為原料、雜多酸作催化劑合成乙酸乙酯的新工藝,不必生產乙醇或乙醛做中間體,使產品成本降低,具有明顯經濟優勢。其合成的基本反應如下:
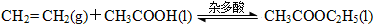
下列描述能說明乙烯與乙酸合成乙酸乙酯的反應已達化學平衡的是 。
A.乙烯、乙酸、乙酸乙酯的濃度相同 |
B.酯化合成反應的速率與酯分解反應的速率相等 |
C.乙烯斷開1mol碳碳雙鍵的同時乙酸恰好消耗1mol |
D.體系中乙烯的百分含量一定 |
(4)在n(乙烯)與n(乙酸)物料比為1的條件下,某研究小組在不同壓強下進行了在相同時間點乙酸乙酯的產率隨溫度的變化的測定實驗,實驗結果如圖所示。回答下列問題:
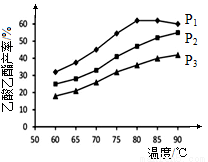
① 溫度在60~80℃范圍內,乙烯與乙酸酯化合成反應速率由大到小的順序是 [用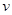 (P1)、
(P1)、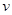 (P2)、
(P2)、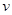 (P3)分別表示不同壓強下的反應速率],分析其原因為 。
(P3)分別表示不同壓強下的反應速率],分析其原因為 。
②壓強為P1MPa、溫度60℃時,若乙酸乙酯的產率為30℅,則此時乙烯的轉化率為 。
③在壓強為P1MPa、溫度超過80℃時,乙酸乙酯產率下降的原因可能是_________。
④根據測定實驗結果分析,較適宜的生產條件是 (填出合適的壓強和溫度)。為提高乙酸乙酯的合成速率和產率,可以采取的措施有 (任寫出一條)。
查看答案和解析>>
科目:高中化學 來源:2017屆安徽省A10聯盟高三下學期開年考試理綜化學試卷(解析版) 題型:選擇題
A、B、 C、D是原子序數依次增大的五種短周期主族元素。B、C、E最外層電子數之和為11;A 原子核外最外層電子數是次外層的2倍;C是同周期中原子半徑最大的元素;工業上一般通過電解氧化物的方法制備D的單質;E單質是制備太陽能電池的重要材料。下列說法正確的是( )
A. 簡單離子半徑:B>C
B. 最高價氧化物對應水化物的酸性: A<E
C. 工業上不用電解氯化物的方法制備單質D是由于其氯化物的熔點高
D. 相同質量的C和D單質分別與足量稀鹽酸反應,前者生成的氫氣多
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河北省石家莊市高一上學期期末考試化學試卷(解析版) 題型:選擇題
向含有FeBr2和FeI2各0.4mol的混合稀溶液中,逐滴滴加稀氯水至過量,反應分三個階段進行,各階段消耗氯氣的物質的量之比依次是
A. 2:1:1 B. 1:2:1 C. 2:1:2 D. 1:1:1
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com