
工業上以軟錳礦為原料,利用硫酸亞鐵制備高純二氧化錳的流程如下: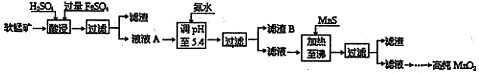
某軟錳礦的主要成分為MnO2,還含有Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物。部分陽離子以氫氧化物或硫化物的形式完全沉淀時溶液的pH見下表。
回答下列問題:
(1)硫酸亞鐵在酸性條件下將MnO2還原為MnSO4,酸浸時發生的主要反應的離子方程式為 。
(2)調節pH時不用氫氧化鈉原因是: ,理論上,調節pH的最小值為 ,濾渣B的主要成分是 。
(3)加入MnS的目的是除去 雜質。
(4)堿性鋅錳電池中,MnO2參與的電極反應方程式為 。回收廢舊堿性錳電池中的錳,可向含錳混合物中加入一定量的稀硫酸、稀草酸,并不斷攪拌至無氣泡為止,其主要反應為:2MnO(OH)+MnO2 +2H2C2O4 +3H2SO4=3MnSO4 +4CO2 ↑+6H2O,該方法的優點是 。
 口算心算速算應用題系列答案
口算心算速算應用題系列答案 同步拓展閱讀系列答案
同步拓展閱讀系列答案科目:高中化學 來源: 題型:填空題
(1)濃度均為0.01 mol·L-1的8種溶液:①HNO3 ②H2SO4 ③CH3COOH ④Ba(OH)2 ⑤NaOH
⑥CH3COONa ⑦KCl ⑧NH4Cl,這些溶液pH由小到大的順序是(填寫編號) 。
(2)pH=2的某酸HnA(An+為酸根)與pH=12的某堿B(OH)m混合,恰好反應生成正鹽,混合液pH=8。
①反應生成的正鹽的化學式為 。
②該鹽中 離子一定能水解,其第一步水解的離子方程式為 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
有0.1 mol/L的鹽酸溶液(a)、硫酸溶液(b)、醋酸溶液(c)各50 mL,試比較:
(1)三種酸的氫離子濃度由大到小的順序是________(填字母代號,下同);三種酸的pH由大到小的順序是________。
(2)三種酸跟足量的鋅反應,開始時產生H2的速率由大到小的順序是________。(不考慮Zn的純度及表面積等因素)
(3)三種酸跟足量的鋅反應產生H2的體積由大到小的順序是________。
(4)三種酸分別跟0.1 mol/L的NaOH溶液中和,消耗NaOH溶液體積由大到小的順序是________。
(5)三種酸分別跟50 mL 0.1 mol/L的NaOH溶液反應后,溶液的pH由大到小的順序是________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
工業上利用鋅焙砂(主要含ZnO、ZnFe2O4,還含有少量CaO、FeO、CuO、NiO等氧化物)制取金屬鋅的流程如圖所示。回答下列問題: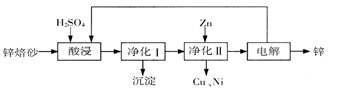
(1)酸浸時ZnFe2O4會生成兩種鹽,該反應的化學方程式為
(2)凈化I操作分為兩步:第一步是將溶液中少量的Fe2+氧化;第二步是控制溶液pH,使Fe3+轉為Fe(OH)3沉淀。
①寫出酸性條件下H2O2與Fe2+反應的離子方程式
②250C時,pH=3的溶液中,c (Fe3+)= mol/L(已知25℃,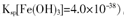 。
。
③凈化I生成的沉淀中還含有溶液中的懸浮雜質,溶液中的懸浮雜質被共同沉淀的原因是 。
(3)若沒有凈化II操作,則對鋅的制備帶來的影響是 。
(4)本流程中可以循環利用的物質除鋅外還有 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
化學學科中的化學平衡、電離平衡、水解平衡和溶解平衡均符合勒夏特列原理。請回答下列問題:
(1)常溫下,取pH=2的鹽酸和醋酸溶液各100 mL,向其中分別加入適量的Zn粒,反應過程中兩溶液的pH變化如圖所示。則圖中表示醋酸溶液中pH變化曲線的是________(填“A”或“B”)。設鹽酸中參加反應的Zn粒質量為m1,醋酸溶液中參加反應的Zn粒質量為m2,則m1________m2(選填“<”、“=”或“>”)。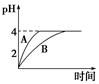
(2)已知常溫下Cu(OH)2的Ksp=2×10-20。又知常溫下某CuSO4溶液里c(Cu2+)=0.02 mol·L-1,如果要生成Cu(OH)2沉淀,則應調整溶液pH大于________;要使0.2 mol·L-1的CuSO4溶液中Cu2+沉淀較為完全(使Cu2+濃度降至原來的千分之一),則應向溶液里加NaOH溶液,使溶液pH為________。
(3)10 ℃時加熱NaHCO3飽和溶液,測得該溶液的pH發生如下變化:
| 溫度/℃ | 10 | 20 | 30 | 加熱煮沸后冷卻到50 ℃ |
| pH | 8.3 | 8.4 | 8.5 | 8.8 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
利用廢舊鍍鋅鐵皮可制備磁性Fe3O4膠體粒子及副產物ZnO。制備流程圖如下:
已知:Zn及其化合物的性質與Al及其化合物的性質相似,請回答下列問題:
(1)用NaOH溶液處理廢舊鍍鋅鐵皮的作用有________。
| A.去除油污 | B.溶解鍍鋅層 | C.去除鐵銹 | D.鈍化 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(1)在25℃時,向濃度均為0.01 mol·L-1的MgCl2和AlCl3混合溶液中逐滴加入氨水,先生成________沉淀(填化學式),生成該沉淀的離子方程式為_____________________。(已知25℃時Ksp[Mg(OH)2]=1.8×10-11,Ksp[Al(OH)3]=3×10-34。)
(2)某溫度(t℃)時,測得0.01 mol·L-1的NaOH溶液的pH=11。在此溫度下,將pH=2的H2SO4溶液VaL與pH=12的NaOH溶液VbL混合,若所得混合液為中性,則Va︰Vb=________。
(3)在25℃時,將c mol·L-1的醋酸溶液與0.02 mol·L-1NaOH溶液等體積混合后溶液剛好呈中性,用含c的代數式表示CH3COOH的電離常數Ka=________。
(4)(2013·山東高考)25℃時,H2SO3 HSO3-+H+的電離常數Ka=1×10-2mol·L-1,則該溫度下NaHSO3水解反應的平衡常數Kb=________mol·L-1,若向NaHSO3溶液中加入少量的I2,則溶液中
HSO3-+H+的電離常數Ka=1×10-2mol·L-1,則該溫度下NaHSO3水解反應的平衡常數Kb=________mol·L-1,若向NaHSO3溶液中加入少量的I2,則溶液中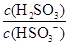 將________(填“增大”、“減小”或“不變”)。
將________(填“增大”、“減小”或“不變”)。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
現有濃度均為0.1 mol·L-1的下列溶液:
①硫酸、②醋酸溶液、③氫氧化鈉溶液、④氯化銨溶液、⑤醋酸銨溶液、⑥硫酸銨溶液、⑦硫酸氫銨溶液、⑧氨水,請回答下列問題:
(1)①、②、③、④四種溶液中由水電離出的H+濃度由大到小的順序是(填序號)________。
(2)④、⑤、⑦、⑧四種溶液中NH4+濃度由大到小的順序是(填序號)________。
(3)將③和④等體積混合后,混合液中各離子濃度關系正確的是________。
| A.c(Na+)=c(Cl-)>c(OH-)>c(NH4+) |
| B.c(Na+)=0.1 mol·L-1 |
| C.c(Na+)+c(NH4+)=c(Cl-)+c(OH-) |
| D.c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
常溫下,將0.05 mol·L-1鹽酸溶液和未知濃度的NaOH溶液以1:2的體積比混合,所得溶液的pH=12。用上述NaOH溶液12.5 mL和pH=3的某一元弱酸HA溶液20.0mL恰好完全反應生成NaA。
(1)此一元弱酸的物質的量濃度為 ;
(2)此條件下該一元弱酸的電離平衡常數為 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com