
一定條件下,在體積為10L的密閉容器中,1molX和1molY進行反應:2X(g)+Y(g) Z(g),60s達到平衡,生成0.3molZ,下列說法正確的是( )
Z(g),60s達到平衡,生成0.3molZ,下列說法正確的是( )
| A.以X濃度變化表示的反應速率為0.001mol/(L·s) |
B.將容器體積變為20L,Z的平衡濃度變為原來的 |
| C.若增大壓強,則物質Y的轉化率減小 |
| D.若升高溫度,X的體積分數增大,則該反應的△H>0 |
科目:高中化學 來源: 題型:單選題
已知:(NH4)2CO3(s)=NH4HCO3(s)+NH3(g) △H="74.9" kJ·mol-1,下列說法中正確的是
| A.該反應中熵變、焓變皆大于0 |
| B.該反應是吸熱反應,因此一定不能自發進行 |
| C.碳酸鹽分解反應中熵增加,因此任何條件下所有碳酸鹽分解一定自發進行 |
| D.能自發進行的反應一定是放熱反應,不能自發進行的反應一定是吸熱反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
在25℃時,密閉容器中X、Y、Z三種氣體的初始濃度和平衡濃度如下表:
| 物質 | X | Y | Z |
| 初始濃度(mol/L) | 0.1 | 0.2 | 0 |
| 平衡濃度(mol/L) | 0.05 | 0.05 | 0.1 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
向某密閉容器中加入0.6 mol A、0.2 mol C和一定量的B三種氣體。一定條件下發生反應,各物質濃度隨時間變化如甲圖所示[其中t0-t1階段c(B)未畫出]。t2時刻后改變條件反應體系中反應速率隨時間變化的情況如乙圖所示,且四個階段都各改變一種條件并且改變的條件均不相同。下列說法正確的是( )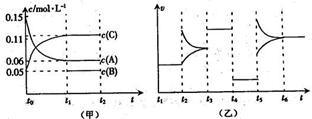
 A.反應的方程式為3A(g)+B(g) 2C(g)
A.反應的方程式為3A(g)+B(g) 2C(g)
B.t3~t4,t4~t5,t5~t6各階段可能改變的條件依次為:加催化劑,降低反應溫度,增大壓強
C.B的起始物質的量為0.08 mol
D.若t1="10" s,A在t0~t1時間段的反應速率為0.00225 mol·L-1·s-1
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
在一定條件下,可逆反應:N2+3H2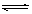 2NH3(正反應是放熱反應)達到平衡,當單獨改變下列條件后,有關敘述錯誤的是
2NH3(正反應是放熱反應)達到平衡,當單獨改變下列條件后,有關敘述錯誤的是
| A.加催化劑,V(正)、V(逆)都發生變化且變化的倍數相等 |
| B.加壓,V(正)、V(逆)都增大,且V(正)增大的倍數大于V(逆)增大的倍數 |
| C.降溫,V(正)、V(逆)都減小,且V(正)減小的倍數小于V(逆)減小的倍數 |
| D.加入氬氣,V(正)、V(逆)都增大,且V(正)增大的倍數大于V(逆)增大的倍數 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
中學化學涉及多種常數,下列說法正確的是
A.兩種物質反應,不管怎樣書寫化學方程式,平衡常數不變
B.某溫度下,2L密閉容器中加入4 mol a和2 mol b發生反應:3A(g) +2B(g)  4C(1)+2D( g)。平衡時測得n(C)="1.6mol" ,反應的化學平衡常數表達式為
4C(1)+2D( g)。平衡時測得n(C)="1.6mol" ,反應的化學平衡常數表達式為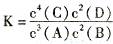
C.溫度一定時,當溶液中。( Ag+)·c( Cl-)等于Ksp值時,此溶液為AgCI的飽和溶液
D.難溶電解質AB2飽和溶液中,c(A2+)=xmol·L-1, c(B-)="y" mo·L-1,則Ksp值為4xy2
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
人體血液內的血紅蛋白(Hb)易與O2結合生成HbO2,因此具有輸氧能力.CO吸入肺中發生反應:CO+HbO2? O2+HbCO,37℃時,該反應的平衡常數K=220。若HbCO的濃度達到HbO2濃度的0.02倍,會使人智力受損.據此下列結論錯誤的是( )
A.CO與HbO2反應的平衡常數K=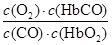 |
| B.人體吸入的CO越多,與血紅蛋白結合的O2越少 |
| C.當吸入的CO與O2濃度之比大于或等于0.02時,人的智力才會受損 |
| D.把CO中毒的病人放入高壓氧倉中解毒,其原理是使上述平衡向左移動 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
一定條件下,分別對反應C(S)+CO2(g) 2CO(g)(正反應吸熱)進行如下操作(只改變該條件):
①升高反應體系的溫度;②增加反應物C的用量;
③縮小反應體系的體積;④減少體系中CO的量。
上述措施中一定能使反應的反應速率顯著加快的是( )
| A.①②③④ | B.①③④ | C.①② | D.①③ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com