
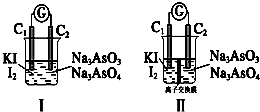
分析 A、B、C、D、E五種短周期主族元素,其原子序數依次增大,原子的核外電子層數:B=C=2A,則A處于第一周期,B、C處于第二周期,則A為H元素;B元素的主要化合價:最高正價+最低負價=2,B處于ⅤA族,則B為N元素;原子的最外層電子數:B+D=8,則D的最外層電子數為8-5=3,D的原子序數大于N元素,則D為Al元素;C是周期表中非金屬性最強的元素,則C為F元素;E是同周期中半徑最小的原子,E處于第三周期,則E為Cl元素,據此進行解答(1)~(5);
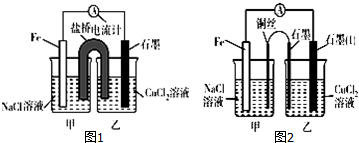
(6)①甲組向圖Ⅰ燒杯中逐滴加入適量濃鹽酸,發生氧化還原反應,不發生原電池反應;
②乙組向圖ⅡB燒杯中逐滴加入適量濃鹽酸或40%NaOH溶液,發生原電池反應,A中發生I2+2e-═2I-,為正極反應,而B中As化合價升高,發生氧化反應,以此分析.
解答 解:A、B、C、D、E五種短周期主族元素,其原子序數依次增大,原子的核外電子層數:B=C=2A,則A處于第一周期,B、C處于第二周期,則A為H元素;B元素的主要化合價:最高正價+最低負價=2,B處于ⅤA族,則B為N元素;原子的最外層電子數:B+D=8,則D的最外層電子數為8-5=3,D的原子序數大于N元素,則D為Al元素;C是周期表中非金屬性最強的元素,則C為F元素;E是同周期中半徑最小的原子,E處于第三周期,則E為Cl元素,
(1)實驗室制取氯氣是二氧化錳和濃鹽酸共熱,反應的離子方程式為:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2H2O+C12↑,
故答案為:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2H2O+C12↑;
(2)A、B分別為N、H元素,N和H組成的離子化合物一定含有銨根離子,可能為:NH4H 或( NH4)3N、NH4N3,
故答案為:NH4H(或( NH4)3N、NH4N3);
(3)由D元素形成的氫氧化物為Al(OH)3,Al(OH)3和NaOH反應的離子方程式為:Al(OH)3+OH-=AlO2-+H2O;
a.金屬性強弱與兩種元素單質的硬度和熔、沸點無關,故a錯誤;
b.金屬元素的最高價氧化物對應水化物的堿性越弱,金屬性越弱,故b正確;
c.金屬性越強,單質與同濃度鹽酸反應的劇烈程度就越大,故c正確
d.金屬性強弱與化合價高低無關(即與失去電子數多少),與難易程度有關,故d錯誤;
故答案為:Al(OH)3+OH-=AlO2-+H2O;bc;
(4)由B、C元素組成的化合物BC3,為NF3,該化合物具有強氧化性,與水反應生成兩種酸HNO3、HF和一種無色氣體,該氣體常溫下遇空氣變紅棕色為NO,該化合物與水反應的化學方程式:3NF3+5H2O=HNO3+2NO↑+9HF;
故答案為:3NF3+5H2O=HNO3+2NO↑+9HF;
(5)A、B和C三種元素組成的鹽為NH4F,銨根離子部分水解,溶液顯示酸性,檢驗銨根離子的反應為:取少量該鹽溶液于一支試管中,加入過量的濃氫氧化鈉溶液,加熱,用濕潤的紅色石蕊試紙檢驗,若變藍,則有NH4+,反之無NH4+,涉及的反應為:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O,
故答案為:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O;
(6)①甲組操作時,兩個電極均為碳棒,不發生原電池反應,則微安表(G)指針不發生偏轉,
故答案為:氧化還原反應在電解質溶液中直接進行,沒有電子沿導線通過;
②乙組向圖ⅡB燒杯中逐滴加入適量濃鹽酸或40%NaOH溶液,發生原電池反應,A中發生I2+2e-═2I-,為正極反應,而B中As化合價升高,發生氧化反應,添加了陽離子交換膜,
故答案為:陽.
點評 本題考查了位置、結構與性質關系的綜合應用,題目難度中等,試題知識點較多、綜合性較強,充分考查學生的分析、理解能力及靈活應用基礎知識的能力,注意熟練掌握原子結構與元素周期表、元素周期律的關系.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
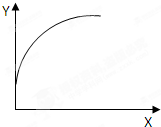 在一密閉容器中通入A、B兩種氣體,在一定條件下反應:2A(g)+B(g)=2C(g)+Q(Q>0),當達到平衡后,改變一個條件(X),下列量(Y)一定符合圖中曲線的是( )
在一密閉容器中通入A、B兩種氣體,在一定條件下反應:2A(g)+B(g)=2C(g)+Q(Q>0),當達到平衡后,改變一個條件(X),下列量(Y)一定符合圖中曲線的是( )| X | Y | |
| A | 溫度 | 混合氣體平均相對分子質量 |
| B | 再加入C | A的質量分數 |
| C | 再加入A | B的轉化率 |
| D | 壓強 | B的濃度 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH2=CH-COOH | B. | CH2=CH-COOCH3 | C. | CH3CH2OH | D. | CH2=CH-CH2OH |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
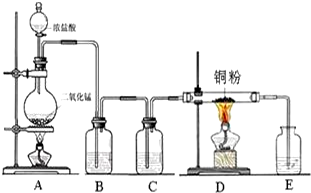 實驗室里用如圖所示裝置制取純凈的無水CuCl2.試回答下列問題:
實驗室里用如圖所示裝置制取純凈的無水CuCl2.試回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 實驗室用如圖所示裝置制取乙烯.
實驗室用如圖所示裝置制取乙烯.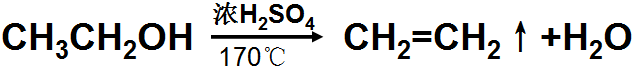
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 元素代號 | X | Y | Z | L | M | Q |
| 原子半徑/nm | 0.160 | 0.143 | 0.102 | 0.099 | 0.077 | 0.074 |
| 主要化合價 | +2 | +3 | +6、-2 | +7、-1 | +4、-4 | -2 |
| A. | 單質與氫氣化合的難易程度:Z>L | |
| B. | Y的氧化物對應的水化物不能溶于過量的氨水 | |
| C. | Z單質在氧氣中燃燒生成ZO3 | |
| D. | L、Q形成的簡單離子核外電子數相等 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
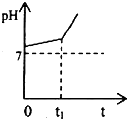 運用化學反應原理研究溶液的組成與性質具有重要意義.請回答下列問題:
運用化學反應原理研究溶液的組成與性質具有重要意義.請回答下列問題:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com