
| X | ||
| Y | Z | W |
| T |
| A. | X、W、Z元素的原子半徑依次減小 | |
| B. | Y、Z、W元素在自然界中均不能以游離態存在,它們的最高價氧化物的水化物的酸性依次遞增 | |
| C. | YX2晶體熔化、液態WX3氣化均需克服分子間作用力 | |
| D. | 根據元素周期律,可以推測T2X3具有氧化性和還原性 |
分析 X、Y、Z、W為短周期元素,由元素周期表可知:X應位于第二周期,且應處于周期表中右半部分,W與X處于同一主族,且W元素原子的核電荷數為X元素的2倍,那么X為O,W為S,可知Y為Si、Z為P、T為As,結合元素周期律與元素化合物結構與性質解答.
解答 解:X、Y、Z、W為短周期元素,由元素周期表可知:X應位于第二周期,且應處于周期表中右半部分,W與X處于同一主族,且W元素原子的核電荷數為X元素的2倍,那么X為O,W為S,可知Y為Si、Z為P、T為As.
A.電子層數越多,原子半徑越大,電子層數相同時,原子序數越大,原子半徑越小,所以Z、W、X元素的原子半徑依次減小,故A錯誤;
B.S元素在自然界中存在游離態單質,常在火山口附近,即W在自然界中存在游離態,故B錯誤;
C.SiO2晶體熔化克服共價鍵,液態SO3分子之存在分子間作用力,氣化需克服分子間作用力,故C錯誤;
D.As2O3中As為+3價,為之間價態,所以As2O3具有氧化性和還原性,故D正確;
故選D.
點評 本題考查原子結構和元素周期律,涉及元素周期表結構、原子結構、元素周期律、化學鍵等知識點,正確判斷元素是解本題關鍵,知道非金屬性、氫化物的穩定性及原子半徑大小比較規律,題目難度不大.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 中子數為20的氯原子符號:20Cl | |
| B. | HClO的結構式:H-Cl-O | |
| C. | HClO4的電離方程式:HClO4═H++ClO4- | |
| D. | Cl-的結構示意圖: |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向稀鹽酸中加入少量蒸餾水,鹽酸中氫離子濃度降低 | |
| B. | 實驗室中常用排飽和食鹽水的方式收集氯氣 | |
| C. | 打開汽水瓶,有氣泡從溶液中冒出 | |
| D. | 對熟石灰的懸濁液加熱,懸濁液中固體質量增加 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 80mL 10mol/L的濃鹽酸與足量的MnO2加熱反應,產生Cl2分子數為0.2NA | |
| B. | 25g質量分數為68%的H2O2水溶液中含氧原子數目為NA | |
| C. | 1L 1mol/L的Fe2(SO4)3溶液中含有的SO42-離子數為3NA | |
| D. | 常溫常壓下,等質量的CO和N2中含有的原子數目均為2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | HCN的結構式:H-C≡N | |
| B. | HClO的電子式: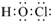 | |
| C. | 中子數為16的硫原子符號為:${\;}_{32}^{16}$S | |
| D. | Na+的離子結構示意圖: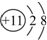 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com