
【題目】元素X、Y、Z和W在周期表中的位置如圖所示,其中X、Y、Z均為短周期元素,且X、Y、W原子的最外層電子數之和為13。下列說法不正確的是( )
X | Y | ||
Z | |||
W |
A. 原子半徑:![]()
B. W的最高價氧化物對應的水化物可能為強堿
C. 上述四種元素可形成化合物![]()
D. 一定條件下,Z單質與X的氫化物及Y的氫化物均能反應
【答案】B
【解析】
X、Y、Z均為短周期元素,設X的最外層電子數為a,則Y的最外層電子數為a+1,W的最外層電子數為a,所以有3a+1=13,解得a=4,所以X為碳元素,W為鍺元素,Y為氮元素,Z為氯元素。
A.進行原子半徑的大小比較,通常首看電子層數,其次看核電荷數,所以原子半徑:r(W)>r(Z)>r(X)>r(Y),A項正確;
B.W的最高價氧化物對應的水化物為H4GeO4或Ge(OH)4,根據對角線規則,該物質是兩性物質,不可能為強堿,B項錯誤;
C.上述四種元素可能形成化合物C3N4、GeCl4,C項正確;
D.一定條件下,氯氣與碳的氫化物(烴)發生取代或加成反應,與氮的氫化物(比如氨氣)可發生氧化還原反應等,D項正確;
所以答案選擇B項。


 名師指導期末沖刺卷系列答案
名師指導期末沖刺卷系列答案 開心蛙口算題卡系列答案
開心蛙口算題卡系列答案科目:高中化學 來源: 題型:
【題目】下列是某同學對相應反應的離子方程式所作的評價,其中對應的評價合理的是( )
編號 | 化學反應 | 離子方程式 | 評價 |
A | 把MgSO4溶液滴入Ba(OH)2溶液 | Mg2++2OH-=Mg(OH)2↓ | 正確 |
B | 氧化銅與稀鹽酸反應 | CuO+2H+=Cu2++H2O | 錯誤,不反應 |
C | 向FeCl2溶液中通入氯氣 | Fe2++Cl2=Fe3++2Cl- | 錯誤,電荷不守恒 |
D | 向沸水滴入飽和氯化 鐵溶液 | Fe3++3H2O | 正確 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】銅片與濃硫酸反應后,銅片表面變黑,為研究該黑色物質的成分,某化學興趣小組查閱資料得知:該黑色物質可能含CuO、CuS、Cu2S及有可能被黑色掩蓋顏色的Cu2O(磚紅色)。該興趣小組通過圖1所示實驗流程對該黑色物質的成分進行探究,其中步驟![]() 在圖2裝置中進行。
在圖2裝置中進行。
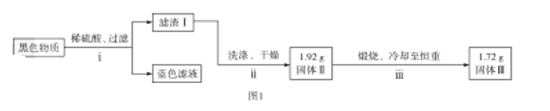
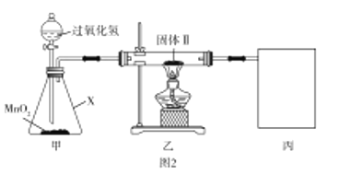
已知:Cu2O在酸中不穩定,生成Cu2+和Cu;銅的硫化物難溶于稀硫酸。回答下列問題:
(1)若測得濾渣Ⅰ中含Cu,寫出“黑色物質”中加入稀硫酸發生反應生成Cu的離子方程式:__________。
(2)檢驗圖2中整套裝置氣密性的方法是__________,儀器![]() 的名稱是__________。
的名稱是__________。
(3)步驟![]() 中檢驗固體Ⅱ洗滌干凈的方法是__________。
中檢驗固體Ⅱ洗滌干凈的方法是__________。
(4)通過計算確定固體Ⅱ中一定存在的硫化物是__________(寫化學式)。
(5)為防止環境污染,丙裝置可選用下列裝置中的__________(填標號)
a.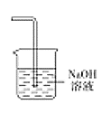 b.
b.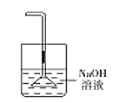 c.
c.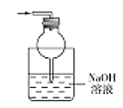 d.
d.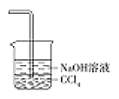
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關說法不正確的是( )
A. 人們最早先根據味道來獲得樸素的酸、堿概念:一切有酸味的物質都是酸,一切有澀味的物質都是堿。
B. 波義耳基于指示劑變色來分辨酸堿:酸一定能使石蕊變紅,堿一定能使石蕊變藍。
C. 地球上最大規模的化學反應是植物的光合作用,人類利用氮肥的最有效的反應是合成氨反應。
D. 酸堿質子理論:凡是能給出![]() 的物質就是酸,凡是能結合
的物質就是酸,凡是能結合![]() 的物質就是堿,適用水溶液,也適用非水溶液或無水條件。
的物質就是堿,適用水溶液,也適用非水溶液或無水條件。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列除去括號內的雜質選用的試劑及方法均正確的是( )
序號 | 被提純的物質 | 除雜試劑 | 分離方法 |
A | 溴化鈉溶液(碘化鈉) | 氯水、四氯化碳 | 萃取、分液 |
B | 碳酸氫鈉溶液(碳酸鈉) | 石灰水 | 過濾 |
C |
| 碳酸鈉溶液 | 洗氣 |
D | 酒精(水) | 生石灰 | 蒸餾 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室制備并收集干燥、純凈氯氣的裝置如圖所示:

(1)寫出實驗室制備Cl2的化學方程式:___。
(2)寫出指定試劑的名稱,C__,D__。
(3)C的作用是__,D的作用是__,F的作用是___。
(4)檢驗氯氣是否收集滿的操作:___。
(5)實驗室除了可用二氧化錳和濃鹽酸反應制取氯氣外,還可以用其他很多方法制取氯氣,其中用高錳酸鉀和濃鹽酸反應制備氯氣的化學方程式可表示為:2KMnO4+16HCl(濃)=2KCl+2MnCl2+5Cl2↑+8H2O,其中該反應中HCl的作用是___,若反應產生0.5mol Cl2,則消耗的氧化劑的物質的量為___mol,反應轉移的電子數是___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法不正確的是( )
A. 干冰升華和液氯氣化時,都只需克服分子間作用力
B. 硫酸氫鈉晶體溶于水,需要克服離子鍵和共價鍵
C. ![]() 和
和![]() 中,每個原子的最外層都具有8電子穩定結構
中,每個原子的最外層都具有8電子穩定結構
D. 石墨轉化為金剛石時,既有共價鍵的斷裂,又有共價鍵的形成
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知有以下物質相互轉化。其中A為金屬試回答:

(1)寫出B的化學式________________,D的化學式________________。
(2)寫出由D轉變成H的化學方程式________________。
(3)寫出向G溶液加入A的有關離子反應方程式________________。
(4)寫出E轉變為F的實驗現象為:_________________________化學方程式:___________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為了證明在實驗室制備得到的Cl2中會混有HCl,甲同學設計了如圖所示的實驗裝置,按要求回答下列問題。

(1)請根據甲同學的示意圖,所需實驗裝置從左至右的連接順序:裝置②→__________。
(2)裝置②中主要玻璃儀器的名稱__________、__________、__________。
(3)實驗室制備Cl2的離子方程式為____________。
(4)裝置③中Cu的作用__________(用化學方程式表示)。
(5)乙同學認為甲同學實驗設計仍然存在缺陷,不能證明最終通入AgNO3溶液中的氣體只有一種。為此,乙同學提出氣體通入裝置①之前,要加裝一個檢驗裝置⑤,以證明最終通入AgNO3溶液中的氣體只有一種。你認為裝置⑤應放入__________。
(6)丙同學看到甲同學設計的裝置后提出無需多加裝置,只需將原來燒杯中的AgNO3溶液換成紫色石蕊試液,如果觀察到__________的現象,則證明制Cl2時有HCl揮發出來。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com