
研究發現,可以用石墨作陽極、鈦網作陰極、熔融CaF2—CaO作電解質,利用圖示裝置獲得金屬鈣,并以鈣為還原劑還原二氧化鐵制備金屬鈦。下列說法中正確的是
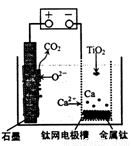
A.將熔融CaF2-CaO換成Ca(NO3)2溶液也可以達到相同目的
B.陽極的電極反應式為:C+2O2--4e-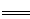 CO2↑
CO2↑
C.在制備金屬鈦前后,整套裝置中CaO的總量減少
D.若用鉛蓄電池作該裝置的供電電源,“+"接線柱應連接Pb電極
B
【解析】
試題分析:金屬鈣很活潑,會和水反應,因此不能用溶液作電解質,A選項錯誤;用石墨作陽極、鈦網作陰極、熔融CaF2-CaO作電解質,陽極發生氧化反應,陰極析出鈣金屬發生還原反應,陽極圖示產物可可知,陽極生成二氧化碳氣體,是電解質中的氧離子失電子生成氧氣,氧氣和陽極石墨反應生成的二氧化碳,所以電極反應為:2O2--4e-=O2↑,C+2O2--4e-=CO2↑,B選項正確,制備TiO2時,在電解槽發生如下反應:2CaO═2Ca+O2↑,2Ca+TiO2  Ti+2CaO,由此可見,CaO的量不變,C選項錯誤;若用鉛蓄電池作該裝置的供電電源,“+"接線柱應連接PbO2電極,D選項錯誤。
Ti+2CaO,由此可見,CaO的量不變,C選項錯誤;若用鉛蓄電池作該裝置的供電電源,“+"接線柱應連接PbO2電極,D選項錯誤。
考點:考查電化學知識。


 勵耘書業暑假銜接寧波出版社系列答案
勵耘書業暑假銜接寧波出版社系列答案科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解


| ||
| ||
查看答案和解析>>
科目:高中化學 來源:2013屆江蘇省鹽城市明達中學高三上學期學情調研考試化學試卷(帶解析) 題型:單選題
研究發現,可以用石墨作陽極、鈦網作陰極、熔融CaF2—CaO作電解質,利用下圖所示裝置獲得金屬鈣,并以鈣為還原劑,還原二氧化鈦制備金屬鈦。下列敘述正確的是
| A.該電池工作過程中O2-向陰極移動 |
| B.陽極的電極反應式為C+2O2--4e-===CO2↑ |
| C.若用鉛蓄電池作該裝置的供電電源,“-”接線柱應連接PbO2電極 |
| D.在制備金屬鈦前后,整套裝置中CaO的總量減少 |
查看答案和解析>>
科目:高中化學 來源:2014屆河北省高三調研考試理綜化學試卷(解析版) 題型:填空題
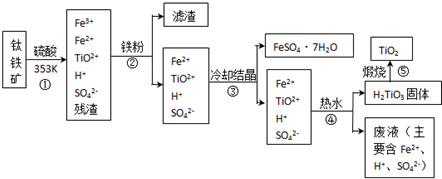
工業上生產金屬鈦的方法很多。以鈦鐵礦(主要成分FeTiO3,鈦酸亞鐵)為主要原料冶煉金屬鈦,生產的工藝流程圖如下,其中鈦鐵礦與濃硫酸發生反應的化學方程式為:
FeTiO3+2H2SO4=TiOSO4+FeSO4+2H2O

回答下列問題:
(1)鈦鐵礦和濃硫酸反應屬于______________________ (選填“氧化還原反應”或“非氧化還原反應”)。
(2)上述生產流程中加入物質A的目的是防止Fe2+被氧化,物質A是________,上述制備TiO2的過程中,所得到的副產物和可回收利用的物質分別是__________、___________。
(3)反應TiCl4+2Mg=2MgCl2+Ti在Ar氣氛中進行的理由是_______________。
(4)由二氧化鈦制取四氯化鈦所涉及的反應有:
TiO2 (s)+ 2Cl2 (g) +2C(s) =TiCl4(g) + 2CO(g) ΔH1 = -72 kJ•mol-1
TiO2(s) + 2Cl2 (g) =TiCl4(g) + O2 (g) ΔH2 =+38.8kJ•mol-1
C(s)+CO2(g)=2CO(g) ΔH3 =+282.8kJ•mol-1
①反應C(s)+CO2(g)=2CO(g)在高溫下能夠自發進行的原因是______________________。
②反應C(s)+O2(g)=CO2 (g)的ΔH=_______________。
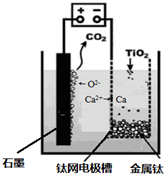
(5)研究發現,可以用石墨作陽極、鈦網作陰極、熔融CaF2-CaO作電解質,利用下圖所示裝置獲得金屬鈣,并以鈣為還原劑,還原二氧化鈦制備金屬鈦。①寫出陽極所發生反應的電極反應式:________________________________。

②在制備金屬鈦前后,CaO的總量不變,其原因是(請結合化學用語解釋) 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com