
分析 A位于周期表的s區,其原子中電子層數和未成對電子數相同,則A為H元素;B原子價電子排布式為nsnnpn,s能級容納2個電子,則n=2,原子價電子排布式為2s22p2,則B為C元素;D原子的最外層電子數是其內層的3倍,原子只能有2個電子層,最外層電子數為6,則D為O元素;C的原子序數介于碳、氧之間,則C為N元素;F元素位于元素周期表的第四行、第十一列,則F為Cu;B和E同主族,E的原子序數小于Cu,則E為Si,據此解答.
解答 解:A位于周期表的s區,其原子中電子層數和未成對電子數相同,則A為H元素;B原子價電子排布式為nsnnpn,s能級容納2個電子,則n=2,原子價電子排布式為2s22p2,則B為C元素;D原子的最外層電子數是其內層的3倍,原子只能有2個電子層,最外層電子數為6,則D為O元素;C的原子序數介于碳、氧之間,則C為N元素;F元素位于元素周期表的第四行、第十一列,則F為Cu;B和E同主族,E的原子序數小于Cu,則E為Si.
(1)元素位于元素周期表的第四行、第十一列,基態F原子的核外電子排布式為:1s22s22p63s23p63d104s1,故答案為:1s22s22p63s23p63d104s1;
(2)①C2H2中H原子不滿足8電子穩定結構,故錯誤;
②C2H2分子結構式為H-C≡C-H,分子中σ鍵和π鍵數目比為3:2,故錯誤;
③C2H2分子結構式為H-C≡C-H,為直線型對稱結構,由極性鍵和非極性鍵構形成的非極性分子,故正確;
④C2H2中心原子形成2個σ鍵、沒有孤對電子,碳原子雜化類型為sp雜化,故正確,
故選:③④;
(3)同周期隨原子序數增大元素第一電離能呈增大趨勢,氮元素原子2p能級為半滿穩定狀態,能量較低,第一電離能高于同周期相鄰元素的,故第一電離能:N>O>C,
故答案為:N>O>C;
(4)C的氣態氫化物與C的最高價氧化物對應的水化物反應生成一種鹽H為NH4NO3,晶體中存在的化學鍵類型有:離子鍵、共價、配位鍵,
故選:①②④;
(5)E為Si元素,基態原子核外電子排布式為:1s22s22p63s23p2,最高能層含有4個原子軌道數,B和E分別與氧元素形成二氧化碳、二氧化硅,前者屬于分子晶體,后者屬于原子晶體,故二氧化硅的熔沸點較高,
故答案為:4;SiO2;
(6)Cu單質的晶體堆積方式為面心立方,以頂點Cu原子研究,與之相鄰的原子處于面心,每個頂點為8個晶胞共用,每個面心為2個晶胞共用,則其配位數為$\frac{3×8}{2}$=12,晶胞中Cu原子數目為8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,相對分子質量為M,則晶胞質量為4×$\frac{M}{{N}_{A}}$g,它的晶胞棱長為a(cm),則F晶體的密度為$\frac{4×\frac{M}{{N}_{A}}g}{(acm)^{3}}$=$\frac{4M}{{N}_{A×{a}^{3}}}$g•cm-3,
故答案為:12;$\frac{4M}{{N}_{A×{a}^{3}}}$.
點評 本題是對物質結構的考查,涉及核外電子排布、電離能、化學鍵、雜化方式、晶體類型與性質、晶胞計算等,注意理解均攤法進行晶胞有關計算,熟記中學常見晶胞結構,理解同周期第一電離能異常情況,難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | Al2O3可用作高溫耐火材料 | |
| B. | 利用漂白粉的氧化性漂白織物 | |
| C. | 濃硫酸可刻蝕石英制藝術品 | |
| D. | 在醫療上碳酸氫鈉可用于治療胃酸過多 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 原子半徑:Z>Y | |
| B. | 簡單離子的半徑:M的離子>Z的離子>Y的離子>X的離子 | |
| C. | X的陰離子和Y的陰離子核外電子數相同 | |
| D. | Z元素的最高價氧化物的水化物的化學式為HZO4 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
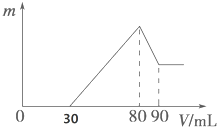 把一定質量的鎂、鋁混合物投入到1mol•L-1的鹽酸中,待金屬完全溶解后,向溶液中加入1mol,•L-1的氫氧化鈉溶液,生成沉淀的質量與加入氫氧化鈉溶液的體積關系如圖所示.則:
把一定質量的鎂、鋁混合物投入到1mol•L-1的鹽酸中,待金屬完全溶解后,向溶液中加入1mol,•L-1的氫氧化鈉溶液,生成沉淀的質量與加入氫氧化鈉溶液的體積關系如圖所示.則:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 碳元素的平均相對原子質量 | B. | 碳原子質量 | ||
| C. | 同位素C-12的行相原子質量 | D. | C-12的質量數 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | H+、Na+、CO32- | B. | Ba2+、SO42-、Cl- | C. | K+、H+、OH- | D. | Ag+、Al3+、NO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫常壓下,1.5 mol NO2的體積約為33.6 L | |
| B. | NaOH的摩爾質量是40 g | |
| C. | 100 mL水中溶解了8.4 g NaHCO3,則溶液中Na+的物質的量濃度為1 mol/L | |
| D. | 同溫同壓下,相同體積的C12和SO2氣體所含的分子數一定相同 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com