
【題目】A、B、C、D、E是元素周期表前四周期中的常見元素,原子序數依次增大,相關信息如下:
元素 | 相關信息 |
A | 基態原子的價電子排布式為nSnnPn |
B | 元素原子的核外p電子數比s電子數少1個 |
C | 最外層電子數是電子層數的3倍 |
D | 簡單離子是第三周期元素中離子半徑最小的 |
E | 價電子層中的未成對電子數為4 |
請回答下列問題:
(1)寫出下列元素符號:A______, B_______,C________,D__________。
(2)寫出C元素在周期表的位置_________,E2+價電子的軌道表示式______________,B元素能量最高的電子為____軌道上的電子,其軌道呈______形。
(3)按原子軌道的重疊方式,1molA與C形成的最高價化合物中σ鍵有______個,π鍵有______個。(阿伏加德羅常數的值用NA表示)
(4)B、C、D的簡單離子的半徑由大到小的順序為________(用離子符號表示)。
(5)寫出C的核外有18個電子的氫化物的電子式_____________。
【答案】C N O Al )第2周期第VIA族  2p 紡錘形(或啞鈴形) 2NA 2NA N3->O2->Al3+
2p 紡錘形(或啞鈴形) 2NA 2NA N3->O2->Al3+ ![]()
【解析】
A、B、C、D、E是元素周期表前四周期中的常見元素,原子序數依次增大,由A的基態原子的價電子排布式可以知道,n=2,則A為C元素;C的最外層電子數是電子層數的3倍,則C為O元素;B的基態原子中的未成對電子數是同周期中最多的,可以知道p能級上只有3個電子,結合原子序數可以知道,B為N元素;D為簡單離子是第三周期元素中離子半徑最小的,則D為Al元素;E的價電子層中的未成對電子數為4,則E為Fe,據以上分析解答。
A、B、C、D、E是元素周期表前四周期中的常見元素,原子序數依次增大,由A的基態原子的價電子排布式可以知道,n=2,則A為C元素;C的最外層電子數是電子層數的3倍,則C為O元素;B的基態原子中的未成對電子數是同周期中最多的,可以知道p能級上只有3個電子,結合原子序數可以知道,B為N元素;D為簡單離子是第三周期元素中離子半徑最小的,則D為Al元素;E的價電子層中的未成對電子數為4,則E為Fe;
(1) 由上述分析可以知道,A為C,B為N,C為O,D為Al;綜上所述,本題答案是:C,N , O ,Al。
(2)C為O,核電荷數8,在周期表的位于第2周期第VIA族;鐵原子基態核外電子排布為:1s22s22p63s23p63d64s2,Fe2+價電子的軌道表示式 ;B為N, 基態核外電子排布為:1s22s22p3,能量最高的電子為2p軌道上的電子,其軌道呈紡錘形(或啞鈴形);綜上所述,本題答案是:第2周期第VIA族 ,
;B為N, 基態核外電子排布為:1s22s22p3,能量最高的電子為2p軌道上的電子,其軌道呈紡錘形(或啞鈴形);綜上所述,本題答案是:第2周期第VIA族 , ,2p; 紡錘形(或啞鈴形)。
,2p; 紡錘形(或啞鈴形)。
(3)按原子軌道的重疊方式,1molC與O形成的最高價化合物為CO2,結構式為O=C=O,含有σ鍵有2NA 個,π鍵有2NA 個;綜上所述,本題答案是:2NA ,2NA。
(4)具有相同電子結構的離子中原子序數大的離子半徑小,則B、C、D的簡單離子的半徑由大到小的順序為N3->O2->Al3+;因此,本題正確答案是:N3->O2->Al3+。
(5)C的核外有18個電子的氫化物為過氧化氫,其電子式為![]() ,因此,本題正確答案是:
,因此,本題正確答案是:![]() 。
。


科目:高中化學 來源: 題型:
【題目】氮氧化物(主要為NO和NO2)是大氣污染物,如何有效地消除氮氧化物污染是目前科學家們研究的熱點問題之一。
(1)用尿素[CO(NH2)2]吸收氮氧化物是一種可行的方法。
①尿素在高溫條件下與NO2反應轉化成無毒氣體,該反應的化學方程式為___________;用尿素溶液也可吸收氮氧化物,研究表明,氮氧化物氣體中NO的體積分數越大,總氮被還原率越低,可能的原因是______。
②在一個體積固定的真空密閉容器中充入等物質的量的CO2和NH3,在恒定溫度下使其發生反應2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(g)并達到平衡,混合氣體中氨氣的體積分數隨時間的變化如圖所示:
CO(NH2)2(s)+H2O(g)并達到平衡,混合氣體中氨氣的體積分數隨時間的變化如圖所示:

則A點的v正(CO2)___________(填“>”“<”或“=”)B點的v逆(H2O),原因是________________。
(2)已知O3氧化氮氧化物的主要反應的熱化學方程式如下:2NO(g)+O2(g)=2NO2(g)△H1=akJ·mol-1,NO(g)+O3(g)=NO2(g)+O2(g)△H2=bkJ·mol-1,6NO2(g)+O3(g)===3N2 O5(g)△H3=c kJ·mol-1,則反應4NO2(g)+O2(g)=2N2O5(g)的△H=___________kJ·mol-1。
(3)氮氧化物也可用堿溶液吸收。若NO和NO2混合氣體被NaOH溶液完全吸收,只生成一種鹽,則該鹽的化學式為_______;已知常溫下,Ka(HNO2)=5×10-4,則反應HNO2(aq)+NaOH(aq)![]() NaNO2(ag)+H2O(1)的平衡常數K=___________,相同物質的量濃度的HNO2、NaNO2混合溶液中,各離子的物質的量濃度由大到小的順序為___________。
NaNO2(ag)+H2O(1)的平衡常數K=___________,相同物質的量濃度的HNO2、NaNO2混合溶液中,各離子的物質的量濃度由大到小的順序為___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】大氣壓對許多物理實驗和化學實驗有著重要影響。如圖是噴泉實驗的裝置圖:

(1)收集氨氣應使用___法,要得到干燥的氨氣時,用___做干燥劑。
(2)請用相應的方程式解釋氨氣溶于水后顯堿性的原因___。
(3)用如圖裝置進行噴泉實驗,上部燒瓶已裝滿干燥的氨氣,引發水上噴的操作是:___,該實驗的原理是___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硒化鋅是一種透明黃色半導體,也可作紅外光學材料,熔點1520℃。
(1)鋅離子的電子排布式是_____________。
(2)根據元素周期律,電負性S______Se,第一電離能Se______As(填“>”或“<”)。
(3)H2O的沸點______________(填“>”或“<”)H2Se的沸點,其原因是:______。
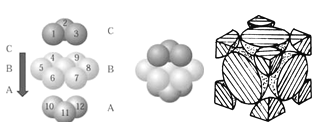
(4)NaCl晶胞如圖所示,陰、陽離子都具有球型對稱結構,它們都可以看做剛性圓球,并彼此“相切”。晶胞中Na+的配位數為____,若晶胞參數為a pm,阿伏加德羅常數的值用NA表示,若晶體密度為_______g·cm﹣3。(列出表達式)。

(5)銅晶體中銅原子的堆積方式如圖所示,銅晶體中原子的堆積模型屬于_______。若已知銅的原子半徑為rcm,表示原子空間占有率的表達式為__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定溫度下在體積為5 L的密閉容器中發生可逆反應。(Ⅰ)若某可逆反應的化學平衡常數表達式為:K=![]()
(1)寫出該反應的化學方程式:
(2)能判斷該反應一定達到化學平衡狀態的依據是 (填選項編號)。
A.容器中氣體的平均相對分子質量不隨時間而變化
B.v正(H2O)=v逆(H2)
C.容器中氣體的密度不隨時間而變化
D.容器中總質量不隨時間而變化
E.消耗n mol H2的同時消耗n mol CO
(Ⅱ)若該密閉容器中加入的是2 mol Fe(s)與1 mol H2O(g),t1秒時,H2的物質的量為0.20 mol,到第t2秒時恰好達到平衡,此時H2的物質的量為0.35 mol。
(1)t1~t2這段時間內的化學反應速率v(H2)= 。
(2)若繼續加入2 mol Fe(s),則平衡 移動(填“向正反應方向”、“向逆反應方向”或“不”),繼續通入1 mol H2O(g),再次達到平衡后,H2物質的量為 mol。
(3)該反應的逆反應速率隨時間變化的關系如圖。t1時改變了某種條件,改變的條件可能是 、 (填寫2項)。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】利用如圖所示裝置測定中和熱的實驗步驟如下:

①用量筒量取50mL0.50mol·L-1鹽酸倒入小燒杯中,測出鹽酸溫度;②用另一量筒量取50mL0.55mol·L-1NaOH溶液,并用另一溫度計測出其溫度;③將NaOH溶液倒入小燒杯中,設法使之混合均勻,測得混合液最高溫度,回答下列問題:
(1)為什么所用NaOH溶液要稍過量____________________。
(2)倒入NaOH溶液的正確操作是________(填序號)。
A.沿玻璃棒緩慢倒入 B.分三次少量倒入 C.一次迅速倒入
(3)使鹽酸與NaOH溶液混合均勻的正確操作是________(填序號)。
A.用溫度計小心攪拌
B.揭開硬紙片用玻璃棒攪拌
C.輕輕地振蕩燒杯
D.用套在溫度計上的環形玻璃攪拌棒輕輕地攪動
(4)現將一定量的稀氫氧化鈉溶液、稀氫氧化鈣溶液、稀氨水分別和1L1mol·L-1的稀鹽酸恰好完全反應,其反應熱分別為△H1、△H2、△H3,則△H1、△H2、△H3的大小關系為________。
(5)________(填“能”或“不能”)用Ba(OH)2溶液和硫酸代替氫氧化鈉溶液和鹽酸,理由是_____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示,從A處通入Cl2。當關閉B閥時,C處的紅布逐漸褪色;當打開B閥后,C處的紅布無明顯現象,則下列判斷正確的是

A.通入的Cl2可能是潮濕的B.紅布一定是干燥的
C.D中的液體可能是NaOHD.使紅布褪色的物質是Cl2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】關于濃度均為0.1 mol/L的三種溶液:①氨水、②鹽酸、③氯化銨溶液,下列說法不正確的是
A. c(NH4+):③>①
B. 水電離出的c(H+):②>①
C. ①和②等體積混合后的溶液:c(H+)=c(OH-)+c(NH3·H2O)
D. ①和③等體積混合后的溶液:c(NH4+)>c(Cl-)>c(OH-)>c(H+)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com