
近年來,酸雨污染較為嚴重,防治酸雨成了迫在眉睫的問題。
(1)有人提出了一種利用氯堿工業產品處理含二氧化硫廢氣的方法,流程如下:
(Ⅰ)將含SO2的廢氣通入電解飽和食鹽水后所得到的溶液中,得NaHSO3溶液。
(Ⅱ)將電解飽和食鹽水所得氣體反應后制得鹽酸。
(Ⅲ)將鹽酸加入NaHSO3溶液中,反應所得到的SO2氣體回收,生成的NaCl循環利用。
①寫出步驟(Ⅰ)反應的化學方程式: 。
②寫出步驟(Ⅱ)中電解飽和食鹽水的化學方程式: 。
③寫出步驟(Ⅲ)反應的離子方程式: 。
(2)還有學者提出利用Fe2+、Fe3+等離子的催化作用,常溫下將SO2氧化成SO42-而實現SO2的回收利用。某研究性學習小組據此設計了如下方案,在實驗室條件下測定轉化器中SO2氧化成SO42-的轉化率。
①該小組采用下圖裝置在實驗室測定模擬煙氣中SO2的體積分數,X溶液可以是 。(填寫序號)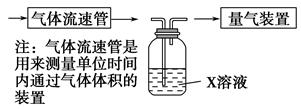
| A.碘的淀粉溶液 | B.酸性高錳酸鉀溶液 |
| C.氫氧化鈉溶液 | D.氯化鋇溶液 |
 的轉化率,已知氣體流速,還需測定的數據有 、 。
的轉化率,已知氣體流速,還需測定的數據有 、 。  閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:單選題
氯氣是一種重要的工業原料。工業上利用反應在3Cl2+8NH3=N2+6NH4Cl檢查氯氣管道是否漏氣。下列說法正確的是
| A.若管道漏氣遇氨就會產生白霧 | B.該反應利用了氨氣的還原性 |
| C.該反應屬于復分解反應 | D.生成6molNH4Cl有18mol電子轉移 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(10分)(I) 海帶中含有碘元素,某校研究性學習小組設計了如下實驗步驟來提取碘:
①在濾液中,滴加幾滴硫酸和適量的雙氧水 ②將海帶燒成灰,向灰中加水,加熱攪拌
③加CC14振蕩、靜置 ④過濾 ⑤分液。
(1)合理的操作順序為 。
(2)步驟③中要用到的玻璃儀器為 ,該步分離I2的操作叫 。
(II)向某含有Fe2+、I—、Br—的溶液中緩緩通入適量氯氣,溶液中各種離子的物質的量變化如圖所示。
(3)AB段表示 離子的減少。
(4)n(Cl2)=2mol時,溶液中反應的離子方程式為 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(14分) 氯堿廠電解飽和食鹽水制取NaOH的工藝流程示意圖如下: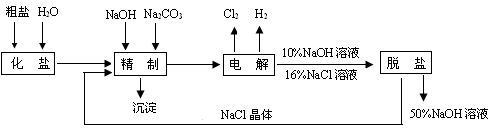
依據上圖,完成下列填空:
在電解過程中,與電源正極相連的電極上所發生反應的方程式為: 。
與電源負極相連的電極附近溶液pH 。(填“不變”“增大”或“減小”)
(2)如果粗鹽中SO42-含量較高,必須添加鋇試劑除去SO42-,該試劑可以選 。
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(3)為有效除去Ca2+、Mg2+、SO42-,加入試劑的合理順序為 (選a、b、c,多選扣分)。
a.先加NaOH,后加Na2CO3,再加鋇試劑
b.先加NaOH,后加鋇試劑,再加Na2CO3
c.先加鋇試劑,后加NaOH,再加Na2CO3
(4)在用陽離子交換膜法電解食鹽水時,電解槽分隔為陽極區和陰極區,防止Cl2與NaOH反應;采用無隔膜電解冷的食鹽水時,Cl2與NaOH充分反應,產物最終僅有NaClO和H2,相應的化學反應方程式為 、 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
硅是重要的半導體材料,構成了現代電子工業的基礎。回答下列問題:
(1)基態Si原子中,電子占據的最高能層符號 ,該能層具有的原子軌道數為 、電子數為 。
(2)硅主要以硅酸鹽、 等化合物的形式存在于地殼中。
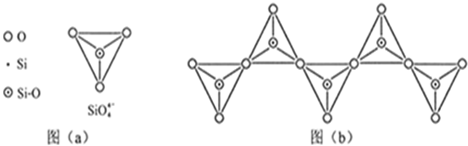
(3)單質硅存在與金剛石結構類似的晶體,其中原子與原子之間以 相結合,其晶胞中共有8個原子,其中在面心位置貢獻 個原子。
(4)單質硅可通過甲硅烷(SiH4)分解反應來制備。工業上采用Mg2Si和NH4CI在液氨介質中反應制得SiH4,該反應的化學方程式為 。
(5)碳和硅的有關化學鍵鍵能如下所示,簡要分析和解釋下列有關事實:
| 化學鍵 | C-C | C-H | C-O | Si-Si | Si-H | Si-O |
| 鍵能(KJ/mol) | 356 | 413 | 336 | 226 | 318 | 452 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
某校化學研究性學習小組,在學習金屬的冶煉以后對一氧化碳還原金屬氧化物的實驗非常感興趣,他們查閱有關資料后發現,一氧化碳的制備可利用甲酸和濃硫酸共熱到60~80 ℃發生脫水反應制取:
HCOOH CO↑+H2O
CO↑+H2O
請根據以下各圖幫他們組裝成一套相對合理的實驗裝置圖(某些裝置可重復使用)。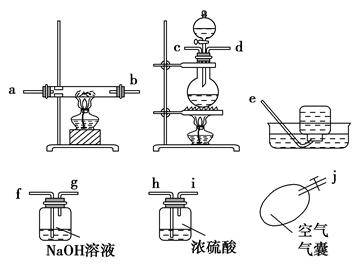
回答以下問題:
(1)合理實驗裝置的連接順序是(寫小寫字母) 。
(2)在反應時一定要先通一會一氧化碳氣體,然后再點燃加熱氧化鐵的酒精燈,原因是 。
| A.因為一般反應從左到右進行 |
| B.排除體系內的空氣,使反應過程更安全 |
| C.甲酸與濃硫酸反應可以產生大量的CO |
| D.此反應加熱時間長有利于產生CO |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(1)瑞典化學家舍勒將軟錳礦(主要成分MnO2)與濃鹽酸混合加熱,在世界上首先制得了氯氣,寫出該反應的離子方程式 ;
(2)洪災過后,飲用水的消毒殺菌成為抑制大規模傳染性疾病爆發的有效方法之一。 漂白粉是常用的消毒劑。工業上將氯氣通入石灰乳[Ca(OH)2]制取漂白粉,化學反應方程式為 ;
(3)在下圖的四條直線分別表示鈉、銅、鋁、鐵與足量Cl2反應時,消耗金屬的質量(縱軸)與反應掉的氯氣質量(橫軸)的關系,其中代表鐵與Cl2反應的直線是 ,如果橫軸表示消耗掉的硫的質量,則b表示的是四種金屬中的 。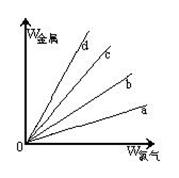
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
金剛石、SiC具有優良的耐磨、耐腐蝕特性,應用廣泛。
(1)碳與短周期元素Q的單質化合僅能生成兩種常見氣態化合物,其中一種化合物R為非極性分子。碳元素在周期表中的位置是____________,Q是____________,R的電子式為________。
(2)一定條件下,Na還原CCl4可制備金剛石。反應結束冷卻至室溫后,回收其中的CCl4的實驗操作名稱為________,除去粗產品中少量鈉的試劑為________。
(3)碳還原SiO2制SiC,其粗產品中雜質為Si和SiO2。現將20.0 g SiC粗產品加入到過量的NaOH溶液中充分反應,收集到0.1 mol氫氣,過濾得SiC固體11.4 g,濾液稀釋到1 L。生成氫氣的離子方程式為__________________________________,硅酸鹽的物質的量濃度為_________。
(4)下列敘述正確的有________(填序號)。
①Na還原CCl4的反應、Cl2與H2O的反應均是置換反應
②水晶、干冰熔化時克服粒子間作用力的類型相同
③Na2SiO3溶液與SO3的反應可用于推斷Si與S的非金屬性強弱
④鈉、鋰分別在空氣中燃燒,生成的氧化物中陰陽離子數目比均為1:2
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
某化學小組進行Na2SO3的性質實驗探究。
在白色點滴板的a、b、c三個凹槽中滴有Na2SO3溶液,再分別滴加下圖所示的試劑:
實驗現象如下表:
| 編號 | 實驗現象 |
| a | 溴水褪色 |
| b | 產生淡黃色沉淀 |
| c | 滴入酚酞溶液變紅,再加入BaCl2溶液后產生沉淀且紅色褪去 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com