
【題目】香蘭素是重要的香料之一,它可由丁香酚經多步反應合成。
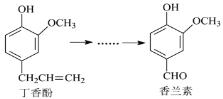
有關上述兩種化合物的說法正確的是( )
A.丁香酚不能與FeCl3溶液發生顯色反應
B.常溫下,1mol丁香酚只能與1molBr2反應
C.香蘭素分子中至少有12個原子共平面
D.1mol香蘭素最多能與3mol氫氣發生加成反應
 培優口算題卡系列答案
培優口算題卡系列答案 開心口算題卡系列答案
開心口算題卡系列答案 口算題卡河北少年兒童出版社系列答案
口算題卡河北少年兒童出版社系列答案科目:高中化學 來源: 題型:
【題目】亞硝酸鈉(NaNO2)被稱為工業鹽,在漂白、電鍍等方面應用廣泛。以木炭、濃硝酸、水和銅為原料制備亞硝酸鈉的裝置如圖所示:
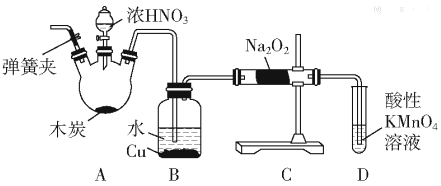
已知:室溫下,①2NO+Na2O2=2NaNO2;
②3NaNO2+3HCl=3NaCl+HNO3+2NO↑+H2O;
③酸性條件下,NO或NO2-都能與MnO4-反應生成NO3-和Mn2+。
請按要求回答下列問題:
(1)檢査完該裝置的氣密性,裝入藥品后,實驗開始前通入一段時間氣體Ar,然后關閉彈簧夾,再滴加濃硝酸,加熱控制B中導管均勻地產生氣泡。上述操作的作用是___。
(2)B中觀察到的主要現象是___;
(3)A裝置中反應的化學方程式為___;
(4)D裝置中反應的離子方程式___;
(5)預測C中反應開始階段,固體產物除NaNO2外,還含有的副產物有Na2CO3和___。為避免產生這些副產物,應在B、C裝置間增加裝置E,則E中盛放的試劑名稱為___。
(6)利用改進后的裝置,將3.12gNa2O2完全轉化成為NaNO2,理論上至少需要木炭___g。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某興趣小組探究SO2氣體還原Fe3+、I2,他們使用的藥品和裝置如圖所示:
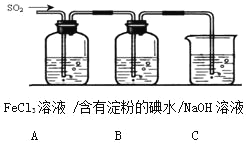
(1)下列實驗方案適用于在實驗室制取所需SO2的是________(填序號).
A Na2SO3溶液與HNO3 B Na2SO3固體與濃硫酸
C 固體硫在純氧中燃燒D 銅與熱濃H2SO4
(2)裝置C的作用是_______
(3)若要從A中所得溶液提取晶體,必須進行的實驗操作步驟:蒸發、冷卻結晶、過濾、____自然干燥,在這一系列操作中沒有用到的儀器有____(填序號).
A 蒸發皿B 石棉網C 漏斗D 燒杯E 玻璃棒F 坩堝
(4)在上述裝置中通入SO2,為了驗證A中SO2與Fe3+發生了氧化還原反應,他們取A中的溶液,分成三份,并設計了如下實驗:
方案①:往第二份試液加入鐵氰化鉀溶液,產生藍色沉淀。
方案②:往第一份試液中加入KMnO4溶液,紫紅色褪去。
方案③:往第三份試液加入用稀鹽酸酸化的BaCl2,產生白色沉淀。
上述方案不合理的是________,原因是___________ 。
(5)能表明I的還原性弱于SO2的化學方程式為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表是幾種弱酸常溫下的電離平衡常數:
CH3COOH | H2CO3 | H2S | H3PO4 |
1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=9.1×10-8 K2=1.1×10-12 | K1=7.5×10-3 K2=6.2×10-8 K3=2.2×10-13 |
則下列說法中不正確的是( )
A. 碳酸的酸性強于氫硫酸
B. 多元弱酸的酸性主要由第一步電離決定
C. 常溫下,加水稀釋醋酸,![]() 增大
增大
D. 向弱酸溶液中加少量NaOH溶液,電離常數不變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據下列圖示所得出的結論不正確的是

A. 圖甲是CO(g)+H2O(g)![]() CO2(g)+H2(g)的平衡常數與反應溫度的關系曲線,說明該反應的ΔH<0
CO2(g)+H2(g)的平衡常數與反應溫度的關系曲線,說明該反應的ΔH<0
B. 圖乙是室溫下H2O2催化分解放出氧氣的反應中c(H2O2 )隨反應時間變化的曲線,說明隨著反應的進行H2O2分解速率逐漸減小
C. 圖丙是室溫下用0.1000 mol·L1NaOH溶液滴定20.00 mL 0.1000 mol·L1某一元酸HX的滴定曲線,說明HX是一元強酸
D. 圖丁是室溫下用Na2SO4除去溶液中Ba2+達到沉淀溶解平衡時,溶液中c(Ba2+ )與c(SO42)的關系曲線,說明溶液中c(SO42 )越大c(Ba2+ )越小
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度下,向10 mL 0.1 mol/LCuCl2溶液中滴加0.1 mol/L的Na2S溶液,滴加過程中溶液中lgc(Cu2+)與Na2S溶液體積(V)的關系如圖所示,已知:lg2=0.3,Ksp(ZnS)=3×10-25 。下列有關說法正確的是( )

A.a、b、c三點中,水的電離程度最大的為b點
B.Na2S溶液中:c(S2-)+c(HS-)+c(H2S)=2c(Na+)
C.該溫度下Ksp(CuS)=4×10-36
D.向100 mL Zn2+、Cu2+濃度均為10-5 mol/L的混合溶液中逐滴加入10-4 mol/L的Na2S溶液,Zn2+先沉淀
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】羰基硫(COS)是全球硫循環的重要中間體,也是有機合成中的重要原料,是化學工作者重要的研究對象。已知:
Ⅰ.COS(g)+H2(g)![]() H2S(g)+CO(g) △Hl=-17kJ/mol;
H2S(g)+CO(g) △Hl=-17kJ/mol;
Ⅱ.COS(g)+H2O(g)![]() H2S(g)+CO2(g) △H2=-35kJ/mol。
H2S(g)+CO2(g) △H2=-35kJ/mol。
回答下列問題:
(1)反應CO(g)+H2O(g)![]() H2(g)+CO2(g)的△H=________。
H2(g)+CO2(g)的△H=________。
(2)在充有催化劑的恒壓密閉容器中進行反應I。設起始充入的n(H2):n(COS)=m,相同時間內測得COS轉化率與m和溫度(T)的關系如圖所示。
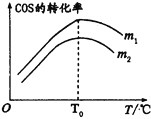 ①m1________m2(填>、<或=)。
①m1________m2(填>、<或=)。
②溫度高于T0時,COS轉化率減小的可能原因為_________。
A.有副反應發生。
B.反應的△H增大。
C.催化劑活性降低。
D.逆反應速率增大的倍數小于正反應速率增大的倍數
(3)在恒溫、恒容密閉容器中.進行反應I。下列說法中能說明反應I已達到平衡狀態的是___________。
A.c(H2S)=c(CO) B.v正(H2)=v逆(H2S)
C.容器中氣體密度保持不變 D.容器中混合氣體平均摩爾質量保持不變
E.c(COS)保持不變
(4)某溫度下,向體積為2 L的恒容密閉容器中通入5 mol COS(g)和5 molH2O(g),發生反應Ⅱ,5 min后反應達到平衡,測得COS(g)的轉化率為80%。
①反應從起始至5 min內,用H2S濃度變化表示的平均反應速度v(H2S)=________。
②該溫度下,上述反應的平衡常數K=________。
③其他條件相同時,既能使上述反應中COS的平衡轉化率降低,又能使反應速率加快的做法是________。
A.縮小容器容積 B.升高溫度
C.分離出硫化氫 D.加入一定量H2O(g)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】向含a mol NaClO的溶液通入b mol SO2充分反應(不考慮二氧化硫與水之間的反應以及次氯酸的分解)。下列說法不正確的是
A.當0<b<a/3時:SO2+H2O+3ClO-=![]() +2HClO+Cl-
+2HClO+Cl-
B.當b=a時,SO2+H2O+ClO-==2H++Cl-+![]()
C.當a/3≤b≤a時,反應后溶液中H+的物質的量: 0<n(H+)≤2b mol
D.當0<b<a時,反應后溶液中ClO-、Cl-和![]() 物質的量之比為:(a-b)∶b∶b
物質的量之比為:(a-b)∶b∶b
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是
A.烷烴的通式為CnH2n+2,隨n值增大,碳元素的質量百分含量逐漸減小
B.乙烯與溴水發生加成反應的產物為溴乙烷
C.1mol苯恰好與3mol氫氣完全加成,說明一個苯分子中有三個碳碳雙鍵
D.C7H16,主鏈上有5個碳原子的同分異構體共有5種
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com