
【題目】下列敘述不正確的是( )
A.過氧化鈉可作為潛水艇的供氧劑
B.氫氣在氯氣中安靜的燃燒,發出蒼白色的火焰
C.Cl2能使濕潤的有色布條褪色,則Cl2具有漂白性
D.用BaCl2溶液可鑒別Na2CO3和NaHCO3兩溶液
科目:高中化學 來源: 題型:
【題目】下列說法不正確的是( )
A.淀粉可以制得葡萄糖和酒精
B.鋁合金的熔點和硬度均高于純鋁
C.玻璃、塑料、金屬、紙類均是可回收的物品
D.硬化油不易被空氣氧化而便于儲存和運輸
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖為元素周期表的一部分,請參照①~⑨在表中的位置,回答下列問題:

(1)②的元素符號是__________,⑥在周期表中的位置是___________。
(2)⑦、⑧兩元素比較,非金屬性強的是(填元素符號)_______,從原子結構角度解釋原因_________。
(3)④-⑥這三種元素中,寫出最高價氧化物對應水化物兩兩之間能反應的離子方程式____________________。
(4)寫出工業冶煉元素⑤單質的化學方程式_________,不選擇熱還原法冶煉這種活潑金屬的原因是___________________。
(5)元素①和③可以組成很多種物質,寫出其中原子個數比為1:4的物質的電子式______,請從化學鍵角度解釋該物質中原子個數比為1:4的原因________________。
(6)已知Se在周期表中的位置如圖所示,請畫出Se的原子結構示意圖________。
請任意寫出三種Se物質的化學式,預測其性質(一條即可),并說明預測依據,完成在下列表格中。________
含Se物質化學式 | 性質 | 預測依據 |
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖為氫氧燃料電池裝置示意圖。

(1)該裝置是利用反應 2H2+O2===2H2O 設計而成的,該反應能設計成電池的原因是___________________。
(2)該電池的正極反應物是_______________,判斷依據是__________________。
(3)下列關于裝置描述不正確的是:__________。
a.導線是電子導體
b.該裝置需要點燃才能產生電流
c.Pt電極主要作用是提供得失電子的場所
d.電子從通氧氣一級沿導線轉移到通氫氣一級
(4)該裝置是如何形成電流的?請進行完整說明:____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知海水中溴元素主要以Br-形式存在,工業上從海水中提取溴的流程如下:

資料:溴單質容易揮發。
(1)寫出“氧化”時的離子方程式_______。
(2)寫出第1步“吸收”時的離子方程式________________,該反應體現了SO2的____性。
(3)得到的“含Br2溶液”通過以下不同操作,都可得到溴單質:
① 直接蒸餾得到溴單質,該操作利用的是溴的何種性質:___________;
② 加入四氯化碳萃取,將得到的溴的四氯化碳溶液蒸餾得到溴單質。可以用四氯化碳對溴溶液進行萃取利用的是溴的何種性質:_______________。
(4)對虛線框中的流程進行整體分析,完整說明該流程中所有操作的目的是___________。
(5)工業可用Na2CO3溶液代替二氧化硫的水溶液吸收Br2,完成下列化學反應方程式:
___Br2+___Na2CO3=___NaBrO3+____CO2+__ ______
若有480g溴完全反應,轉移電子的物質的量為__________ mol。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關物質性質的說法錯誤的是( )
A.熱穩定性:HCl>H2S
B.原子半徑:N>O
C.結合質子能力:S2﹣>Cl﹣
D.酸性:H2SO3>H2SO4
查看答案和解析>>
科目:高中化學 來源: 題型:
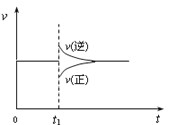
【題目】在一定條件下,向一帶活塞的密閉容器中充入2mol NO2,發生下列反應2NO2(g) ![]() N2O4(g) ΔH < 0,達到平衡狀態后,在t1時刻改變條件,化學反應速率隨時間變化關系如圖。下列對t1時刻改變條件的推測中正確的是
N2O4(g) ΔH < 0,達到平衡狀態后,在t1時刻改變條件,化學反應速率隨時間變化關系如圖。下列對t1時刻改變條件的推測中正確的是
A.保持壓強不變,升高反應溫度
B.保持溫度和容器體積不變,充入1mol N2(g)
C.保持溫度和容器體積不變,充入1mol N2O4 (g)
D.保持溫度和壓強不變,充入1mol N2O4 (g
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】按要求完成下列填空:
(1)常溫時,AlCl3的水溶液呈________(填“酸”、“中”、“堿”)性,原因是(用離子方程式表示):________________________。AlCl3溶液蒸干并灼燒得到的物質是__________(填化學式)。
(2)泡沫滅火器滅火時發生反應的離子方程是____________;
(3)為了使Na2S溶液中![]() 的比值變小,可加入的物質是_______
的比值變小,可加入的物質是_______
A.適量鹽酸 B.適量NaOH溶液
C.適量KOH溶液 D.適量蒸餾水
(4)已知25℃ 時,Ksp[Cu(OH)2]=2×10-20,某CuSO4溶液里c(Cu2+)=0.02molL-1,如要生成Cu(OH)2 沉淀,應調整溶液的pH,使之大于______________。
(5)已知c(Ca2+)≤10-5 mol·L-1時可視為沉淀完全;Ksp(CaCO3)=4.96×10-9。在Ca(NO3)2溶液中加入(NH4)2CO3溶液后過濾,若測得濾液中c(CO![]() )=10-3 mol·L-1,則Ca2+是否沉淀完全?________(填“是”或“否”)。
)=10-3 mol·L-1,則Ca2+是否沉淀完全?________(填“是”或“否”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列反應屬于取代反應的是( )
A. 乙醇與濃H2SO4共熱170℃
B. 乙烯使溴水褪色
C. 甲苯與濃硫酸、濃硝酸混合
D. 苯與Cl2一定條件生成六氯環己烷
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com