
【題目】下列關系正確的是( )
A. 熔點:正戊烷>2,2-二甲基戊烷>2,3-二甲基丁烷>丙烷
B. 沸點:CH3CH2CH2OH >CH3CH2CH2Br> CH3CHClCH3> CH3CH2CH2Cl> CH3CH2CH3
C. 密度:CCl4>CHCl3>CH2Cl2>H2O>苯
D. 等物質的量的烴燃燒消O2量:環己烷>己烷>苯
 鴻圖圖書寒假作業假期作業吉林大學出版社系列答案
鴻圖圖書寒假作業假期作業吉林大學出版社系列答案科目:高中化學 來源: 題型:
【題目】如下反應條件的控制中,不恰當的是( )
A.為加快H2O2的分解速率增大H2O2的濃度
B.為加快H2O2的分解速率而把反應容器放到冷水中冷卻
C.為加快KClO3的分解速率而加入MnO2
D.為防止火災,在面粉廠、加油站等場所要嚴禁煙火
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖六個操作是常見物質的分離提純操作,則有關這的說法不正確的是


A. 操作1、操作2、操作6都可以是蒸餾,也可以是蒸發
B. 操作2可以是蒸發濃縮、冷卻結晶、過濾
C. 操作3可以是洗劑、干燥
D. 操作4、操作5分別是萃取、分液
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某課外活動小組進行Fe(OH)3膠體的制備實驗并檢驗其相關性質。
(1)若將飽和FeCl3溶液分別滴入下列物質中,能形成膠體的是______________(填序號)。
A.冷水 B.沸水 C.NaOH濃溶液 D.NaCl濃溶液
(2)寫出制備Fe(OH)3膠體的化學反應方程式:________________。
(3)怎樣證明制得的物質是膠體?請簡述操作過程:__________________。
(4)取少量制得的膠體加入試管中,再加入少量(NH4)2SO4溶液,觀察到的現象是__________, 這種現象稱為膠體的________________。
(5)Fe(OH)3膠體能穩定存在的主要原因是________(填序號)。
A. 膠粒直徑小于1nm B. 膠粒帶正電荷
C. 膠粒作布朗運動 D . 膠粒能透過濾紙
(6)Fe(OH)3膠體區別于FeCl3溶液最本質的特征是________(填序號)。
A. Fe(OH)3膠體粒子的直徑在1~100nm之間
B. Fe(OH)3膠體具有丁達爾效應
C. Fe(OH)3膠體是均一的分散系
D. Fe(OH)3膠體的分散質粒子能透過濾紙
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用石油產品A(C3H6)為主要原料,合成具有廣泛用途的有機玻璃PMMA。流程如下(部分產物和條件省略)

試回答下列問題:
(1)B的名稱________; D 中官能團名稱_________。
(2)E→G 的化學方程式為____,反應類型是_________。
(3)T是G的同分異構體,1molT與足量新制Cu(OH)2懸濁液反應最多生成2molCu2O沉淀,T的結構有________種(不含立體結構)。
(4)若高分子化合物PMMA 的相對分子質量為1.5×106,其聚合度為_______。
(5)參照上述流程,以![]() 為原料合成
為原料合成 (其它原料自選)。設計合成路線:________________________。
(其它原料自選)。設計合成路線:________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某試液中只可能含有下列K+、NH4+、Fe2+、Al3+、Cl-、SO42-、CO32-、AlO2-中的若干種離子,離子濃度均為0.1mol·L-1。某同學進行了如下實驗:
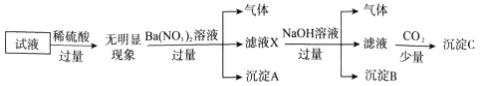
下列說法正確的是( )
A. 無法確定原試液中是否含有Al3+、Cl-
B. 濾液X中大量存在的陽離子有NH4+、Fe2+和Ba2+
C. 無法確定沉淀C的成分
D. 原溶液中存在的離子為NH4+、Fe2+、Cl-、SO42-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】因在航空、核能、電池等高技術領域的重要作用——鋰被稱為“21世紀的能源金屬”。完成下列填空:
(1)鋰位于元素周期表的________。鋰的很多化學性質與鎂相似,請依據元素周期律進行解釋:_________。
(2)氫化鋰(LiH)是離子化合物,寫出其陰離子的電子式_______________,LiH中陰離子半徑大于陽離子半徑,其原因是__________________________________________________。
(3) 工業上用Li2CO3制取鋰的化合物及金屬鋰。碳原子核外電子有________種不同能量的電子,其中有兩個電子的能量最高且能量相等,這兩個電子所處的軌道是_____________________。
(4)用Li2CO3、氨水和液溴制備LiBr·H2O的流程如下:

①合成時,除生成LiBr外,還產生了兩種參與大氣循環的氣體,補全產物并配平該反應的化學方程式:
Li2CO3+Br2+ NH3·H2O→LiBr+(___) __________。
②溴化鋰的溶解度隨溫度變化曲線如圖所示,請補全從溶液中得到LiBr·H2O晶體的實驗步驟:_____、過濾、用乙醇洗滌,干燥。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)6.02×1023個氫氧根離子的物質的量是________mol,其摩爾質量為________。
(2)在標準狀況下,0.01 mol某氣體的質量為0.44 g,則該氣體的密度為________g·L1(保留小數點后兩位),該氣體的相對分子質量為________。
(3)在標準狀況下,由CO和CO2組成的混合氣體為6.72 L,質量為12 g,此混合物中CO和CO2物質的量之比是________,CO的體積分數是________,CO的質量分數是________,C和O原子個數比是________,混合氣體的平均相對分子質量是________,密度是________g·L1。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com