
【題目】工業制得的氮化鋁(AlN)產品中常含有少量Al4C3、Al2O3、C等雜質。某同學設計如下實驗分別測定氮化鋁(AlN樣品中AlN和Al4C3的質量分數(忽略NH3在強堿性溶液中的溶解)。
(1)實驗原理:①Al4C3與硫酸反應可生成CH4;
②AlN溶于強酸產生銨鹽,溶于強堿生成氨氣,請寫出AlN與NaOH溶液反應的化學方程式:____________。
(2)實驗裝置(如圖所示,量氣管為堿式滴定管改裝)
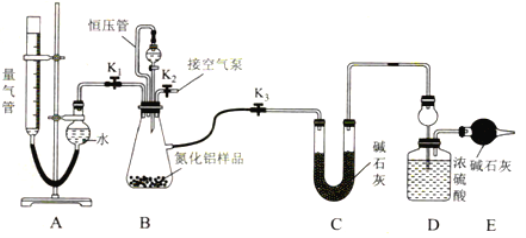
連好裝置后,首先應進行的操作是________。
(3)實驗過程:稱得裝置D的初始質量為y g;稱取x g AlN樣品置于裝置B錐形瓶中,各裝置中加入相應藥品,重新連好裝置;讀取量氣管的初始讀數為a mL(量氣裝置左右液面相平)。
①欲首先測量Al4C3質量分數的有關數據,對三個活塞的操作是________。
②若無恒壓管,對所測氣體體積的影響是________(填“偏大”“偏小”或“無影響”)
③量氣管中液面不再發生變化,說明反應已經結束。讀取讀數之前,應對量氣管進行調整量氣管高度,使左右兩邊液面相平 ,若量氣管中的液面高于右側球形容器中的液面,所測氣體的體積______(填“偏大”“偏小”或“無影響”)。
④記錄滴定管的讀數為b mL(已知:該實驗條件下的氣體摩爾體積為Vm L·mol-1),則Al4C3的質量分數為______(用含a、b、x、y、Vm的代數式表示)。
⑤測量AlN質量分數的數據:首先關閉活塞 K1 ,打開活塞K3,通過分液漏斗加入過量___,與裝置B瓶內物質充分反應;反應完成后,____(填入該步應進行的操作),最后稱得裝置D的質量為z g。
【答案】AlN+NaOH+H2O=NaAlO2+NH3↑ 檢查裝置的氣密性 關閉活塞K2、K3,打開活塞K1 偏大 偏小 ![]() ×100% NaOH溶液 打開K2,通入一段時間空氣
×100% NaOH溶液 打開K2,通入一段時間空氣
【解析】
(1)AlN與NaOH溶液反應生成偏鋁酸鈉和氨氣;
(2)涉及氣體的實驗要檢驗裝置氣密性;
(3)①欲首先測量Al4C3質量分數,需測量Al4C3與硫酸反應生成甲烷的體積;
②若無恒壓管,分液漏斗中的液體排出部分B中的空氣;
③若量氣管中的液面高于右側球形容器中的液面,則球形容器中壓強偏大;
④記錄滴定管的讀數為bm L(已知:該實驗條件下的氣體摩爾體積為Vm L·mol-1),生成甲烷的物質的量是![]() ;
;
⑤AlN與強堿生成氨氣,氨氣被D吸收,根據D的質量變化計算AlN的質量;
(1)AlN與NaOH溶液反應生成偏鋁酸鈉和氨氣,反應方程式是AlN+NaOH+H2O=NaAlO2+NH3↑;
(2)連好裝置后,首先應進行的操作檢查裝置的氣密性;
(3)①欲首先測量Al4C3質量分數,測量Al4C3與硫酸反應生成甲烷的體積,應關閉活塞K2、K3,打開活塞K1,用排水量氣法測量生成甲烷的體積;
②若無恒壓管,分液漏斗中的液體排出部分B中的空氣,測量甲烷的體積偏大;
③若量氣管中的液面高于右側球形容器中的液面,則球形容器中壓強偏大,所測氣體的體積偏小;
④記錄滴定管的讀數為b mL(已知:該實驗條件下的氣體摩爾體積為Vm L·mol-1),生成甲烷的物質的量是![]() ,根據碳元素守恒,Al4C3的物質的量是
,根據碳元素守恒,Al4C3的物質的量是![]() ,Al4C3的質量分數為
,Al4C3的質量分數為![]()
![]() 100% ;
100% ;
⑤AlN與強堿生成氨氣,所以分液漏斗加入過量NaOH溶液,與裝置B瓶內物質充分反應;反應完成后,打開K2,通一段時間空氣,將B中氨氣完全趕進D中吸收。


科目:高中化學 來源: 題型:
【題目】下圖中反應①是制備SiH4的一種方法,其副產物MgCl2·6NH3是優質的鎂資源。回答下列問題:
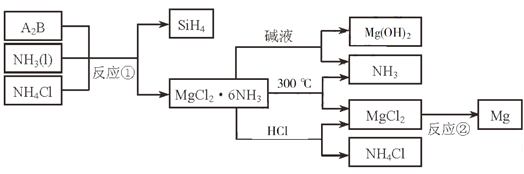
(1)MgCl2·6NH3所含元素的簡單離子半徑由小到大的順序(H-除外):_________________________,Mg在元素周期表中的位置:_____________________,Mg(OH)2的電子式:____________________。
(2)A2B的化學式為_______________。反應②的必備條件是_______________。上圖中可以循環使用的物質有_______________。
(3)在一定條件下,由SiH4和CH4反應生成H2和一種固體耐磨材料_______________(寫化學式)。
(4)為實現燃煤脫硫,向煤中加入漿狀Mg(OH)2,使燃燒產生的SO2轉化為穩定的Mg化合物,寫出該反應的化學方程式:_______________。
(5)用Mg制成的格氏試劑(RMgBr)常用于有機合成,例如制備醇類化合物的合成路線如下:
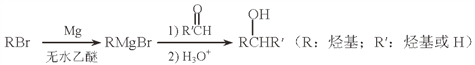
依據上述信息,寫出制備![]() 所需醛的可能結構簡式:_______________。
所需醛的可能結構簡式:_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】利用“化學計量在實驗中的應用”的相關知識進行填空(設NA表示阿伏加德羅常數的值)。
(1)標準狀況下,0.2 mol氨氣的體積是__________, 其中含有的NH3分子數是__________,
(2) 20℃時,飽和KCl溶液的密度為0.745g·cm﹣3,物質的量濃度為4.0 mol·L﹣1,則此溶液中KCl 的質量分數為______
(3)從500 mL 0.2 mol/L Na2SO4 溶液中取出10 mL,取出的Na2SO4溶液物質的量濃度為___mol/L;若將這10 mL溶液用水稀釋到100 mL,所得溶液中Na+的物質的量濃度為______mol/L。
(4)19g某二價金屬氯化物(ACl2)中含有0.4molCl-,則ACl2的摩爾質量是______;ACl2的化學式是_________。
(5)物質的量濃度相同的NaCl、MgCl2、AlCl3三種溶液,當溶液的體積比為3∶2∶1時,三種溶液中Cl-的物質的量之比為________
(6)300mL Al2(SO4)3溶液中,含Al3+為1.62g,在該溶液中加入0.1mol/L Ba(OH)2溶300mL,反應后溶液中SO42﹣的物質的量的濃度為__________(混合體積看成兩液體體積之和)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】甲烷是一種重要的化工原料和清潔能源,研究其再生及合理利用有重要意義。
請回答:
(1)已知一定條件下發生如下反應:CO2(g)+2H2O(g)![]() CH4(g)+2O2(g) △H=+802kJ·mol-1。將一定量的CO2(g)和H2O(g)充入10L密閉容器中,分別在催化劑M、N的作用下發生上述反應,CH4(g)的產量(n)與光照時間(t)和溫度(T)變化的關系如圖1所示。
CH4(g)+2O2(g) △H=+802kJ·mol-1。將一定量的CO2(g)和H2O(g)充入10L密閉容器中,分別在催化劑M、N的作用下發生上述反應,CH4(g)的產量(n)與光照時間(t)和溫度(T)變化的關系如圖1所示。
①若甲烷的燃燒熱(△H)為-890kJ·mol-1,則水的汽化熱△H=___________。(汽化熱指1mol液體轉化為氣體時吸收的熱量)
②T1℃、催化劑M作用下,0~20h內該反應速率v(H2O)=___________,該反應的平衡常數表達式K=___________
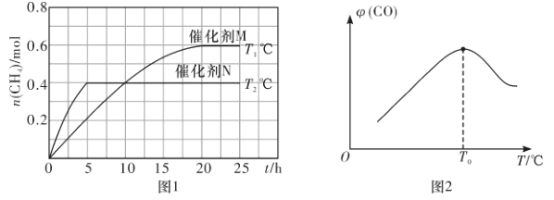
③根據圖1判斷,T1___________T2(填“>”“<”或“=”),理由為___________。
催化劑的催化效果:M___________N(填“強于”或“弱于”)。
(2)甲烷可用于制備合成氣:CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H。將CH4(g)和H2O(g)以物質的量之比為1:3充入盛有催化劑的剛性容器中發生該反應。相同時間段內測得CO的體積分數(
CO(g)+3H2(g) △H。將CH4(g)和H2O(g)以物質的量之比為1:3充入盛有催化劑的剛性容器中發生該反應。相同時間段內測得CO的體積分數(![]() )與溫度(T)的關系如圖2所示。T0℃時,CO的體積分數最大的原因為_________________________________。該反應的△H_______0(填“>”“<”)
)與溫度(T)的關系如圖2所示。T0℃時,CO的體積分數最大的原因為_________________________________。該反應的△H_______0(填“>”“<”)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)①標準狀況下,1g氫氣和14g氮氣的體積相同
②常溫常壓下,16g氧氣和臭氧的混合氣體中含有的質子數為8NA
③0.1L 0.5mol/LCH3CH2OH溶液中含有氫原子數為0.3NA
④常溫常壓下,28gCO的體積大于22.4L
⑤分子總數相等的NO2和CO2,所含氧原子數均為2NA
上述表述中正確的有:_______
(2)用容量瓶配制溶液時,由于操作不當會引起誤差
①用天平稱量時所用砝碼生銹
②用量筒量取所需濃溶液時,仰視刻度
③溶液轉移到容量瓶后,燒杯及玻璃棒未用蒸餾水洗滌
④轉移溶液前容量瓶內有少量蒸餾水
⑤定容時,俯視容量瓶的刻度線
⑥定容后搖勻,發現液面降低,又補加少量水,重新達到刻度線
上述情況會使所配溶液濃度偏低的是 :_______
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】萜品油烯(D)可用作香料的原料,它可由A合成得到如下所示,下列說法正確的是 ( )
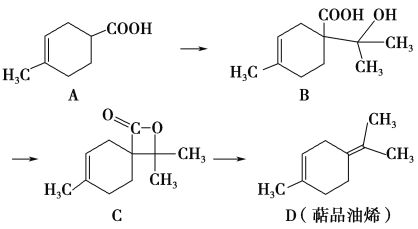
A. 有機物B的分子式為C11H19O3
B. 有機物D分子中所有碳原子一定共面
C. 1 mol有機物A中含有1.204×1024個雙鍵
D. 有機物C的同分異構體中不可能有芳香化合物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物 Urolithin A常用于合成某藥物,其結構簡式如圖所示。下列說法錯誤的是
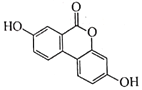
A. Urolithin A分于中苯環上的一氯代物有6種
B. Urolithin A分子中所有原子不可能共平面
C. Urolithin A能發生加成、取代和氧化反應
D. Urolithin A在稀硫酸中的水解產物含2種官能團
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)海水中蘊含的元素有80多種,它是一個巨大的寶藏。
①海水中被稱為海洋元素是___。(填元素名稱)
②下列物質不經過化學變化就能從海水中獲得的是___。(填字母)
A.單質鈉 B.單質碘 C.氯化鈉
③加碘食鹽中碘酸鉀的化學式是___。
(2)實驗室可以用高錳酸鉀和濃鹽酸反應制取氯氣,反應的化學方程式如下:2KMnO4+16HCl(濃)=2KCl+2MnCl2+5Cl2↑+8H2O
①在該反應的化學方程式上用雙線橋標出電子轉移的方向和數目___。
②該反應中濃鹽酸表現的性質有___。
③如反應中轉移了20mol電子,則產生的Cl2在標準狀況下體積為__ L。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列我國科研成果所涉及材料中,主要成分為同主族元素形成的無機非金屬材料的是
|
|
|
|
A.4.03米大口徑碳化硅反射鏡 | B.2022年冬奧會聚氨酯速滑服 | C.能屏蔽電磁波的碳包覆銀納米線 | D.“玉兔二號”鈦合金篩網輪 |
A. AB. BC. CD. D
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com