
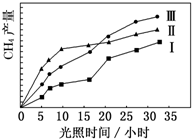
 利用光能和光催化劑,可將 CO2 和 H2O(g)轉化為 CH4 和 O2.紫外光照射時,在不同催化劑(Ⅰ,Ⅱ,Ⅲ)作用下,CH4產量隨光照時間的變化如圖所示.
利用光能和光催化劑,可將 CO2 和 H2O(g)轉化為 CH4 和 O2.紫外光照射時,在不同催化劑(Ⅰ,Ⅱ,Ⅲ)作用下,CH4產量隨光照時間的變化如圖所示.分析 (1)相同時間甲烷的物質的量的變化量越大,表明平均速率越大,相同時間甲烷的物質的量的變化量越小,平均反應速率越小.由圖2可知反應開始后的12小時內,在第Ⅱ種催化劑的作用下,收集的CH4最多;
(2)CH4(g)+H2O(g)?CO(g)+3H2(g),該反應的△H=+206kJ•mol-1,反應是吸熱反應,反應物能量低于生成物能量;依據能量變化畫出圖象.
解答 解:(1)由圖2可知,在0~30h內,甲烷的物質的量變化量為△n(Ⅰ)<△n(Ⅱ)<△n(Ⅲ),故在0~30h內,CH4的平均生成速率v(Ⅲ)>v(Ⅱ)>v(Ⅰ);
由圖2可知反應開始后的12小時內,在第Ⅱ種催化劑的作用下,收集的CH4最多;
故答案為:vⅢ>vⅡ>vⅠ;Ⅱ.
(2)CH4(g)+H2O(g)?CO(g)+3H2(g),該反應的△H=+206kJ•mol-1,反應是吸熱反應,反應過程中體系的能量變化圖為: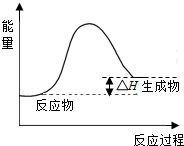 .
.
點評 本題考查了圖象分析和畫圖象的方法,題目難度中等,注意圖象信息的提取.


科目:高中化學 來源: 題型:選擇題
| A. | KNO3 | B. | CH3COONa | C. | CuSO4 | D. | Na2CO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2L 0.01mol/L的蔗糖溶液 | B. | 2L 0.01mol/L的CaCl2溶液 | ||
| C. | 1L 0.02mol/L的NaCl溶液 | D. | 1L 0.02mol/L的CH3COOH溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用Na與水反應:Na+H2O═Na++OH-+H2↑ | |
| B. | 少量Ca(HCO3)2溶液與NaOH溶液反應:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| C. | 石灰石溶于稀鹽酸:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | 鐵與硫酸銅溶液反應:2Fe+3Cu2+═2Fe3++3Cu |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ②③④⑤ | B. | ②③④ | C. | ②⑤ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 離子 | K+ | Na+ | NH4+ | H+ | SO42- | NO3- | Cl- |
| 濃度/mol•L-1 | 4×10-6 | 6×10-6 | 2×10-5 | a | 4×10-5 | 3×10-5 | 2×10-5 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.1mol/LNa2S2O3和H2SO4各5mL,加水5mL,反應溫度10℃ | |
| B. | 0.1mol/LNa2S2O3和H2SO4各5mL,加水10mL,反應溫度10℃ | |
| C. | 0.1mol/LNa2S2O3和H2SO4各5mL,加水5mL,反應溫度30℃ | |
| D. | 0.2mol/LNa2S2O3和H2SO4各5mL,加水10mL,反應溫度30℃ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| Fe3+ | Fe2+ | Cu2+ | |
| 開始沉淀時的pH | 2.7 | 7.6 | 5.2 |
| 完全沉淀時的pH | 3.7 | 9.6 | 6.4 |
| 第一次實驗 | 第二次實驗 | |
| 坩堝質量(g) | 14.520 | 14.670 |
| 坩堝質量+晶體質量(g) | 17.020 | 18.350 |
| 第一次加熱、冷卻、稱量(g) | 16.070 | 16.989 |
| 第二次加熱、冷卻、稱量(g) | 16.070 | 16.988 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com