
(9分)
Ⅰ.中和熱的測定是高中重要的定量實驗。50 mL 0.50 mol/L鹽酸與50 mL 0.55 mol/L NaOH溶液在如圖所示的裝置中進行中和反應。通過測定反應過程中所放出的熱量可計算中和熱,回答下列問題: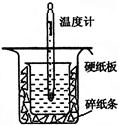
(1)從右圖實驗裝置看,其中尚缺少的一種玻璃用品是 ,除此之外,裝置中的一個明顯錯誤是 。
(2)大燒杯上如不蓋硬紙板,求得的中和熱數值將 ________ (填“ 偏大”“偏小”或“無影響”)。
Ⅱ.酸堿中和滴定是中學化學常見實驗。某學校化學課外小組用標準液鹽酸滴定未知濃度的氫氧化鈉溶液,試回答下列問題。
(1)滴定過程中,眼睛應注視 。
(2)在鐵架臺上墊一張白紙,其目的是 。
(2)某學生根據3次實驗分別記錄有關數據如下表:
| 滴定次數 | 待測NaOH溶液的體積/mL | 0.1000 mol/L鹽酸的體積/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液體積/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
(9分)
Ⅰ.(1)環形玻璃攪拌棒(1分) 大燒杯內碎紙條塞少了(或小燒杯口未用硬紙板蓋住,未將小燒杯墊的足夠高)(1分) (2)偏小(1分)
Ⅱ.(1)錐形瓶內溶液顏色的變化(1分) (2)便于觀察錐形瓶內液體顏色的變化,減小滴定誤差(1分)
(3)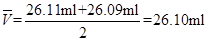 ,(1分)
,(1分)
c(NaOH)=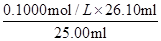 =0.1044 mol/L。(1分)
=0.1044 mol/L。(1分)
(4)a.偏高(1分) b.偏高(1分)
解析試題分析:Ⅰ.(1)從右圖實驗裝置看,其中尚缺少的一種玻璃用品是環形玻璃攪拌棒;由于該實驗的關鍵是盡可能的減少熱量的損失,所以另外一缺點就是大燒杯內碎紙條塞少了(或小燒杯口未用硬紙板蓋住,未將小燒杯墊的足夠高)。
(2)大燒杯上如不蓋硬紙板,將導致熱量損失,所以求得的中和熱數值將偏小。
Ⅱ.(1)中和滴定的關鍵問題之一是準確判斷滴定終點,所以滴定過程中,眼睛應注視錐形瓶內溶液顏色的變化。
(2)墊上一張白紙便于觀察錐形瓶內液體顏色的變化,減小滴定誤差。
(3)根據實驗得出的數據可知,第二次實驗數據完成太大,舍去,因此消耗鹽酸溶液的平均值是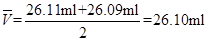 ,所以該NaOH溶液的物質的量濃度是c(NaOH)=
,所以該NaOH溶液的物質的量濃度是c(NaOH)=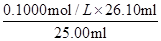 =0.1044 mol/L。
=0.1044 mol/L。
(4)根據n=c·V可知,如果觀察酸式滴定管液面時,開始俯視,滴定終點平視,則消耗鹽酸的體積偏多,因此滴定結果偏高;若將錐形瓶用待測液潤洗,然后再加入10.00 mL待測液,則消耗鹽酸的體積偏多,因此滴定結果偏高。
考點:考查反應熱的測定、中和滴定的有關計算、判斷和誤差分析
點評:該題高考中的常見圖像,屬于基礎性強試題的考查,難度不大。該題的關鍵是實驗原理,然后靈活運用即可。該題的難點在于數據處理和誤差分析。配制一定物質的量濃度溶液的實驗是中學化學中一個重要的定量實驗,實驗過程中引起溶液濃度存在誤差的因素有很多。從大的方面講,一是由實驗過程中的不規范操作引起的;二是由儀器或藥品等系統原因引起的。由于引起誤差的原因復雜,所以誤差分析就成為高考化學實驗中的一個難點


 教學練新同步練習系列答案
教學練新同步練習系列答案科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源:2012-2013年海南瓊海嘉積中學高二上高中教學質量監測理化學試卷(帶解析) 題型:填空題
(10分)某化學興趣小組要完成中和熱的測定。
(1)實驗桌上備有燒杯(大、小兩個燒杯)、泡沫塑料、泡沫塑料板、膠頭滴管、環形玻璃攪拌棒、0.5mol· L-1鹽酸、0.55mol· L-1NaOH溶液,
尚缺少的實驗玻璃用品是 、 。
(2)實驗中能否用環形銅絲攪拌棒代替環形玻璃攪拌棒?
(填“能”或“否”),其原因是 。
(3)他們記錄的實驗數據如下:
| 實 驗 用 品 | 溶 液 溫 度 | 中和熱 △H | |||
| t1 | t2 | ||||
| ① | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.3℃ | |
| ② | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.5℃ | |
查看答案和解析>>
科目:高中化學 來源:2014屆吉林省長春市高二上學期期末考試化學試卷(解析版) 題型:填空題
(9分)
Ⅰ.中和熱的測定是高中重要的定量實驗。50 mL 0.50 mol/L鹽酸與50 mL 0.55 mol/L NaOH溶液在如圖所示的裝置中進行中和反應。通過測定反應過程中所放出的熱量可計算中和熱,回答下列問題:

(1)從右圖實驗裝置看,其中尚缺少的一種玻璃用品是 ,除此之外,裝置中的一個明顯錯誤是 。
(2)大燒杯上如不蓋硬紙板,求得的中和熱數值將 ________ (填“ 偏大”“偏小”或“無影響”)。
Ⅱ.酸堿中和滴定是中學化學常見實驗。某學校化學課外小組用標準液鹽酸滴定未知濃度的氫氧化鈉溶液,試回答下列問題。
(1)滴定過程中,眼睛應注視 。
(2)在鐵架臺上墊一張白紙,其目的是 。
(2)某學生根據3次實驗分別記錄有關數據如下表:
|
滴定次數 |
待測NaOH溶液的體積/mL |
0.1000 mol/L鹽酸的體積/mL |
||
|
滴定前刻度 |
滴定后刻度 |
溶液體積/mL |
||
|
第一次 |
25.00 |
0.00 |
26.11 |
26.11 |
|
第二次 |
25.00 |
1.56 |
30.30 |
28.74 |
|
第三次 |
25.00 |
0.22 |
26.31 |
26.09 |
依據上表數據列式并計算該NaOH溶液的物質的量濃度
。
(4)下列實驗操作對滴定結果產生什么影響(填“偏高”、“偏低”或“無影響”)?
a.觀察酸式滴定管液面時,開始俯視,滴定終點平視,則滴定結果 。
b.若將錐形瓶用待測液潤洗,然后再加入10.00 mL待測液,則滴定結果 。
查看答案和解析>>
科目:高中化學 來源: 題型:
Ⅰ.中和熱的測定是高中重要的定量實驗。50 mL 0.50 mol/L鹽酸與50 mL 0.55 mol/L NaOH溶液在如圖所示的裝置中進行中和反應。通過測定反應過程中所放出的熱量可計算中和熱,回答下列問題:
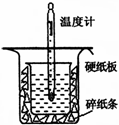
(1)從右圖實驗裝置看,其中尚缺少的一種玻璃用品是 ,除此之外,裝置中的一個明顯錯誤是 。
(2)大燒杯上如不蓋硬紙板,求得的中和熱數值將 ________ (填“ 偏大”“偏小”或“無影響”)。
Ⅱ.酸堿中和滴定是中學化學常見實驗。某學校化學課外小組用標準液鹽酸滴定未知濃度的氫氧化鈉溶液,試回答下列問題。
(1)滴定過程中,眼睛應注視 。
(2)在鐵架臺上墊一張白紙,其目的是 。
(2)某學生根據3次實驗分別記錄有關數據如下表:
| 滴定次數 | 待測NaOH溶液的體積/mL | 0.1000 mol/L鹽酸的體積/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液體積/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
依據上表數據列式并計算該NaOH溶液的物質的量濃度
。
(4)下列實驗操作對滴定結果產生什么影響(填“偏高”、“偏低”或“無影響”)?
a.觀察酸式滴定管液面時,開始俯視,滴定終點平視,則滴定結果 。
b.若將錐形瓶用待測液潤洗,然后再加入10.00 mL待測液,則滴定結果 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com