
分析 本題是探究模擬工業原理制備氨基甲酸銨,涉及利用濃氨水與氫氧化鈉固體制備氨氣,再將氨氣和二氧化碳通入四氯化碳中,不斷攪拌混合生成氨基甲酸銨,因反應是放熱反應,為了防止產物因溫度高分解及提高反應物的轉化率,選擇利用冰水進行水浴降溫,另外還涉及到產品的提純及尾氣的處理,
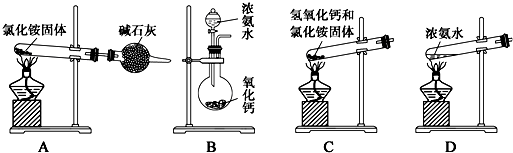
(1)A、裝置中氯化銨受熱分解生成氨氣和氯化氫,氨氣和氯化氫在冷卻時又結合成氯化銨,會堵塞導管;
B、將濃氨水滴入氧化鈣中,氧化鈣與水反應放熱,促使氨氣揮發,可以制得氨氣;
C、氯化銨與氫氧化鈣加熱分解生成氨氣,同時有水生成,試管口高于試管底,水會流入試管底部,會使試管破裂;
D、濃氨水加熱,促使氨氣揮發,可以制得氨氣;
實驗室用氯化銨與氫氧化鈣加熱制得氨氣;
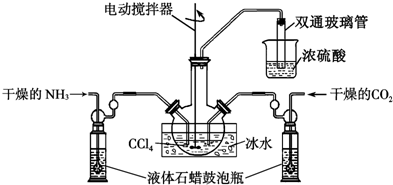
(2)①反應是放熱反應降溫平衡正向進行,液體石蠟鼓泡瓶的主要作用是控制反應進行程度,控制氣體流速和原料氣體的配比;依據反應過程中的產物分析,不能把污染性的氣體排放到空氣中,吸收易溶于水的氣體需要放倒吸;實驗中有未反應的氨氣會污染空氣,所以要進行尾氣吸收,同時要防止空氣中的水蒸氣進入裝置使氨基甲酸銨水解;
②生成的氨基甲酸銨小晶體懸浮在四氯化碳中,利用過濾得到的氨基甲酸銨(NH2COONH4)是一種白色固體,易分解,應選擇低溫干燥;
(3)根據實驗目的,檢驗氨基甲酸銨可能含有碳酸氫銨、碳酸銨中的一種或兩種,通過向試管中加入過量的BaCl2溶液,靜置溶液不變渾濁,證明固體中不含碳酸銨;在不含碳酸銨的基礎上在通過向試管中加入少量澄清石灰水,看溶液是否變渾濁證明固體中是否含有碳酸氫銨.
解答 解:本題是探究模擬工業原理制備氨基甲酸銨,涉及利用濃氨水與氫氧化鈉固體制備氨氣,再將氨氣和二氧化碳通入四氯化碳中,不斷攪拌混合生成氨基甲酸銨,因反應是放熱反應,為了防止產物因溫度高分解及提高反應物的轉化率,選擇利用冰水進行水浴降溫,另外還涉及到產品的提純及尾氣的處理,
(1)A、裝置中氯化銨受熱分解生成氨氣和氯化氫,氨氣和氯化氫在冷卻時又結合成氯化銨,會堵塞導管,故A有錯誤;
B、將濃氨水滴入氧化鈣中,氧化鈣與水反應放熱,促使氨氣揮發,可以制得氨氣,故B正確;
C、氯化銨與氫氧化鈣加熱分解生成氨氣,同時有水生成,試管口高于試管底,水會流入試管底部,會使試管破裂,故C有錯誤;
D、濃氨水加熱,促使氨氣揮發,可以制得氨氣,故D正確;
故選AC;
實驗室用氯化銨與氫氧化鈣加熱制得氨氣,反應方程式為2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3 ↑+CaCl2+2H2O,
故答案為:AC;2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3 ↑+CaCl2+2H2O;
(2)①反應2NH3(g)+CO2(g)?NH2COONH4(s)+Q,是放熱反應,降溫平衡正向進行,溫度升高;發生器用冰水冷卻提高反應物質轉化率,防止生成物溫度過高分解,液體石蠟鼓泡瓶的作用是控制反應進行程度,控制氣體流速和原料氣體的配比,雙通玻璃管的作用是防止液體倒吸,實驗中有未反應的氨氣會污染空氣,所以濃硫酸的作用是吸收多余氨氣,防止空氣中水蒸氣進入反應器使氨基甲酸銨水解,
故答案為:降溫提高反應物轉化率、防止產物分解;通過觀察氣泡,調節NH3與CO2通入比例;防止倒吸;吸收多余氨氣,防止空氣中水蒸氣進入反應器使氨基甲酸銨水解;
②生成的氨基甲酸銨小晶體懸浮在四氯化碳中,利用過濾得到的氨基甲酸銨(NH2COONH4)是一種白色固體,易分解、不能加熱烘干,應在真空40℃以下烘干,故選c,故答案為:過濾;c;
(3)根據實驗目的,檢驗氨基甲酸銨可能含有碳酸氫銨、碳酸銨中的一種或兩種,實驗操作為取少量固體樣品于試管中,加入蒸餾水至固體溶解,向試管中加入過量的BaCl2溶液,若溶液不變渾濁,證明固體中不含碳酸銨,否則含有碳酸銨;取試管中的上層清液,滴加澄清石灰水,若變渾濁,證明固體中含有碳酸氫銨,否則不含碳酸氫銨,
故答案為:取少量固體樣品于試管中,加入蒸餾水至固體溶解,向試管中加入過量的BaCl2溶液,若溶液不變渾濁,證明固體中不含碳酸銨,否則含有碳酸銨;取試管中的上層清液,滴加澄清石灰水,若變渾濁,證明固體中含有碳酸氫銨,否則不含碳酸氫銨.
點評 本題考查了物質制備實驗的設計應用,主要是氨氣的制備方法,氨基甲酸的制備實驗裝置分析判斷,實驗基本操作,混合物分離的實驗設計,有關混合物的計算,題目難度中等.


 導學與測試系列答案
導學與測試系列答案 新非凡教輔沖刺100分系列答案
新非凡教輔沖刺100分系列答案科目:高中化學 來源: 題型:選擇題
| 溫度(K) | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1173 | 2.15 | 1.67 |
| A. | △H=△H1-△H2 | |
| B. | K=$\frac{{K}_{1}}{{K}_{2}}$ | |
| C. | 該反應進行時不斷分離出H2O,可以提高CO2的轉化率和反應速率 | |
| D. | 該反應正反應為吸熱反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 石油的裂解可以提高汽油等輕質油的質量和產量 | |
| B. | 在一定條件下煤和氫氣作用得到液體燃料的過程是煤的液化途徑之一 | |
| C. | 葡萄糖、淀粉、油脂在一定條件下都能發生水解反應 | |
| D. | 往蛋白質溶液中加入飽和硫酸銨溶液,產生的沉淀再加水又可溶解 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
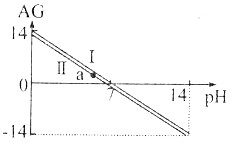
| A. | AG與pH的關系一定是AG=14-2pH | |
| B. | 直線Ⅰ和Ⅱ是因溶液的溫度不同引起的,且T(Ⅰ)>T(Ⅱ) | |
| C. | AG=0時,溶液一定呈中性 | |
| D. | a點的溶液中可以有大量Na+、Cl-、Fe3+存在 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
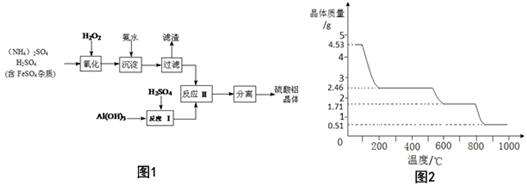
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 平衡常數的大小與溫度、濃度、壓強、催化劑等有關 | |
| B. | Ksp(AgCl)>Ksp(AgI),由此可以判斷AgCl(s)+I-(aq)?AgI(s)+Cl-(aq)能夠發生 | |
| C. | 當溫度升高時,弱酸的電離平衡常數Ka變小 | |
| D. | 化學平衡常數不變時,說明化學反應已達化學平衡狀態 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 實驗組 | 溫度/K | 平衡濃度mol/L | ||
| CH3OH | CH3OCH3 | H2O | ||
| l | 403 | 0.01 | 0.2 | 0.2 |
| 2 | 453 | 0.02 | 0.3 | 0.4 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com