
| 滴定次數 | 滴定前讀數(mL) | 滴定后讀數(mL) |
| 1 | 1.20 | 16.21 |
| 2 | 3.00 | 18.90 |
| 3 | 4.50 | 19.49 |
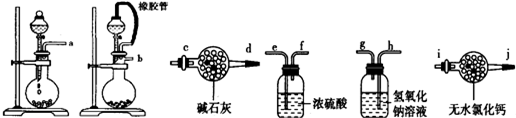
分析 I.(1)根據反應裝置--干燥裝置--吸收裝置-尾氣處理裝置排序;
(2)鹽酸和硝酸都具有揮發性;
(3)空氣中的水和二氧化碳影響實驗結果;
II.(4)酸式滴定管只能量取酸性溶液,堿式滴定管只能量取堿性溶液,根據溶液的酸堿性確定滴定管;根據滴定終點確定指示劑;滴定終點時溶液從無色變為淺紅色,30s內不褪色;根據氫氧化鈉和硫酸銨的關系式計算硫酸銨的量,最后再計算N元素的含量;
(5)在滴定實驗結束后發現滴定用的堿式滴定管玻璃尖嘴內出現了氣泡,滴定開始時無氣泡,導致硫酸銨的測定結果偏小;
解答 解:I.(1)根據反應裝置--干燥裝置--吸收裝置-尾氣處理裝置排序,所以其排列順序是:b-e,f-h,g-c,
故答案為:b-e,f-h,g-c;
(2)制取二氧化碳時需要碳酸鹽和酸反應,稀鹽酸、濃硝酸都具有揮發性,影響實驗結果,氫氧化鈉和鹽不能生成二氧化碳,故選B;
(3)為防止影響實驗結果,需要吸收二氧化碳和水蒸氣,
故答案為:防止空氣中水和二氧化碳進入裝置影響實驗結果;
II.(4)硫酸銨屬于強酸弱堿鹽,其溶液呈酸性,所以需要酸式滴定管量取硫酸銨溶液,滴定終點的pH約為8.8,酚酞的變色范圍是8-10,所以選取酚酞作指示劑;
滴定終點時,溶液從無色變為淺紅色,30s內不褪色;
2(NH4)2SO4+6HCHO=(CH2)6N4+2H2SO4+6H2O、2NaOH+H2SO4=Na2SO4+2H2O,所以硫酸銨和NaOH的關系式為:(NH4)2SO4---2NaOH,NaOH溶液的平均體積=$\frac{(16.21-1.20)+(18.90-3.00)+(19.49-4.50)}{3}$mL=15.3mL,根據(NH4)2SO4---2NaOH得m[(NH4)2SO4]=$\frac{0.0153L×0.08mol/L}{2}$=0.0808g,0.6g硫酸銨中硫酸銨的質量=0.0808g×5=0.404g,氮元素的質量分數為$\frac{0.404g×\frac{28}{132}}{0.6g}$×100%=14%,
故答案為:酸式滴定管;酚酞;溶液從無色變為淺紅色,30s內不褪色;14%;
(5)在滴定實驗結束后發現滴定用的堿式滴定管玻璃尖嘴內出現了氣泡,滴定開始時無氣泡,導致NaOH溶液的量偏小,根據(NH4)2SO4---2NaOH得,導致測定N含量偏小,故答案為:偏小.
點評 本題考查了物質含量的測定,明確實驗原理是解本題關鍵,根據物質間的反應結合實驗操作進行解答,此種類型的題閱讀量較大,同時考查書寫獲取信息、加工信息的能力,注意II(4)中酸堿指示劑的選取方法,注意取用的溶液為配制溶液的五分之一,不是全部溶液,為易錯點.


 第三學期贏在暑假系列答案
第三學期贏在暑假系列答案 學練快車道快樂假期暑假作業新疆人民出版社系列答案
學練快車道快樂假期暑假作業新疆人民出版社系列答案科目:高中化學 來源: 題型:選擇題
| A. | O2和O3互為同位素,性質相似 | |
| B. | 等質量的碳酸鈉和碳酸氫鈉粉末分別與足量同濃度的稀鹽酸反應,前者產生的二氧化碳多,后者產生二氧化碳的速率慢 | |
| C. | 明礬和漂白粉常用于自來水的凈化和殺菌消毒,兩者的作用原理相同 | |
| D. | 濃硫酸通常可用鋁槽車來運輸 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | NaNO2是氧化劑 | |
| B. | NH4Cl中的氮元素被氧化 | |
| C. | 每生成1 mol N2轉移的電子的物質的量為6 mol | |
| D. | N2既是氧化劑,又是還原劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
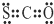
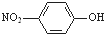
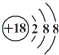

| A. | ①④⑤ | B. | ①②③④⑤ | C. | ③⑤⑥⑦ | D. | 全部正確 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NO2和N2O4組成的46g混合氣體中氮原子的數目為NA | |
| B. | 1molC2H2分子中含有σ鍵的數目為2NA | |
| C. | HClO光照分解產生22.4LO2,轉移的電子數為4NA | |
| D. | 常溫下,1L0.1mol/LFe2(SO4)3溶液中陽離子數小于0.2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 向含有CaCO3沉淀的水中通入CO2至沉淀恰好溶解,再向溶液中加入NaHCO3飽和溶液,無CaCO3沉淀產生 | |
| B. | SO2具有漂白性,將過量SO2氣體通入紫色石蕊試液時,石蕊試液先變紅后褪色 | |
| C. | CO、SO2、NO2都是對大氣產生污染的氣體,它們的空氣中都能穩定存在 | |
| D. | 類比(比較)是研究物質性質的常用辦法之一,可預測許多物質的性質.例如:將SO2通入BaCl2溶液不產生沉淀,則SO2通入Ba(NO3)2溶液也不產生沉淀 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Cl2既是氧化劑也是還原劑 | |
| B. | 被氧化的氯原子數是被還原的氯原子數的5倍 | |
| C. | 當有11.7 g的NaCl生成時,電子轉移數為0.2NA | |
| D. | NaCl是還原產物,NaClO3是氧化產物 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com