
【題目】在下列物質轉化中,已知A是一種正鹽,D的相對分子質量比C的相對分子質量大16,E是酸;當X無論是強酸還是強堿時,都有如下的轉化關系:

說明:當X是強酸時A、B、C、D、E均含同一種元素;當X是強堿時,A、B、C、D、E均含另外同一種元素。(已知H2CO3、H2S、H2SO3、H2SiO3皆為二元弱酸)
請回答下列問題:
(1)A是___________,Y是___________,Z是____________(填化學式,下同)。
(2)當X是強酸時,E是_______________,寫出B生成C的化學方程式:__________________。
(3)當X是強堿時,E是_______________,寫出D生成E的離子方程式:________________。
【答案】(NH4)2S O2 H2O H2SO4 2H2S+3O2![]() 2SO2+2H2O HNO3 4NH3+5O2
2SO2+2H2O HNO3 4NH3+5O2![]() 4NO+6H2O
4NO+6H2O
【解析】
D的相對分子質量比C的相對分子質量大16,恰好是1個O原子的相等原子質量,說明D的分子式中比C多一個O原子,且E是酸,所以D是非金屬元素的氧化物,根據所學知識判斷,D若是SO3,C是SO2;則Y是氧氣,B應是H2S,A是一種正鹽,則A是硫化物,與酸反應產生硫化氫氣體;若D是NO2,則C是NO,則B是NH3,氨氣與氧氣反應產生NO,所以A與強堿反應產生氨氣,所以A是硫化銨,Y是氧氣,Z是水。據此分析解答。
(1)根據以上分析,A、Y、Z的化學式分別為(NH4)2S ;O2 ;H2O;
(2)當X是強酸時,E是硫酸,化學式為 H2SO4;硫化氫與氧氣點燃生成二氧化硫和水,化學方程式為2H2S+3O2![]() 2SO2+2H2O;
2SO2+2H2O;
(3)當X是強堿時,E是HNO3;二氧化氮與水反應生成硝酸和NO,離子方程式為3NO2+H2O ==2H++2NO3-+NO。


 出彩同步大試卷系列答案
出彩同步大試卷系列答案科目:高中化學 來源: 題型:
【題目】25℃ 時,向體積均為20mL、濃度均為0.1000mol·L-1的三種酸HX、HY、HZ溶液中分別逐滴加入0.1000mol·L-1的NaOH溶液,所得溶液的pH與加入NaOH溶液的體積關系如圖所示。下列說法正確的是( )
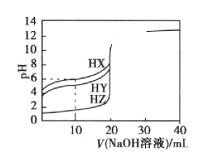
A.當V(NaOH溶液)=0mL時,三種溶液相比較c(X-)>c(Y-)>c(Z-)
B.當三種溶液pH均等于7時,反應消耗的n(HX)>n(HY)>n(HZ)
C.當V(NaOH溶液)=10mL時,反應后溶液中各離子濃度由大到小的順序為c(X-)>c(Y-)>c(Z-)>c(Na+)
D.HY與HZ混合溶液中:c(H+)=c(Y-)+c(Z-)+![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知下列反應的熱化學方程式:
6C(s)+5H2(g)+3N2(g)+9O2(g)=2C3H5(ONO2)3(l)△H1
2 H2(g)+ O2(g)= 2H2O(g)△H2
C(s)+ O2(g)=CO2(g)△H3
則反應4C3H5(ONO2)3(l)= 12CO2(g)+10H2O(g) + O2(g) +6N2(g)的△H為
A. 12△H3+5△H2-2△H1 B. 2△H1-5△H2-12△H3
C. 12△H3-5△H2-2△H1 D. △H1-5△H2-12△H3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】![]() 實驗室欲用NaOH固體配制
實驗室欲用NaOH固體配制![]() 的NaOH溶液
的NaOH溶液![]() 。
。
①本實驗必須用到的儀器有天平、藥匙、玻璃棒、燒杯、250mL容量瓶、還有_________;
②要完成本實驗該同學應稱出____________![]() ;
;
③若直接在天平的兩個托盤上放兩張質量相等的紙片進行稱量,則會使得配制結果_______。![]() 偏低、偏高或無影響
偏低、偏高或無影響![]()
![]() 鐵不能與冷、熱水反應,但能與水蒸氣反應。老師用如圖所示實驗裝置,完成還原鐵粉與水蒸氣反應的演示實驗。
鐵不能與冷、熱水反應,但能與水蒸氣反應。老師用如圖所示實驗裝置,完成還原鐵粉與水蒸氣反應的演示實驗。

①反應一段時間后,有肥皂泡吹起時,用點燃的火柴靠近肥皂泡,當_________時![]() 填實驗現象
填實驗現象![]() ,說明“鐵與水蒸氣”能夠進行反應;
,說明“鐵與水蒸氣”能夠進行反應;
②寫出該反應的化學方程式,并用單線橋表示出電子轉移情況___________;
③為了研究一定時間內鐵粉的消耗量,他們設計了如下實驗:準確稱量一定質量的鐵粉進行反應,收集并測量反應后生成的氣體體積![]() 已折算成標準狀況
已折算成標準狀況![]() 。收集并測量氣體體積應選下圖中的________裝置;
。收集并測量氣體體積應選下圖中的________裝置;

若稱取![]() 鐵粉,然后與水蒸氣加熱至無氣體放出,最好選用__________規格的量筒
鐵粉,然后與水蒸氣加熱至無氣體放出,最好選用__________規格的量筒![]() 選填字母序號
選填字母序號![]() 。
。
A.100mL B.200mL C.500mL D.1000mL
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化合物A的相對分子質量為136,其紅外光譜和核磁共振氫譜如圖,下列關于A的說法中正確的是( )

A. 若A可水解,與其同類的化合物![]() 包括
包括![]() 的同分異構體只有5種
的同分異構體只有5種
B. 符合題中A分子結構特征的有機物類型可能不只1類
C. A的可能結構中在一定條件下最多可與![]() 發生加成反應
發生加成反應
D. A一定屬于酯類化合物,在一定條件下能發生水解反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某實驗小組欲探究Na2CO3和NaHCO3的性質,發現實驗室里盛放兩種固體的試劑瓶丟失了標簽。于是,他們先對固體A、B進行鑒別,再通過實驗進行性質探究。
(1)分別加熱固體A、B,發現固體A受熱產生的氣體能使澄清石灰水變渾濁。A受熱分解的化學方程式為_____。
(2)稱取兩種固體各2g,分別加入兩個小燒杯中,再各加10 mL蒸餾水,振蕩,測量溫度變化;待固體充分溶解,恢復至室溫,向所得溶液中各滴入2滴酚酞溶液。
①發現Na2CO3固體完全溶解,而NaHCO3固體有剩余,由此得出結論_________________。
②同學們在兩燒杯中還觀察到以下現象。其中,屬于盛放Na2CO3的燒杯中出現的現象的是______(填字母序號)。
a.溶液溫度下降 b.溶液溫度升高 c.滴入酚酞后呈淺紅色 d.滴入酚酞后呈紅色
(3)如圖所示,在氣密性良好的裝置Ⅰ和Ⅱ中分別放入藥品,將氣球內的固體同時倒入試管中。

①兩試管中均產生氣體,__________(填“Ⅰ”或“Ⅱ”)的反應程度更為劇烈。
②反應結束后,氣球均有膨脹,恢復至室溫,下列說法正確的是__________。
a.裝置Ⅰ的氣球體積較大
b.裝置Ⅱ的氣球體積較大
c.生成氣體的體積根據鹽酸計算
d.生成氣體的體積根據固體計算
(4)同學們將兩種固體分別配制成0.5 mol·L-1的溶液,設計如下方案并對反應現象作出預測:
實驗方案 | 預測現象 | 預測依據 |
操作1:向2 mLNa2CO3溶液中滴加1mL 0.5mol·L-1CaCl2溶液 | 有白色沉淀 | Na2CO3溶液中的CO32—濃度較大,能與CaCl2發生反應______________(寫離子方程式) |
操作2:向2 mLNaHCO3溶液中滴加1 mL 0.5mol·L-1CaCl2溶液 | 無白色沉淀 | NaHCO3溶液中的CO32—濃度很小,不能與CaCl2反應 |
實際實驗后,發現操作2的現象與預測有差異:產生白色沉淀和氣體。則該條件下,NaHCO3溶液與CaCl2溶液反應的離子方程式為_______________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法中正確的是
A.分子組成相差一個或若干個![]() 原子團的物質互為同系物
原子團的物質互為同系物
B.相對分子質量相同的有機物互為同分異構體
C.碳原子之間只以單鍵相結合的烴一定為烷烴
D.烯烴、炔烴、芳香烴在一定條件下均能與氫氣發生加成反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列敘述中,錯誤的是
A.苯與濃硝酸、濃硫酸共熱并保持![]() 反應生成硝基苯
反應生成硝基苯
B.苯乙烯在合適條件下催化加氫可生成乙基環己烷
C.乙烯與溴的四氯化碳溶液反應生成1,![]() 二溴乙烷
二溴乙烷
D.甲苯與氯氣在光照下反應主要生成![]() 氯甲苯
氯甲苯
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氮的化合物是重要的工業原料,也是主要的大氣污染來源,研究氮的化合物的反應具有重要意義。回答下列問題:
(1)肼(N2H4)與四氧化二氮分別是火箭發射器中最常用的燃料與氧化劑。已知3.2g液態肼與足量液態四氧化二氮完全反應,生成氮氣和液態水放出熱量61. 25 kJ,則該反應的熱化學方程式為____。
(2)尾氣中的NO2可以用燒堿溶液吸收的方法來處理,其中能生成NaNO2等物質,該反應的離子方程式為____。
(3)在773 K時,分別將2.00 mol N2和6.00 mol H2充入一個固定容積為1 L的密閉容器中發生反應生成NH3,氣體混合物中c(N2)、c(H2)、c(NH3)與反應時間(t)的關系如圖所示。
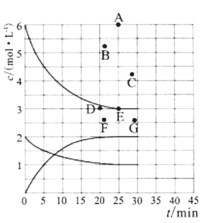
①下列能說明反應達到平衡狀態的是____(選填字母)。
a.v正(N2)=3v逆(H2) b.體系壓強不變
c.氣體平均相對分子質量不變 d.氣體密度不變
②在此溫度下,若起始充入4. 00 mol N2和12. 00 mol H2,則反應剛達到平衡時,表示 c(H2)~t的曲線上相應的點為 ___(選填字母)。
(4)在373 K時,向體積為2L的恒容真空容器中充入0.40mol NO2,發生如下反應:![]()
測得NO2的體積分數[φ(NO2)]與反應時間(t)的關系如下表:
t/min | 0 | 20 | 40 | 60 | 80 |
φ(NO2) | 1.0 | 0.75 | 0.52 | 0.40 | 0.40 |
①計算0~20min時,v(N2O4)=____。
②已知該反應![]() ,其中k1、k2為速率常數,則373K時,
,其中k1、k2為速率常數,則373K時,![]() =_____;改變溫度至T1時,k1=k2,則T1___ 373 K(填“>”“<”或“=”)。
=_____;改變溫度至T1時,k1=k2,則T1___ 373 K(填“>”“<”或“=”)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com