
【題目】830K時,在密閉容器中發生下列可逆反應:CO(g)+H2O(g)CO2(g)+H2(g)△H>0
試回答下列問題:
(1)請寫出該化學反應的平衡常數表達式: .
(2)830K溫度下,若起始時c(CO)=2molL﹣1 , c(H2O)=3molL﹣1 , 達到平衡時CO的轉化率為50%,則在該溫度下,該反應的平衡常數K= .
(3)若降低溫度,該反應的K值將 , 該反應的正反應速率將; 該反應的逆反應速率將(均填“增大”“減小”或“不變”).
(4)若要提高CO的轉化率,可采取的措施有: .
(5)830K溫度下,若起始時c(CO)=1molL﹣1 , c(H2O)=2molL﹣1 , 反應進行一段時間后,測得H2的濃度為0.5molL﹣1 , 則此時該反應是否達到平衡狀態(填“是”與“否”),你判斷的依據是
【答案】
(1)K= ![]()
(2)0.5
(3)減小;減小;減小
(4)增大水蒸氣濃度、減小二氧化碳、減小氫氣濃度或升高溫度
(5)否;濃度商= ![]() =0.33<K,平衡正向移動
=0.33<K,平衡正向移動
【解析】解:(1)化學平衡常數K等于生成物濃度冪之積與反應物濃度冪之積的比,則該反應化學平衡常數K= ![]() ;
;
所以答案是:K= ![]() ;(2)830K溫度下,若起始時c(CO)=2molL﹣1 , c(H2O)=3molL﹣1 , 達到平衡時CO的轉化率為50%,則反應的c(CO)=2mol/L×50%=1mol/L,
;(2)830K溫度下,若起始時c(CO)=2molL﹣1 , c(H2O)=3molL﹣1 , 達到平衡時CO的轉化率為50%,則反應的c(CO)=2mol/L×50%=1mol/L,
CO(g) | + | H2O(g) | = | CO2(g) | + | H2(g) | △H>0 | |
開始(mol/L) | 2 | 3 | 0 | 0 | ||||
反應(mol/L) | 1 | 1 | 1 | 1 | ||||
平衡(mol/L) | 1 | 2 | 1 | 1 |
化學平衡常數K= ![]() =
= ![]() =0.5,
=0.5,
所以答案是:0.5;(3)該反應的正反應是吸熱反應,降低溫度平衡逆向移動,化學平衡常數減小,降低溫度導致活化分子百分數減小,正逆反應速率減小,
所以答案是:減小;減小;減小;(4)要提高CO轉化率,可以通過增大水蒸氣濃度、減小二氧化碳、減小氫氣濃度、升高溫度來實現,
所以答案是:增大水蒸氣濃度、減小二氧化碳、減小氫氣濃度或升高溫度;(5)
CO(g) | + | H2O(g) | = | CO2(g) | + | H2(g) | △H>0 | |
開始(mol/L) | 2 | 3 | 0 | 0 | ||||
反應(mol/L) | 1 | 1 | 1 | 1 | ||||
平衡(mol/L) | 1 | 2 | 1 | 1 |
濃度商= ![]() =0.33<K,平衡正向移動,反應沒有達到平衡狀態,
=0.33<K,平衡正向移動,反應沒有達到平衡狀態,
所以答案是:否;濃度商= ![]() =0.33<K,平衡正向移動.
=0.33<K,平衡正向移動.
【考點精析】解答此題的關鍵在于理解化學平衡的計算的相關知識,掌握反應物轉化率=轉化濃度÷起始濃度×100%=轉化物質的量÷起始物質的量×100%;產品的產率=實際生成產物的物質的量÷理論上可得到產物的物質的量×100%.


 靈星計算小達人系列答案
靈星計算小達人系列答案科目:高中化學 來源: 題型:
【題目】4.8 g O2和0.2 mol CO2,O2的物質的量是______mol,它們的物質的量之比是________,CO2的質量是_______g,質量之比是________,在同溫同壓下的體積之比是________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】獲得中科院“百人計劃”和“863”計劃支持的環境友好型鋁碘電池是以AlI3溶液為電解質溶液,以金屬鋁和附有碘單質的石墨為電極形成的原電池.已知電池總反應為2Al+3I2═2AlI3 . 下列說法不正確的是( )
A.電池工作時,溶液中的鋁離子向正極移動
B.該電池可能是一種可充電的二次電池
C.消耗相同質量金屬時,用鋰做負極時,產生電子的物質的量比鋁多
D.該電池負極的電極反應為:Al﹣3e﹣═Al3+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用VSEPR模型預測下列分子或離子的立體結構,其中不正確的是( )
A.NH4+為正四面體形
B.CS2為直線形
C.HCN為V形
D.PCl3為三角錐形
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】我國自主研發的大飛機C919其主結構材料大量使用了鋁鋰合金,利用的是鋁鋰合金的( )
A.低密度、高強度B.高強度、導熱性
C.低密度、導電性D.導熱性、導電性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某研究性學習小組通過下列反應原理制備SO2并進行性質探究.反應原理為:Na2SO3(固)+H2SO4(濃)=Na2SO4+SO2↑+H2O 
(1)根據上述原理制備并收集干燥SO2的實驗裝置連接順序為 .
(2)D中盛裝的試劑為 .
(3)甲同學用注射器吸取純凈的SO2并結合裝置G進行SO2的性質實驗,若X是Na2S溶液,其目的是檢驗SO2的 , 可觀察到的現象 .
(4)實驗1:乙同學將溶液X換為濃度均為0.1mol/L Fe(NO3)3和BaCl2的混合溶液(已經除去溶解氧),通入少量SO2后觀察到燒杯產生白色沉淀,乙同學認為白色沉淀為BaSO4 , 為探究白色沉淀的成因,他繼續進行如下實驗驗證:(已知:0.1mol/L Fe(NO3) 3的pH=2)
實驗 | 操作 | 現象 | 結論和解釋 |
2 | 將SO2通入0.1mol/L和BaCl2混合液 | 產生白色沉淀 | Fe3+能氧化H2SO3 |
3 | 將SO2通入和 BaCl2混合液 | 產生白色沉淀 | 酸性條件NO3﹣能將H2SO3氧化為SO42﹣ |
(5)丙同學認為以上實驗只能說明Fe3+和酸性條件下NO3﹣均能將H2SO3氧化為SO42﹣ , 不能說明誰先氧化H2SO3 , 他利用提供的試劑(限選試劑:KSCN溶液,K3[Fe(CN)6]溶液,苯酚溶液,硝酸溶液)設計實驗方案探究何種微粒先發生反應.請幫助他完成方案(包括操作現象和結論):取乙同學實驗1后裝置G中燒杯的上層清液于試管中, .
(6)丁同學在實驗2過程發現,黃色溶液先變紅棕色后慢慢變淺綠色,查閱資料得:Fe3++6SO2Fe(SO2)63+(紅棕色).請用化學平衡移動原理解釋實驗2中溶液顏色變化的原因 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知Cl﹣、Br﹣、Fe2+、I﹣的還原性依次增強.現向FeBr2、FeI2的混合溶液中通入適量氯氣,溶液中某些離子的物質的量變化如圖所示,請回答: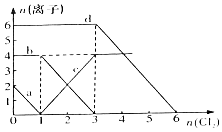
(1)a、c線分別代表溶液中、(填離子符號,下同)的變化情況.
(2)原溶液中Fe2+與Br﹣的物質的量為 .
(3)原混合溶液中FeI2的物質的量為 .
(4)當通入2mol Cl2時,溶液中離子反應為 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于有機化合物的說法正確的是( )
A.乙酸和乙酸乙酯可用Na2CO3溶液加以區別
B.戊烷(C5H12)有兩種同分異構體
C.C2H4、C3H6和 ![]() 中均含有碳碳雙鍵
中均含有碳碳雙鍵
D.糖類、油脂和蛋白質均可發生水解反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下面是用98%的濃H2SO4(ρ=1.84g/cm3)配制成0.5mol/L的稀H2SO4 500mL的操作,請按要求填空:
(1)用量筒量取所需濃H2SO4的體積為
(2)如果實驗室有15mL、20mL、50mL量筒,應選用mL量筒最好.量取時發現量筒不干凈,用水洗凈后直接量取,所配溶液濃度將(填偏高、偏低、無影響).
(3)將量取的濃H2SO4沿燒杯內壁慢慢注入盛有約100mL水的里,并不斷攪拌,目的是
(4)將冷卻后的上述溶液沿注入中,并用50mL蒸餾水洗滌燒杯次,洗滌液也要注入容量瓶中,并搖勻.如未冷卻就轉移,則所配溶液的濃度會(填偏高、偏低或無影響);若未洗滌燒杯,則所配溶液的濃度會(填偏高、偏低或無影響).
(5)加水至液面距刻度線下時,改用加水,使溶液的 .
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com