
| A. | 鋁熱反應是冶煉難熔金屬的方法之一 | |
| B. | 鋁熱劑是混合物 | |
| C. | 活潑金屬的冶煉常用電解方法,如電解NaCl溶液就可制備Na | |
| D. | 濕法煉銅的原理是 Fe+CuSO4=Cu+FeSO4 |
分析 金屬冶煉一般是用熱還原、熱分解或電解,鋁熱反應屬于熱還原法,鋁熱劑為鋁單質與不活潑金屬氧化物的混合物,制備金屬鈉采用電解熔融的氯化鈉,濕法煉銅的原理是 Fe+CuSO4=Cu+FeSO4.
解答 解:A.金屬冶煉一般是用熱還原、熱分解或電解,鋁熱反應屬于熱還原法,是冶煉難熔金屬的方法之一,故A正確;
B.鋁熱劑為鋁單質與不活潑金屬氧化物的混合物,故B正確;
C.制備金屬鈉采用電解熔融的氯化鈉,電解其溶液得不到金屬鈉,故C錯誤;
D.濕法煉銅的原理是 Fe+CuSO4=Cu+FeSO4,故D正確.
故選C.
點評 本題考查金屬的冶煉,金屬的活潑性不同,冶煉方法不同,活潑金屬采用電解法冶煉,不活潑的金屬采用直接加熱法冶煉,大部分金屬的冶煉都是在高溫下采用氧化還原反應法,題目難度不大.


 黃岡冠軍課課練系列答案
黃岡冠軍課課練系列答案科目:高中化學 來源: 題型:推斷題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 將NaOH濃溶液滴加到飽和FeCl3溶液中制備Fe(OH)3膠體 | |
| B. | 用向上排空氣法收集銅粉與稀硝酸反應產生的NO | |
| C. | 配制氯化鐵溶液時,將氯化鐵溶解在較濃的鹽酸中再加水稀釋 | |
| D. | 將Cl2與HCl混合氣體通過飽和食鹽水可得到純凈的Cl2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氧化性:ClO->I2>SO42- | |
| B. | 藍色消失的原因是Na2SO3溶液反應生成SO2具有漂白性 | |
| C. | 淀粉KI溶液變藍是因為I-被ClO-氧化為I2,I2遇淀粉變藍 | |
| D. | 若將Na2SO3溶液加入溴水,溴水褪色 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
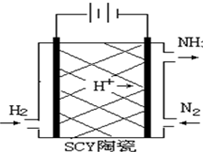 科學家采用質子高導電性的SCY陶瓷(可傳遞H+)實現了低溫常壓下高轉化率的電化學合成氨,其實驗原理示意圖如圖所示,則陰極的電極反應式是反應式為N2+6H++6e-=2NH3.
科學家采用質子高導電性的SCY陶瓷(可傳遞H+)實現了低溫常壓下高轉化率的電化學合成氨,其實驗原理示意圖如圖所示,則陰極的電極反應式是反應式為N2+6H++6e-=2NH3.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
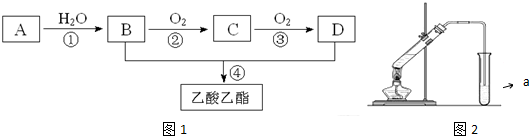
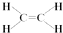 ,C的結構簡式:CH3CHO.
,C的結構簡式:CH3CHO.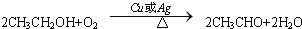 ;反應類型:氧化反應.
;反應類型:氧化反應.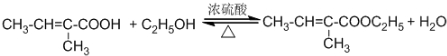 ,為從該實驗后的混合氣體中分離出乙酸乙酯,右側試管中所選用的試劑a是飽和碳酸鈉溶液,a試劑的作用是中和乙酸、吸收乙醇、降低乙酸乙酯在溶液中的溶解度,有利于分層析出.
,為從該實驗后的混合氣體中分離出乙酸乙酯,右側試管中所選用的試劑a是飽和碳酸鈉溶液,a試劑的作用是中和乙酸、吸收乙醇、降低乙酸乙酯在溶液中的溶解度,有利于分層析出.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com