
【題目】向500mL稀硝酸中加入一定質量的鐵粉,鐵粉完全溶解后,放出NO氣體5.6L(標準狀況),同時溶液質量增加9.3g,下列判斷正確的是( )
A.原溶液中投入鐵粉物質的量是0.25mol
B.原溶液中的HNO3濃度是2.0mol/L
C.反應后的溶液中還可以溶解9.6g銅
D.反應后的溶液中c(Fe2+):c(Fe3+)=1:2
【答案】B
【解析】解:生成NO的物質的量為 ![]() =0.25mol,
=0.25mol,
設Fe2+、Fe3+的物質的量分別為xmol、ymol,
由溶液質量增重9.3g,則:(x+y)mol×56g/mol﹣0.25mol×30g/mol=9.3g,
由電子轉移守恒,則:2xmol+3ymol=0.25mol×3,
聯立方程,解得x=0.15、y=0.15,
反應后c(Fe2+):c(Fe3+)為=0.15:0.15=1:1,
A.原溶液中投入鐵粉物質的量是0.15mol+0.15mol=0.3mol,故A錯誤;
B.n(HNO3)=2n(Fe2+)+3n(Fe3+)+n(NO)=2×0.15mol+3×0.15mol+0.25mol=1mol,c(HNO3)= ![]() =2mol/L,故B正確;
=2mol/L,故B正確;
C.由反應2Fe3++Cu=2Fe2++Cu2+可知,還可溶解0.075molCu,質量為0.075mol×64g/mol=4.8g,故C錯誤;
D.由以上計算可知反應后的溶液中c(Fe2+):c(Fe3+)=1:1,故D錯誤.
故選B.
溶液質量增重為參加反應Fe的質量與生成NO的質量之差,再根據電子轉移守恒列方程計算溶液中n(Fe2+)、n(Fe3+),進而計算該題.


 教材全解字詞句篇系列答案
教材全解字詞句篇系列答案科目:高中化學 來源: 題型:
【題目】已知A、B、C、D四種短周期元素的核電荷數依次增大.A原子s軌道電子數是p軌道電子數的兩倍,C原子的L能層中有兩對成對電子,C、D同主族. E、F是第四周期元素,且E位于周期表中ds區,F原子核外有33種不同運動狀態的電子.根據以上信息用相應的元素符號填空:
(1)E+核外電子排布式為 , FC43﹣離子的空間構型為 , 與其互為等電子體的一種有機分子為(填化學式).
(2)B元素所在周期第一電離能最大的元素是(填元素符號).
(3)D所在周期元素最高價氧化物對應的水化物中,酸性最強的是(填化學式);能導電的A單質與B、D、E的單質形成的晶體相比較,熔點由高到低的排列順序是(填化學式).
(4)已知EDC4溶液中滴入氨基乙酸鈉(H2N﹣CH2﹣COONa)即可得到配合物A.其結構如圖所示: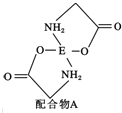
①配合物A中碳原子的軌道雜化類型為 .
②1mol氨基乙酸鈉(H2N﹣CH2﹣COONa)含有σ鍵的數目為 .
(5)化合物F2C3常用于標定未知濃度的酸性KMnO4溶液,反應生成F的最高價含氧酸,該反應的離子方程式是 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據題意填空
(1)2SO2(g)+O2(g) △ v 2 O 5 2SO3(g);△H=﹣196.6KJ/mol,是制備硫酸的重要反應.下列關于該反應的敘述正確的是 . (填字母)
A.催化劑V2O5不改變該反應的逆反應速率
B.增大反應體系的壓強,反應速率一定增大
C.該反應是放熱反應,降低溫度將縮短反應達到平衡的時間
D.在t1、t2時刻,SO3(g)的濃度分別是c1 , c2 , 則時間間隔t1~t2內,SO3(g)生成的平均速率為u= c 2 c 1 t 2 t 1
E.使用催化劑V2O5能提高SO2的轉化率
F.使用催化劑V2O5會改變該反應的△H
(2)判斷該反應達到平衡狀態的標志是 .(填字母)
a.SO2和SO3濃度相等
b.SO2百分含量保持不變
c.在體積不變的容器中,氣體的壓強不變
d.SO3的生成速率與SO2的消耗速率相等
e.在體積不變的容器中混合氣體,的密度保持不變
f.SO2、O2、SO3的濃度比保持不變.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】漂白粉在空氣中容易變質的原因是( )
A. CaCl2易吸收空氣中的水分
B. Ca(ClO)2易與鹽酸反應
C. Ca(ClO)2見光易分解
D. Ca(ClO)2易與空氣中的CO2和水作用
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知bBm+、aAn+、cCn-、dDm-(m>n>o)均具有相同的電子層結構,關于A、B、C、D四種元素的敘述正確的是( )
A. 原子半徑:A>B>C>D B. 原子序數:b>a>c>d
C. 離子半徑:D>C>B>A D. 金屬性B>A,非金屬性D>C
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列化學用語正確的是( )
A.氯化鈉的電子式: ![]()
B.聚氯乙烯的結構簡式: ![]()
C.硫離子的結構示意圖: 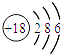
D.碳酸氫銨的電離方程式:NH4HCO3=NH4++H++CO32ˉ
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】質量分數為a%,物質的量濃度為c1 mol/L的稀硫酸蒸發水后,其質量分數變為2a%,此時物質的量濃度為c2 mol/L,則c1與c2的關系為
A. c2=2c1B. c2<2c1C. c2>2c1D. c1=2c2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學設計如圖所示元素周期表,已知Z元素的最外層電子數是次外層的3倍。空格中均有對應的元素填充。以下說法正確的是
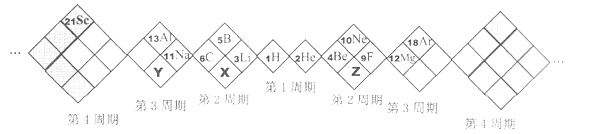
A. 白格中都是主族元素,灰格中都是副族元素
B. X和Z形成的化合物只有兩種
C. X、Y元素最高價氧化物對應的水化合物酸性:X>Y
D. X、Y、Z的氣態氫化物中最穩定的是X的氫化物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物M的結構如圖所示.關于M的描述正確的是( ) 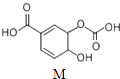
A.分子式為C8H6O6
B.能發生中和、取代、消去、氧化、加成反應
C.1molM與溴水發生反應的產物可能有3種
D.1molM與足量氫氧化鈉溶液反應,消耗4molNaOH
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com