
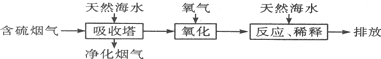
分析 (1)根據氧氣將H2SO3氧化來分析;利用酸堿反應分析混合的目的;
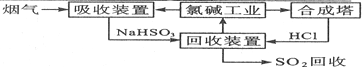
(2)①含SO2的煙氣,與NaOH反應生成NaHSO3;
②回收裝置中NaHSO3溶液與HCl反應生成NaCl溶液,NaCl溶液又是氯堿工業的原料,故循環利用的物質是NaCl溶液;
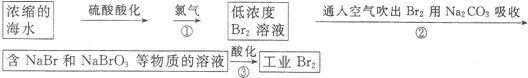
(3)由流程可知,濃縮后增大溴離子的濃度,與氯氣發生2Br-+C12=Br2+2Cl-,用空氣將溴吹出,用純堿溶液吸收,從而達到富集溴,②中發生3Br2+3Na2CO3═5NaBr+3CO2+NaBrO3,③中發生5Br-+6H++BrO3-═3Br2+3H2O,以此來解答;
(4)①石灰乳能將鎂離子轉化為沉淀;
②用作鎂蒸氣的冷卻劑,應不與Mg反應,以此來解答.
解答 解:(1)氧氣將H2SO3氧化為硫酸,該反應為2H2SO3+O2=2H2SO4,氧化后的“海水”需要用大量的天然海水與之混合后才能排放,是因中和稀釋經氧氣氧化后海水中生成的酸(H+),即NaOH與硫酸發生中和反應,
故答案為:2H2SO3+O2═2H2SO4;NaOH與硫酸發生中和反應;
(2)①氯堿工業產品之一為NaOH,用NaOH吸收SO2,其離子方程式為SO2+OH-=HSO3-,
故答案為:SO2+OH-=HSO3-;
②回收裝置中NaHSO3溶液與HCl反應生成NaCl溶液,NaCl溶液又是氯堿工業的原料,故循環利用的物質是NaCl溶液,故答案為:NaCl;
(3)由流程可知,濃縮后增大溴離子的濃度,與氯氣發生2Br-+C12=Br2+2Cl-,用空氣將溴吹出,用純堿溶液吸收,從而達到富集溴,②中發生3Br2+3Na2CO3═5NaBr+3CO2+NaBrO3,③中發生5Br-+6H++BrO3-═3Br2+3H2O,
①由上述分析可知,用Na2CO3吸收的目的是富集溴,故答案為:富集溴;
②反應③中發生5Br-+6H++BrO3-═3Br2+3H2O,由NaBrO3中溴元素的化合價降低為5-0=5可知,每生成3mol Br2,轉移電子的物質的量是5mol,故答案為:5;
③除去工業Br2中微量的Cl2,不能選碳酸鈉、亞硫酸鈉,均與溴、氯氣反應,a會引入雜質,只有b中NaBr溶液與Cl2反應,然后分液可除去Cl2,故答案為:b;
(4)①石灰乳能將鎂離子轉化為沉淀,則在母液中加入石灰乳所起的作用是沉淀Mg2+,故答案為:沉淀Mg2+;
②用作鎂蒸氣的冷卻劑,應不與Mg反應,只有A符合,而Mg與二氧化碳、氧氣、水蒸氣等均可反應,故答案為:A.
點評 本題考查海水資源的綜合利用,為高頻考點,試題知識點較多、綜合性較強,側重于學生的分析能力和實驗能力的考查,注意把握相關物質的性質,為解答該題的關鍵,題目難度中等,注意(3)③中除雜不能引入新雜質,且易于分離.


 期末沖刺100分創新金卷完全試卷系列答案
期末沖刺100分創新金卷完全試卷系列答案科目:高中化學 來源: 題型:選擇題
| 物質 | 選用試劑(過量) | 操作方法 | |
| A | Cu(CuO) | 氧氣 | 通入氧氣并加熱 |
| B | CO2(HCl) | 氫氧化鈉溶液 | 氣體通過盛有氫氧化鈉溶液的洗氣瓶 |
| C | N2(O2) | 銅粉 | 氣體通過熾熱的銅粉 |
| D | KCl溶液(K2CO3) | 氯化鈣溶液 | 加入氯化鈣溶液充分反應后過濾 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH2=CH2+HCl$\stackrel{催化劑}{→}$CH3CH2Cl 加聚反應 | |
| B. | CH3COOH+CH3CH2OH$?_{△}^{濃H_{2}SO_{4}}$CH3COOCH2CH3+H2O 酯化反應 | |
| C. | 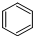 +Br2 $\stackrel{FeBr_{3}}{→}$ +Br2 $\stackrel{FeBr_{3}}{→}$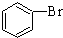 +HBr 加成反應 +HBr 加成反應 | |
| D. | 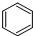 +HNO3$→_{50~60℃}^{濃H_{2}SO_{4}}$ +HNO3$→_{50~60℃}^{濃H_{2}SO_{4}}$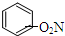 +H2O 取代反應 +H2O 取代反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,18 g H20所含的中子數為10NA | |
| B. | 一定條件下1 mol鐵粉與濃硫酸反應,轉移電子數一定為3NA | |
| C. | 在1 L的碳酸鈉溶液中,若c(CO32一)=1 mol•L-1,則Na+數目大于2NA | |
| D. | 含陰陽離子總數為4NA的固體Na202溶于水配成1 L溶液,所得溶液中Na+的物質的量濃度為2 mol•L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
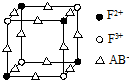 已知A、B、C、D、E、F都是周期表中前 四周期的元素,它們的核電荷數依次增大,其中A、B、C、D、E為不同主族的元素.A、C的最外層電子數都是其電子層數的2倍,B的電負性大于C,透過藍色鈷玻璃觀察E的焰色反應為紫色,F的基態原子中有4個未成對電子.
已知A、B、C、D、E、F都是周期表中前 四周期的元素,它們的核電荷數依次增大,其中A、B、C、D、E為不同主族的元素.A、C的最外層電子數都是其電子層數的2倍,B的電負性大于C,透過藍色鈷玻璃觀察E的焰色反應為紫色,F的基態原子中有4個未成對電子.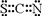 ]-,其中心原子采用sp雜化.
]-,其中心原子采用sp雜化.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 三種溶液中,相關微粒存在如下關系:c(X-)=c(Y-)+c(HY)=c(Z-)+c(HZ) | |
| B. | 三種溶液中離子濃度c(X-)<c(Y-)<c(Z-) | |
| C. | 將三種溶液均加水稀釋到1000mL后,三種溶液的pH分別為8、9、10 | |
| D. | HX、HY、HZ的酸性依次增強,電離平衡常數K(HX)>K(HY)>K(HZ) |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
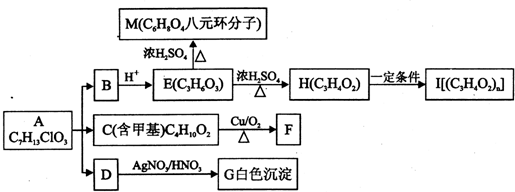
 +O2$→_{△}^{Cu}$
+O2$→_{△}^{Cu}$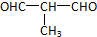 +2H2O.
+2H2O.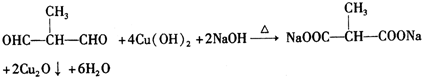 .
.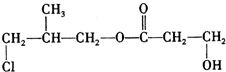
 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com