
37. (15分)
Ⅰ. 砷化鎵為第三代半導體,以其為材料制造的燈泡壽命長.耗能少。已知砷化鎵的晶胞結構如圖所示。請回答下列問題:
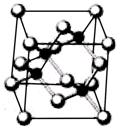
(1)下列說法正確的是__________(填序號)
A.砷化鎵晶胞結構與NaCl相同 B.第一電離能 As>Ga
C.電負性 As>Ga D.原子半徑 As>Ga
(2)砷化鎵可由(CH3)3Ga和AsH3在700℃下反應制得,反應的方程式為__________;
(3)AsH3空間形狀為___________;已知(CH3)3 Ga為非極性分子,則其中鎵原子的雜化方式為____________;
Ⅱ. 金屬銅的導電性僅次于銀,居金屬中的第二位,大量用于電氣工業。
(4)請解釋金屬銅能導電的原因 , Cu2+的核外電子排布式為__________________________。
(5)在硫酸銅溶液中通入過量的氨氣,小心蒸發,最終得到深藍色的[Cu(NH3)4]SO4晶體,晶體中含有的化學鍵除普通共價鍵外,還有 和 。
 時刻準備著暑假作業原子能出版社系列答案
時刻準備著暑假作業原子能出版社系列答案 暑假銜接教材期末暑假預習武漢出版社系列答案
暑假銜接教材期末暑假預習武漢出版社系列答案 假期作業暑假成長樂園新疆青少年出版社系列答案
假期作業暑假成長樂園新疆青少年出版社系列答案科目:高中化學 來源: 題型:
15分)有機物A、D均是重要的有機合成中間體,D被稱為佳味醇(chavicol),具有特殊芳香的液體,也可直接作農藥使用。下圖所示的是由苯酚為原料合成A、D的流程。
已知:
① (THF為一種有機溶劑)
②
③請回答下列問題:
(1)寫出A、C、D的結構簡式___________、_____________、_______________。
(2)是化合物B的一種同分異構體,用1H核磁共振譜可以證明該化合物中有______種氫處于不同的化學環境。
(3)指出有機反應類型:___________。
(4)化合物B經過下列轉化,可合成用于制造樹脂、合成橡膠乳液的有機原料丙烯酸。
①設置反應②、⑥的目的是______________________。
②寫出反應③的化學反應方程式 ___________________________。
③G與甲醇反應生成的酯H是生產丙烯酸樹脂的一種重要單體,寫出H聚合的化學反應方程式_____________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
(15分,每小題各3分)下圖中,A到L為常見物質或該物質的水溶液,B在A氣體
中燃燒產生棕黃色煙,B、G為中學化學中常見金屬單質,I的焰色反應為黃色,組成J的
元素原子核內只有一個質子,F為無色、有刺激性氣味氣體,且能使品紅溶液褪色。
回答下列問題:
(1)J的結構式為 。
(2)K的電子式為 ,屬于 晶體,所含的化學鍵有 。
(3)若D的水溶液呈黃色,沉淀H的化學式為 。
(4)若D的水溶液呈藍色,B與C反應的化學方程式為 。
(5)G與H2O反應的離子方程式為 。
查看答案和解析>>
科目:高中化學 來源: 題型:
(每空3分,共15分)根據下框圖關系,完成下列問題:
H(白色↓)不溶于鹽酸,A、B都是酸式鹽。
(1)工業生產D的典型設備是 ,工業生產F選擇的條件是
(2)石墨電極電解C溶液時陽極的電極方程式是
(3)B溶液中加入I溶液反應恰好顯中性時的離子方程式為
(4)B溶液與A溶液反應的離子方程式為
查看答案和解析>>
科目:高中化學 來源: 題型:
寫出下列反應的離子方程式:(每題3分5小題共15分)
(1)石灰石溶于稀鹽酸
(2)稀硫酸與氫氧化鋇溶液的反應
(3)碳酸鈉溶液與硝酸反應
(4)氫氧化銅與稀硫酸反應
(5)向澄清石灰水中通入少量的二氧化碳
查看答案和解析>>
科目:高中化學 來源: 題型:
(15分)向一個體積可變的密閉器中充入4molA、1molB,發生如下反應:
4A(g)+B(s) 3C(s)+4D(g)。在高溫下達到平衡,測得混合氣體中D的濃度為0.3mol·L-1。
請填寫下列空白:
(1)若容器體積為10L,反應經2min達平衡,則以A物質濃度變化表示的化學反應率為
。
(2)若壓縮容器增大壓強,則逆反應的速率 ,容器中D的體積分數 。(填“增大”“減小”“不變”)
(3)若相對分子質量M(B)>3M(C),溫度升高時混合氣體的平均相對分子質量減少,則正反應 。(填“吸熱”或“放熱”)
(4)在最初的容器改充1.5molC、4.4molD溫度保持不變,要使反應達平衡時D的濃度為0.6mol·L-1,則容器的體積是 L。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com