
【題目】我國有世界儲量第一的天然石膏(主要成分CaSO4),同時也有大量磷酸工業副產品石膏,可用于硫酸及水泥的聯合生產。硫酸鈣在高溫下被CO還原,發生的反應有:
I.CaSO4(s)+4CO(g)CaS(s)+4CO2(g) K1
II.CaSO4(s)+CO(g)CaO(s)+SO2(g)+CO2(g) K2
III.3CaSO4(s)+CaS(s)4CaO(s)+4SO2(g) K3
上述反應的平衡常數的對數值(lgK)與溫度(T)的關系如圖所示。下列說法錯誤的是( )
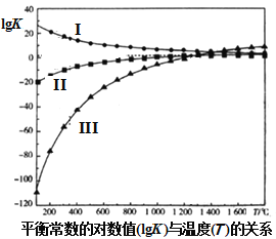
A.反應II的△H>0
B.lgK3=4lgK2lgK1
C.使用適當的催化劑能夠加快反應速率,提高原料的平衡轉化率
D.調控適當的溫度可以抑制反應I促進反應III而得到較純凈的CaO
【答案】C
【解析】
A.lgK越大,K越大,根據圖像顯示,反應II升高溫度lgK增大,反應II的K值增大,說明平衡正向移動,則正反應吸熱反應,△H>0,故A正確;
B.利用蓋斯定律,將反應Ⅱ×4反應Ⅰ得反應Ⅲ,以此可得焓變△H3=4△H2△H1,由反應轉化平衡常數時,化學計量數擴大n倍,新平衡常數是原來的n次方冪,兩方程式相減,新平衡常數為兩者之商,兩方程式相加則為兩者之積,則平衡常數K3=![]() ,則lgK3= lg
,則lgK3= lg![]() =4lgK2lgK1,故B正確;
=4lgK2lgK1,故B正確;
C.使用適當的催化劑能夠加快反應速率,但不影響平衡移動,則不能提高原料的平衡轉化率,故C錯誤;
D.lgK越大,K越大,根據圖像,反應I升高溫度,lgK減小,說明平衡逆向移動,反應I被抑制,反應III升高溫度,lgK增大,說明平衡正向移動,反應III被促進,則調控適當的溫度可以抑制反應I促進反應III而得到較純凈的CaO,故D正確;
答案選C。


 小學奪冠AB卷系列答案
小學奪冠AB卷系列答案 ABC考王全優卷系列答案
ABC考王全優卷系列答案科目:高中化學 來源: 題型:
【題目】實驗室常用王水(濃硝酸和濃鹽酸按體積比1:3的混合物)來溶解白金等貴金屬進行科學實驗。王教授用質量分數為63%的濃硝酸(密度1.40g/ ![]() )和質量分數為36.5%的濃鹽酸(密度1.19g/
)和質量分數為36.5%的濃鹽酸(密度1.19g/ ![]() )來配制王水600毫升,假設忽略兩種酸混合時的體積變化也不考慮混合后的化學變化,下列說法錯誤的是
)來配制王水600毫升,假設忽略兩種酸混合時的體積變化也不考慮混合后的化學變化,下列說法錯誤的是
A. 該王水中硝酸的物質的量濃度是3.5mol/L
B. 該王水中氧元素的質量是100.8g
C. 該王水的密度約為1.24g/ ![]()
D. 該王水中HCl的質量分數約為26.2%
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】利用廢鐵屑(主要成分為Fe,還含有C,S,P等)制取高效凈水劑K2FeO4流程如圖:

下列說法不正確的是
A. 廢鐵屑在酸溶前可用熱的純堿溶液去油污
B. 步驟②是將Fe2+轉化為Fe(OH)3
C. 步驟③中發生的反應的離子方程式為2Fe(OH)3+3ClO-==2FeO42-+3Cl-+4H++H2O
D. 步驟④中反應能發生的原因是在相同條件下,K2FeO4的溶解度小于Na2FeO4
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學小組實驗探究KI和FeCl3生成KCl、I2和FeCl2的反應存在一定限度。
實驗:i.向5mL0.1mol/L KI溶液中滴加5~6滴0.1mol/L FeCl3溶液。充分反應后,將所得溶液分成甲、乙、丙三等份;
ⅱ.向甲中滴加CCl4,充分振蕩;
ⅲ.向乙中滴加試劑X。
(1)將KI和FeCl3反應的離子方程式補充完整。_____I-+___Fe3+![]() ______I2+_______Fe2+
______I2+_______Fe2+
(2)步驟ⅲ中,試劑X是_____________。
(3)步驟ⅱ和ⅲ的實驗現象中,能說明①中反應存在一定限度的實驗現象是_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知某種鋰鹽的結構如圖,它是一種新型鋰離子電池的電解質,其陰離子由W、X、Y、Z四種同周期主族元素構成,Y原子的最外層電子數是X的次外層電子數的3倍(箭頭指向表示共用電子對由W提供)。下列說法錯誤的是( )

A.元素非金屬性強弱順序是W>Y>Z>X
B.陰離子中X與Z的雜化方式相同
C.原子半徑X>Z>Y>W
D.該物質中含有極性鍵、非極性鍵、配位鍵和離子鍵
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鉑鈷合金在磁控、儀表等領域有重要用途。回答下列問題:
(1)基態Co原子價層電子的軌道表達式為___________;Co與Ca處于同一周期,且核外最外層電子構型相同,但金屬Co的熔點比金屬Ca的高,原因為________________。
(2)Pt與Cl、吡啶(![]() )能形成如圖所示兩種分子。
)能形成如圖所示兩種分子。

①吡啶中所含同周期元素的第一電離能由小到大的順序為________________。
②1mol化合物Ⅰ中含有![]() 鍵的數目為__________________。
鍵的數目為__________________。
③相同條件下,兩種化合物中在水中溶解度更大的為__(填“Ⅰ”或“Ⅱ”),原因為____。
(3)某Pt-Co合金的晶體堆積模型為面心立方堆積,其中Co原子處于頂角位置、Pt原子處于面心位置,則該合金的化學式為_______。
(4)![]() 可用于檢驗可卡因。其中陰離子的立體構型為__,碳原子的雜化形式為____。
可用于檢驗可卡因。其中陰離子的立體構型為__,碳原子的雜化形式為____。
(5)![]() 是一種磁性材料,其晶胞結構如圖甲所示,俯視圖如圖乙所示。
是一種磁性材料,其晶胞結構如圖甲所示,俯視圖如圖乙所示。

①原子坐標參數:A為(0,0,0);B為(0.31,0.31,0)。則C原子的坐標參數為__。
②若阿伏加德羅常數的值為![]() ,則晶體密度為___
,則晶體密度為___![]() (列出計算表達式)。
(列出計算表達式)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一定溫度下,下列敘述不是可逆反應A(g)+3B(g)![]() 2C(g)達到平衡狀態標志的是( )
2C(g)達到平衡狀態標志的是( )
①C生成的速率與C分解的速率相等;②單位時間內生成a mol A,同時生成3a mol B;③A、B、C的濃度不再變化;④A、B、C的壓強不再變化;⑤混合氣體的總壓強不再變化;⑥混合氣體的物質的量不再變化;⑦單位時間內消耗a mol A,同時生成3a mol B;⑧A、B、C的分子數之比為1∶3∶2
A.②⑧B.①⑥C.②④D.③⑧
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在由Fe、FeO和Fe2O3組成的混合物中加入100mL2mol/L的鹽酸,恰好使混合物完全溶解,并放出448mL氣體(標準狀況),此時溶液中無Fe3+離子,則下列判斷正確的是
①混合物里三種物質反應時消耗鹽酸的物質的量之比為1:1:3
②反應后所得溶液中的Fe2+離子與Cl-離子的物質的量之比為1:2
③混合物里,FeO的物質的量無法確定,但Fe比Fe2O3的物質的量多
④混合物里,Fe2O3的物質的量無法確定,但Fe比FeO的物質的量多
A.②③B.①④C.②④D.①③
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有一含NaCl、Na2CO3·10H2O和NaHCO3的混合物,某同學設計如圖所示的實驗裝置,通過測量反應產生的CO2和H2O的質量,來確定該混合物中各組分的質量分數。

(1)實驗步驟:
①按圖(夾持儀器未畫出)組裝好實驗裝置后,首先進行的操作是__________。
②稱取樣品,并將其放入硬質玻璃管中,稱量裝濃硫酸的洗氣瓶C的質量和裝堿石灰的U形管D的質量。
③打開活塞K1、K2,關閉K3,緩緩鼓入空氣數分鐘,其目的是________。
④關閉活塞K1、K2,打開K3,點燃酒精燈加熱至不再產生氣體。裝置B中發生反應的化學方程式為________、________。
⑤打開活塞K1,緩緩鼓入空氣數分鐘,然后拆下裝置,再次稱量洗氣瓶C的質量和U形管D的質量。
(2)關于該實驗方案,請回答下列問題。
①若加熱反應后不鼓入空氣,對測定結果的影響是_______________。
②E處干燥管中盛放的藥品是堿石灰,其作用是_____________,如果實驗中沒有該裝置,則會導致測量結果NaHCO3的質量_____________(填“偏大”“偏小”或“無影響”)。
③若樣品質量為w g,反應后C、D裝置增加的質量分別為m1g、m2g,則混合物中Na2CO3·10H2O的質量分數為________(用含w、m1、m2的代數式表示)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com