
【題目】在溫度相同、容積均為2 L的3個恒容密閉容器中,按不同方式投入反應物,保持恒溫,測得反應達到平衡時的有關數據如下。下列說法正確的是
容器 | 甲 | 乙 | 丙 |
反應物投入量 | 1mo N2、3mol H2 | 2mol N2、6mol H2 | 2mol NH3 |
NH3濃度(mol/L) | c1 | c2 | c3 |
反應的能量變化 | 放出Q1kJ | 放出Q2kJ | 吸收Q3kJ |
體系壓強(Pa) | p1 | p2 | p3 |
反應物轉化率 | α1 | α2 | α3 |
已知N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4 kJ·mol-1
2NH3(g) ΔH=-92.4 kJ·mol-1
A. 2p1=2p3<p2 B. 達到平衡時丙容器中NH3的體積分數最大
C. α2+α3<1 D. Q1+Q3=92.4
【答案】D
【解析】
甲投入1molN2、3molH2,丙容器投入量2molNH3,恒溫恒容條件下,甲容器與丙容器是等效平衡,各組分的物質的量、含量、轉化率等完全相等;而甲容器投入1molN2、3molH2,乙容器加入2molN2、6molH2,乙中加入量是甲中的二倍,如果恒溫且乙容器容積是甲容器2倍,則甲容器與乙容器為等效平衡,所以乙所到達的平衡,可以看作在恒溫且容積是甲容器兩倍條件下,到達平衡后,再壓縮體積為與甲容器體積相等所到達的平衡,由于該反應是體積減小的反應,縮小容器體積,增大了壓強,平衡向著正向移動,所以乙中氮氣、氫氣轉化率大于甲的,平衡后乙中氨氣含量最大,據此判斷。
A、丙容器反應物投入量2molNH3,和甲起始量相同,甲和丙平衡狀態相同,乙中壓強為甲的二倍;由于乙中相當于增大壓強,平衡向著正向移動,所以乙中壓強減小,小于甲的2倍,即2p1=2p3>p2,A錯誤;
B、丙容器反應物投入量2molNH3,采用極限轉化法轉化為反應物為1molN2、3molH2,和甲中的相同,乙容器加入2molN2、6molH2,乙中加入量是甲中的二倍,乙所到達的平衡,可以看作在恒溫且容積是甲容器兩倍條件下,到達平衡后,再壓縮體積為與甲容器體積相等所到達的平衡,由于該反應是體積減小的反應,縮小容器體積,增大了壓強,平衡向著正向移動,所以乙中氮氣、氫氣轉化率大于甲的,平衡后乙中氨氣含量最大,B錯誤;
C、丙容器中加入2molNH3,和甲最后達到相同的平衡狀態,若平衡不移動,轉化率α1+α3=1;乙容器反應物投入量2mol N2、6mol H2,由于乙中相當于增大壓強,平衡向著正向移動,氨氣的轉化率增大,所以轉化率α2+α3>1,C錯誤;
D、甲投入1molN2、3molH2,丙中投入2molNH3,則甲與乙是完全等效的,根據蓋斯定律可知,甲與乙的反應的能量變化之和為92.4kJ,故Q1+Q3=92.4,D正確;
答案選D。


科目:高中化學 來源: 題型:
【題目】實驗室用含有雜質(FeO、Fe2O3)的廢CuO制備膽礬晶體,經歷了下列過程(已知 Fe3+在 pH=5時沉淀完全).其中分析錯誤的是

A. 步驟②發生的主要反應為:2Fe2++H2O2+2H+=2Fe3++2H2O
B. 步驟②不能用氯水、硝酸等強氧化劑代替H2O2
C. 步驟③用 CuCO3代替CuO也可調節溶液的pH
D. 步驟④為過濾,步驟⑤蒸發結晶
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如下圖所示,甲、乙為相互串聯的兩電解池。
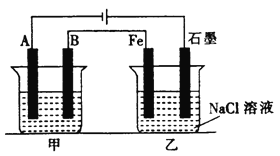
試回答:
(1)乙池中Fe電極為____________極。若在乙池中滴入少量酚酞試液,開始電解一段時間后,鐵電極附近呈_____________色。
(2)甲池若為精煉銅(假設粗銅的組成是均勻的,且其中活潑和不活潑的成份均存在)的裝置,則電解質溶液可以是________________;通過一段時間后,A電極增重12.8g,則乙池石墨電極放出的氣體在標準狀況下的體積為_____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室模擬工業漂白液(有效成分為NaClO)脫除廢水中氨氮(NH3)的流程如下:
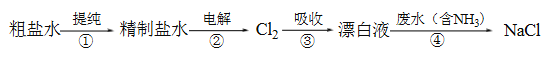
下列分析正確的是
A. ①中采用蒸餾的方法精制粗鹽水
B. ②中陽極的主要電極反應:4OH- - 4e- = 2H2O + O2↑
C. ③中制備漂白液的反應:Cl2 + OH- = Cl- + HClO
D. ②、③、④中均發生了氧化還原反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】若往20 mL 0.01 mol·L-1 HNO2(弱酸)溶液中逐滴加入一定濃度的燒堿溶液,測得混合溶液的溫度變化如圖所示。下列有關說法不正確的是

A. HNO2的電離平衡常數:c點>b點
B. b點混合溶液顯酸性:c(Na+)>c(NO2-)>c(H+)>c(OH-)
C. c點混合溶液中:c(OH-)>c(HNO2)
D. d點混合溶液中:c(Na+)>c(OH-)>c(NO2-)>c(H+)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定溫度下,向容積為2 L的恒容密閉容器中充入6molCO2 和8molH2,發生反應CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) △H= -49.0kJmol-1,測得n(H2)隨時間的變化如曲線Ⅰ所示。下列說法正確的是
CH3OH(g)+H2O(g) △H= -49.0kJmol-1,測得n(H2)隨時間的變化如曲線Ⅰ所示。下列說法正確的是
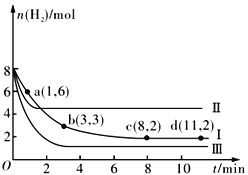
A. 該反應在0~8 min內CO2 的平均反應速率是0.375mol·L-1·min-1
B. 保持溫度不變,若起始時向上述容器中充入4molCO2、2molH2、2molCH3OH(g)和1mol H2O(g),則此時反應向正反應方向進行
C. 保持溫度不變,若起始時向上述容器中充入3molCO2 和4molH2,則平衡時H2 的體積分數等于20%
D. 改變條件得到曲線Ⅱ、Ⅲ,則曲線Ⅱ、Ⅲ改變的條件分別是升高溫度、充入氦氣
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】試直接判斷下列熱化學方程式書寫不正確的是( )
A. 1/2H2(g)+1/2Cl2(g)![]() HCl(g)ΔH=-91.5 kJ/mol
HCl(g)ΔH=-91.5 kJ/mol
B. 1/2H2(g)+1/2Cl2(g)![]() HCl(g)ΔH=+91.5 kJ/mol
HCl(g)ΔH=+91.5 kJ/mol
C. H2(g)+Cl2(g)![]() 2HCl(g) ΔH=-183 kJ/mol
2HCl(g) ΔH=-183 kJ/mol
D. 2HCl(g)![]() H2(g)+Cl2(g) ΔH=+183kJ/mol
H2(g)+Cl2(g) ΔH=+183kJ/mol
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com