
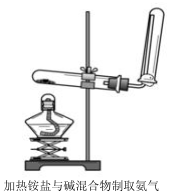
 實驗室一般采用如下裝置制取氨氣,按要求回答下列問題:
實驗室一般采用如下裝置制取氨氣,按要求回答下列問題:分析 (1)實驗室用加熱氯化銨與氫氧化鈣的方法制取氨氣,二者反應生成氯化鈣、水和氨氣;
(2)氨氣溶于水顯堿性,可以用濕潤的紅色石蕊試紙檢驗;氨氣密度小于空氣密度,收集時容易與空氣形成對流;
(3)ⅰ.依據配制一定物質的量濃度溶液的一般操作步驟選擇需要的儀器;
ii.依據溶液稀釋過程中溶質的物質的量不變計算需要濃氨水的體積,依據濃氨水體積選擇合適規格量筒;
ⅲ.分析操作對溶質的物質的量和溶液體積的影響,依據C=$\frac{n}{V}$進行誤差分析.
解答 解:(1)氯化銨與氫氧化鈣加熱反應生成氯化鈣、水和氨氣,方程式:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;
故答案為:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;
(2)氨氣溶于水顯堿性,可以用濕潤的紅色石蕊試紙檢驗;氨氣密度小于空氣密度,收集時容易與空氣形成對流,收集時,一般在管口塞一團棉花球,可減少NH3與空氣的對流速度,收集到純凈的NH3;
故答案為:紅色石蕊試紙 可減少NH3與空氣的對流速度,收集到純凈的NH3;
(3)ⅰ.配制一定物質的量濃度溶液的一般操作步驟:計算、量取、稀釋、冷卻、移液、洗滌、定容、搖勻等,用到的儀器:量筒、燒杯、玻璃棒、100mL容量瓶、膠頭滴管,用不到的儀器:燒瓶、藥匙、托盤天平;
故選:③④⑥;
ⅱ.用10mol•L-l的濃氨水配制100mLl mol•L-1的稀氨水,設需要濃氨水體積為V,則依據溶液稀釋過程中溶質的物質的量不變得:10mol/L×V=1mol/L×100mL,解得V=10.0mL,應選擇10mL量筒;
故答案為:10.0;①;
ⅲ.A.容量瓶中原來含有少量蒸餾水,對溶質的物質的量和溶液體積都不產生影響,溶液濃度不變,故A不選;
B.向容量瓶中加水定容時眼睛一直俯視刻度線,導致溶液體積偏小,溶液濃度偏高,故B選;
C.燒杯沒有洗滌,導致部分溶質損耗,溶質的物質的量偏小,溶液濃度偏低,故C不選;
D.向奔量瓶中加水定容時眼睛一直仰視刻度線,導致溶液體積偏大,溶液濃度偏低,故D不選;
故選:B.
點評 本題考查了氨氣的實驗室制備與一定物質的量濃度溶液的配制,明確氨氣制備原理及氨氣的性質,一定物質的量濃度溶液配制原理是解題關鍵,注意誤差分析的方法.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,2.24 L CCl4含有0.1 NA個CCl4分子 | |
| B. | 18gD2O含有的質子數為10NA | |
| C. | 標準狀況下,2.24 L Cl2與過量稀NaOH溶液反應,轉移的電子總數為0.2NA | |
| D. | 1.5molCu和足量稀硝酸反應產生NA個NO分子 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
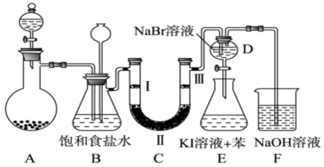
| a | b | c | d | |
| Ⅰ | 干燥的有色布條 | 干燥的有色布條 | 濕潤的有色布條 | 濕潤的有色布條 |
| Ⅱ | 堿石灰 | 硅膠 | 濃硫酸 | 無水氯化鈣 |
| Ⅲ | 濕潤的有色布條 | 濕潤的有色布條 | 干燥的有色布條 | 干燥的有色布條 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 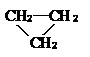 和CH3CH=CH2 和CH3CH=CH2 | B. | 淀粉和纖維素 | ||
| C. | CH3CH2CH2CH3和CH3CH2CH3 | D. | 乙烷和乙酸 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
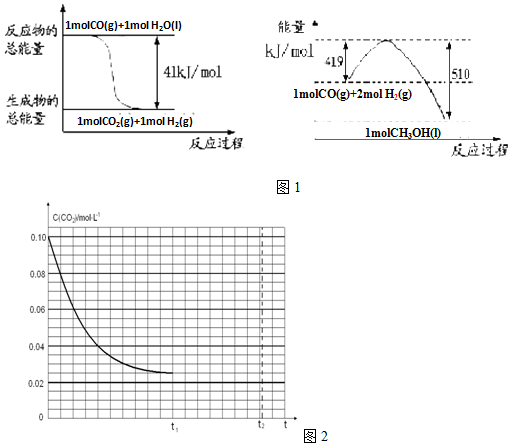
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
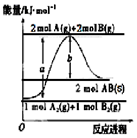
| A. | 該反應熱△H=+(a-b)kJ•mol-1 | |
| B. | AB(g)═A(g)+B(g)△H=+b/2kJ•mol-1 | |
| C. | 斷裂1 mol A-A鍵和1 mol B-B鍵,吸收a kJ能量 | |
| D. | 該反應在任何條件下都不可能自發進行 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | pH=7的溶液 | |
| B. | c(H+)=c(OH-)=10-6mol/L溶液 | |
| C. | 醋酸鈉溶液 | |
| D. | 酸與堿恰好完全反應生成正鹽的溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①③④⑥ | B. | ②③④⑤ | C. | ②④⑥⑦ | D. | ①③⑤⑦ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com