
【題目】2019年12月中旬以來,新型冠狀病毒肺炎(NCP)肆虐全球,酒精、84消毒液、雙氧水、過氧乙酸等化學品是常用的消毒劑,能夠殺死新型冠狀病毒。
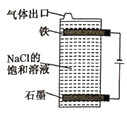
Ⅰ.如圖是簡易84消毒液發生器,寫出該電解池中發生的總反應的化學方程式:__。
Ⅱ.過氧化尿素是一種新型漂白劑、消毒劑,漂白、消毒的效果優于H2O2和過氧乙酸。
某工業用過氧化尿素的部分參數見下表:
分子式 | 外觀 | 熱分解溫度 | 熔點 | 水溶性(20℃) |
CO(NH2)2·H2O2 | 白色晶體 | 45℃ | 75~85℃ | 500g·L-1 |
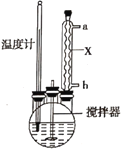
合成過氧化尿素的流程及反應器的示意圖如圖:

回答下列問題:
(1)流程中操作①的名稱為__,儀器X的名稱是__。
(2)流程中操作②的具體過程是__。
A.鹽析、過濾 B.減壓蒸餾、結晶、過濾 C.分液、過濾 D.常壓蒸餾、萃取
(3)攪拌器選用的材質是玻璃而不是鐵質的原因是__。
(4)為測定產品中活性氧的含量(含雙氧水34%,則其中活性氧為16%),一般采用KMnO4標準溶液進行滴定,但由于KMnO4的強氧化性,其溶液很容易被空氣或水中的少量還原性物質還原,生成難溶性物質MnO(OH)2,因此配制KMnO4標準溶液有如下步驟:
a.利用氧化還原滴定方法,在70~80℃條件下用基準試劑純度高、相對分子質量較大、穩定性較好的物質)溶液標定其濃度。
b.過濾得到的KMnO4溶液貯存于棕色試劑瓶中并放在暗處。
c.稱取稍多于所需量的KMnO4固體溶于水中,將溶液加熱并保持微沸![]() 。
。
d.用微孔玻璃漏斗過濾除去難溶的MnO(OH)2。
①請按照正確的流程對上述步驟進行排序__(填字母)。
②在下列物質中,用于標定KMnO4溶液的基準試劑最好選用__。
A.H2C2O4·2H2O B.FeSO4 C.濃鹽酸 D.Na2SO3
③若準確稱取Wg你選的基準試劑溶于水配成500mL溶液,取25.00mL置于錐形瓶中,用KMnO4溶液滴定至終點,消耗KMnO4溶液VmL。稱取干燥樣品1.2g,溶解后置于錐形瓶中加入1mL6mol·L-1的硫酸,然后用上述KMnO4標準溶液滴定(KMnO4溶液與尿素不反應),平行實驗三次,實驗結果如下:
實驗序號 | 1 | 2 | 3 | |
KMnO4溶液體積 (mL) | 滴定前讀數 | 0.00 | 0.00 | 1.00 |
滴定后讀數 | 19.90 | 22.70 | 21.10 |
產品中活性氧的質量分數為__(用含字母的最簡等式表示)。
【答案】NaCl+H2O![]() NaClO+H2↑ 過濾 冷凝管 B Fe會被過氧化氫氧化,且生成的Fe3+會催化過氧化氫分解 cdba A
NaClO+H2↑ 過濾 冷凝管 B Fe會被過氧化氫氧化,且生成的Fe3+會催化過氧化氫分解 cdba A ![]()
【解析】
Ⅰ.如圖是簡易84消毒液發生器,電解氯化鈉的飽和溶液,生成氫氧化鈉,氫氣,氯氣,氯氣會與氫氧化鈉反應生成次氯酸鈉,該電解池中發生的總反應為氯化鈉和水在通電的條件下生成次氯酸鈉和氫氣;
Ⅱ.(1)流程中操作①為固液分離,根據圖示儀器的結構判斷名稱;
(2)根據題中提供的過氧化尿素的物理性質分析推斷操作②的過程;
(3)雙氧水是強氧化劑,能氧化活潑金屬;
(4)①由于KMnO4的強氧化性,其溶液很容易被空氣或水中的少量還原性物質還原,生成難溶性物質MnO(OH)2,結合該性質分析配制步驟;
②選做基準試劑的物質必須滿足純度高、穩定性好,如硫酸亞鐵、亞硫酸鈉容易被氧化變質的試劑不能作為基準試劑,濃鹽酸具有揮發性,也不能做基準試劑;
③先計算草酸的物質的量濃度,再根據草酸和高錳酸鉀之間的關系式計算高錳酸鉀的物質的量濃度,再用高錳酸鉀的量計算雙氧水的質量分數,根據質量分數為34%的雙氧水,則其中活性氧為16%,計算活性氧含量。
Ⅰ.簡易84消毒液發生器,該電解池中發生的總反應的化學方程式:NaCl+H2O![]() NaClO+H2↑;
NaClO+H2↑;
Ⅱ.(1)流程中操作①從混合物中分離出固體和溶液,所以采用過濾操作;儀器X的名稱是冷凝管;
(2)根據過氧化尿素的部分參數表,45℃左右受熱易分解,熔點低,水溶性較大,需要在較低的溫度下過氧化尿素形成晶體分離,不能使用常壓蒸餾,應使用減壓蒸餾的方法,降低蒸餾操作所需的溫度,確保過氧化尿素不分解,則流程中操作②要將過氧化尿素分離出來的操作應選B;
(3)雙氧水具有氧化性,鋁、鐵具有強還原性,容易被H2O2氧化,所以攪拌器不能選擇鐵質或鋁質材料;
(4)①由于KMnO4的強氧化性,它的溶液很容易被空氣中或水中的某些少量還原性物質還原,生成難溶性物質MnO(OH)2,因此配制KMnO4標準溶液的操作如下:稱取稍多于所需量的KMnO4固體溶于水中,將溶液加熱并保持微沸![]() ,用微孔玻璃漏斗過濾除去難溶的MnO(OH)2,過濾得到的KMnO4溶液貯存于棕色試劑瓶中并放在暗處,利用氧化還原滴定方法,在70~80℃條件下用基準試劑純度高、相對分子質量較大、穩定性較好的物質)溶液標定其濃度,順序為cdba;
,用微孔玻璃漏斗過濾除去難溶的MnO(OH)2,過濾得到的KMnO4溶液貯存于棕色試劑瓶中并放在暗處,利用氧化還原滴定方法,在70~80℃條件下用基準試劑純度高、相對分子質量較大、穩定性較好的物質)溶液標定其濃度,順序為cdba;
②A.H2C2O42H2O常溫下是穩定的結晶水水化物,溶于水后純度高、穩定性好,可以用作基準試劑,故A正確;
B.FeSO47H2O在空氣中不穩定,亞鐵離子容易被氧化成鐵離子,不宜用作基準試劑,故B錯誤;
C.濃鹽酸不穩定,易揮發,不宜用作基準試劑,故C錯誤;
D.Na2SO3具有還原性,在空氣中容易被氧化成硫酸鈉,不宜用作基準試劑,故D錯誤;
答案選A;
③草酸的物質的量濃度為: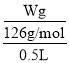 =
=![]() mol/L,根據反應方程式6H++2MnO4-+5H2C2O42H2O═2Mn2++10CO2↑+18H2O中草酸和高錳酸鉀之間的關系式得,酸性高錳酸鉀的物質的量濃度=
mol/L,根據反應方程式6H++2MnO4-+5H2C2O42H2O═2Mn2++10CO2↑+18H2O中草酸和高錳酸鉀之間的關系式得,酸性高錳酸鉀的物質的量濃度=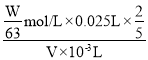 =
=![]() mol/L;根據得失電子守恒知,5H2O2~2KMnO4,n(H2O2)=
mol/L;根據得失電子守恒知,5H2O2~2KMnO4,n(H2O2)=![]() n(KMnO4),由于第2組數據偏差較大,應舍去,所以消耗高錳酸鉀溶液的體積為實驗1和實驗3兩組的平均值,即20.00 mL,n(H2O2)=
n(KMnO4),由于第2組數據偏差較大,應舍去,所以消耗高錳酸鉀溶液的體積為實驗1和實驗3兩組的平均值,即20.00 mL,n(H2O2)=![]() ×
×![]() mol·L-1×0.02 L=
mol·L-1×0.02 L=![]() mol,雙氧水的質量分數=
mol,雙氧水的質量分數=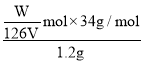 =
=![]() ×100%,根據質量分數為34%的雙氧水,其中活性氧為16%,則產品中活性氧的質量分數為
×100%,根據質量分數為34%的雙氧水,其中活性氧為16%,則產品中活性氧的質量分數為![]() ×100%×
×100%×![]() =
=![]() 。
。


 千里馬走向假期期末仿真試卷寒假系列答案
千里馬走向假期期末仿真試卷寒假系列答案科目:高中化學 來源: 題型:
【題目】控制適合的條件,將反應Fe3++AgFe2++Ag+設計成如下圖所示的原電池(鹽橋裝有瓊脂-硝酸鉀溶液;靈敏電流計的0刻度居中,左右均有刻度)。已知接通后,觀察到電流計指針向右偏轉。下列判斷不正確的是
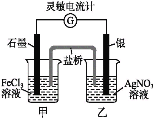
A. 在外電路中,電子從銀電極流向石墨電極
B. 鹽橋中的K+移向甲燒杯
C. 一段時間后,電流計指針反向偏轉,越過0刻度,向左邊偏轉
D. 電流計指針居中后,往甲燒杯中加入一定量的鐵粉,電流計指針將向左偏轉
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知HF分子在一定條件下會發生二聚反應:2HF(g)(HF)2(g)。經實驗測得,不同壓強下,體系的平均相對分子質量(M=![]() )隨溫度(T)的變化曲線如圖所示,下列說法正確的是( )
)隨溫度(T)的變化曲線如圖所示,下列說法正確的是( )
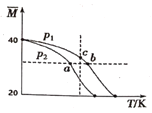
A.該反應的ΔH>0B.氣體的壓強:p(a)>p(b)=p(c)
C.平衡常數:K(a)=K(b)<K(c)D.測定HF的相對分子質量要在低壓、高溫條件下
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】普通水泥在固化過程中自由水分子減少并產生Ca(OH)2,溶液呈堿性。根據這一物理化學特點,科學家發明了電動勢法測水泥初凝時間。此方法的原理如圖所示,反應的總方程式為:2Cu+Ag2O=Cu2O+2Ag,下列有關說法正確的

A.Cu為正極,Ag2O為負極
B.電池工作時,OH—向正極移動
C.正極的電極反應為:2Cu+2OH——2e—=Cu2O+H2O
D.外電路中每通過2mol電子,正極質量減少16g
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物X的蒸氣相對氫氣的密度為51,X中氧元素的質量分數為31.5%,則能與NaOH溶液發生反應的X的同分異構體有(不考慮立體異構)( )
A. 15種B. 14種C. 13種D. 12種
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】H2(g)+2ICl(g)→2HCl(g)+I2(g)能量曲線如圖。描述正確的是
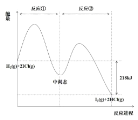
A.反應①為吸熱反應
B.若加入催化劑可降低反應熱
C.I2(g)+2HCl(g)的能量高于 I2(s)+2HCl(g)的總能量
D.熱化學方程式為 H2(g)+2ICl(g)→2HCl(g)+I2(g)-218kJ
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】金屬鉻和氫氣在工業上都有重要的用途。已知:鉻能與稀硫酸反應,生成氫氣和硫酸亞鉻(CrSO4)。銅鉻構成原電池如圖所示,鹽橋中裝的是飽和KCl瓊脂溶液,下列關于此電池的說法正確的是

A.鹽橋的作用是使整個裝置構成通路、保持溶液呈電中性,凡是有鹽橋的原電池,鹽橋中均可以用飽和KCl瓊脂溶液
B.理論上1molCr溶解,鹽橋中將有2molCl-進入左池,2molK+進入右池
C.此過程中H+得電子,發生氧化反應
D.電子從鉻極通過導線到銅極,又通過鹽橋到轉移到左燒杯中
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某校課外活動小組為了探究銅與稀硝酸反應產生的是NO氣體,設計了如下實驗。實驗裝置如圖所示(已知NO、NO2能與NaOH溶液反應):
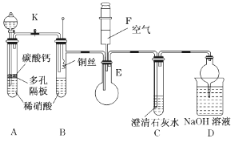
(1)設計裝置A的目的是_____________________________________,為達此目的應進行的操作______________________________________________________。
(2)在(1)中的操作后將裝置B中銅絲插入稀硝酸,并微熱之,觀察到裝置B中的現象是____________________________________________________________;B中反應的離子方程式是_____________________________________________________。
(3)將注射器F中的空氣推入E中,E中的氣體變為紅棕色,該實驗的目的是____________。
(4)D裝置的作用是_______________________________________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com