
【題目】乳酸亞鐵晶體{[CH3CH(OH)COO]2Fe·3H2O}(相對分子質量:288),可由乳酸與FeCO3反應制得,它易溶于水,幾乎不溶于乙醇,是一種很好的補鐵劑,但其水溶液易被氧化,光照可促進氧化。
I.制備碳酸亞鐵:裝置如圖所示。
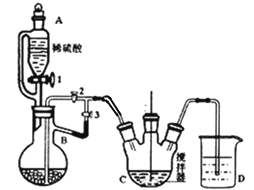
鋅鐵 NH4HCO3溶液
(1)儀器B的名稱是________。
(2)實驗操作如下:關閉活塞2,打開活塞1、3,加入適量稀硫酸反應一段時間,其目的是____________________________,然后關閉活塞1,接下來的操作是____________________,此后,C裝置溶液中有沉淀生成,并有大量氣泡冒出,則C中發生反應的離子方程式為_____________________________________。
Ⅱ.制備乳酸亞鐵:
(3)向純凈的FeCO3固體加入足量乳酸溶液,在75℃下攪拌使之充分反應。該反應的加熱方式為____________。為防止乳酸亞鐵變質,在上述體系中還應加入適量鐵粉。反應結束后,將所得溶液隔絕空氣低溫濃縮、_________、過濾、洗滌、干燥,得乳酸亞鐵晶體。該晶體存放時應注意_________________________。
III.乳酸亞鐵晶體純度的測量:
(4)某同學查閱文獻后,用(NH4)4Ce(SO4)4滴定法測定樣品中Fe2+的含量并計算樣品純度(反應中Ce4+還原為Ce3+),他稱取6.00g樣品,配制成250.00mL溶液,取出25.00mL,用濃度為0.10mol·L-1的(NH4)4Ce(SO4)4標準溶液滴定至終點,消耗標準液20.00mL。則產品中乳酸亞鐵晶體的純度為________(以質量分數表示)。
【答案】蒸餾燒瓶 排盡裝置內的空氣,防止Fe2+被氧化 打開活塞2,關閉活塞3 Fe2++2HCO3-=FeCO3↓+CO2↑+H2O 水浴75℃加熱 冷卻結晶 避光、密封保存 96%
【解析】
利用鐵與稀硫酸反應生成的氫氣,將生成的硫酸亞鐵溶液壓入碳酸氫銨溶液中,從而制得碳酸亞鐵;控制一定條件,碳酸亞鐵與乳酸反應生成乳酸亞鐵溶液,經冷卻結晶制得乳酸亞鐵晶體;因為亞鐵具有還原性,可用氧化還原滴定法測定其純度。
I.(1)儀器B是蒸餾燒瓶。
(2)關閉活塞2,打開活塞1、3時,稀硫酸與鐵反應生成硫酸亞鐵溶液和氫氣,氫氣可排出裝置內空氣,防止亞鐵被氧化。然后關閉活塞1,打開活塞2,關閉活塞3,此時生成的氫氣使蒸餾燒瓶中壓強變大,硫酸亞鐵溶液沿導管上升,經活塞2進入三頸燒瓶,進而發生反應生成碳酸亞鐵沉淀和氣體,故C中離子方程式為Fe2++2HCO3-=FeCO3↓+CO2↑+H2O。
Ⅱ.(3)FeCO3固體溶于足量的乳酸溶液需要75℃、攪拌條件,可采用75℃水浴加熱,同時加入適量鐵粉防止亞鐵被氧化。乳酸亞鐵晶體含結晶水,只能使用冷卻結晶方法,故將生成的乳酸亞鐵溶液在隔絕空氣條件下,經低溫濃縮、冷卻結晶、過濾、洗滌、干燥,得乳酸亞鐵晶體。據題意,乳酸亞鐵易被空氣中氧氣氧化,且光照可促進氧化,故保存乳酸亞鐵晶體應密封、避光。
III.(4)滴定過程中發生反應Fe2++Ce4+=Fe3++Ce3+,得關系式[CH3CH(OH)COO]2Fe·3H2O ~ (NH4)4Ce(SO4)4。
25.00mL樣品溶液中n(Fe2+)=n(Ce4+)=0.10mol·L-1×20.00×10-3L=2.000×10-3mol
6.00g樣品中,n(Fe2+)=2.000×10-3mol×![]() =2.000×10-2mol
=2.000×10-2mol
產品中乳酸亞鐵晶體的純度=![]() =96%
=96%


 海淀黃岡名師導航系列答案
海淀黃岡名師導航系列答案 普通高中同步練習冊系列答案
普通高中同步練習冊系列答案 優翼小幫手同步口算系列答案
優翼小幫手同步口算系列答案科目:高中化學 來源: 題型:
【題目】氮化硼(BN)晶體有多種相結構。六方相氮化硼是通常存在的穩定相,與石墨相似,具有層狀結構,可作高溫潤滑劑,但不能導電。立方相氮化硼是超硬材料,有優異的耐磨性。它們的晶體結構如圖所示。關于這兩種晶體的說法,正確的是
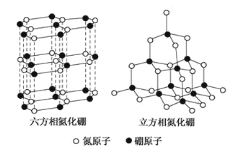
A. 立方相氮化硼含配位鍵B→N
B. 六方相氮化硼層間作用力小,所以質地軟,熔點低
C. 兩種氮化硼中的硼原子都是采用sp2雜化
D. 六方相氮化硼晶體其結構與石墨相似卻不導電,原因是沒有可以自由移動的電子
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】1.52 g銅鎂合金完全溶解于50 mL密度為1.40 g/mL、質量分數為63%的濃硝酸中,得到NO2和N2O4的混合氣體1120 mL(標準狀況),向反應后的溶液中加入1.0 mol/L NaOH溶液,當金屬離子全部沉淀時,得到2.54 g沉淀。下列說法不正確的是( )
A.該合金中銅與鎂的物質的量之比是2:1
B.該濃硝酸中HNO3的物質的量濃度是14.0 mol/L
C.得到2.54 g沉淀時,加入NaOH溶液的體積是600 mL
D.NO2和N2O4的混合氣體中,NO2的體積分數是80%
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用混有硫酸亞鐵和硫酸鎂等雜質的錳礦(含MnO2、MnCO3)生產硫酸錳,實驗室模擬生產過程如下:
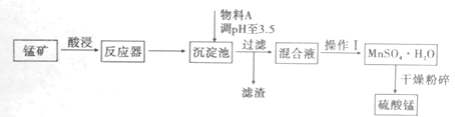
已知金屬離子完全沉淀時的pH值如下:Fe3+:3.5;Fe2+:9.5;Mn2+:10.8;Mg2+:11.6。
(1)反應器中發生氧化還原反應的離子方程式是________。
(2)從經濟效益考慮,物料A可以是________。
(3)硫酸錳和硫酸鎂的溶解度曲線如右圖所示:
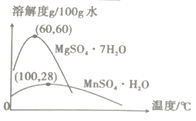
則操作Ⅰ包含的主要操作為________。
(4)MnSO4·H2O在1150℃條件下分解,產物是Mn2O4、含硫化合物、水,在該條件下硫酸錳晶體分解反應的化學方程式是________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定溫度下,某容器中加入足量的碳酸鈣,發生反應CaCO3(s)![]() CaO(s)+CO2(g),達到平衡,下列說法正確的是
CaO(s)+CO2(g),達到平衡,下列說法正確的是
A. 將體積縮小為原來的一半,當體系再次達到平衡時,CO2的濃度不變
B. 將體積增大為原來的2倍,再次達到平衡時,氣體的密度變大
C. 因CaCO3(s)需加熱條件才分解生成CaO(s)和CO2(g),所以是△H<0
D. 保持容器壓強不變,充入He,平衡向逆反應方向進行
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25 ℃時,在“H2A—HA-—A2-”的水溶液體系中,H2A、HA-和A2- 三者中各自所占的物質的量分數(α)隨溶液pH變化的關系如圖所示。下列說法正確的是

A. 在含H2A、HA-和A2- 的溶液中,加入少量NaOH固體,α(HA-)一定增大
B. 將等物質的量的NaHA和Na2A混合物溶于水,所得溶液中α(HA-)=α(A2-)
C. NaHA溶液中,HA-的水解能力大于HA-的電離能力
D. 在含H2A、HA-和A2-的溶液中,若c(H2A)+2c(A2-)+c(OH-)=c(H+),則α(H2A)與α(HA-)不一定相等
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:D為烴;E分子中碳元素與氫元素的質量之比6∶1,相對分子質量為44,其燃燒產物只有CO2和H2O。A的最簡式與F相同,且能發生銀鏡反應,可由淀粉水解得到。
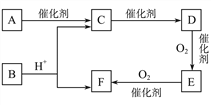
(1)A的結構簡式為__________________。
(2)寫出D→E的化學方程式:_______________________。
(3)下列說法正確的是____。
A.有機物F能使石蕊溶液變紅
B.用新制的氫氧化銅無法區分有機物C、E、F的水溶液
C.等物質的量的C和D分別完全燃燒消耗氧氣的量相等
D.可用飽和碳酸鈉溶液除去有機物B中混有的少量C、F
E. B的同分異構體中能發生銀鏡反應的酯類共有2種
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列表示式錯誤的是( )
A. Na+的軌道表示式:![]() B. Na+的結構示意圖:
B. Na+的結構示意圖:![]()
C. Na的電子排布式:1s22s22p63s1 D. Na的外圍電子排布式:3s1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】含鉻化合物有毒,對人畜危害很大。因此含鉻廢水必須進行處理才能排放。已知:Cr3+![]() Cr(OH)3
Cr(OH)3![]() CrO2-。
CrO2-。
(1)在含+6價鉻的廢水中加入一定量的硫酸和硫酸亞鐵,使+6價鉻還原成+3價鉻;再調節溶液pH在6~8之間,使Fe3+和Cr3+轉化為Fe(OH)3、Cr(OH)3沉淀而除去。
①寫出Cr2O72-與FeSO4溶液在酸性條件下反應的離子方程式_______________________。
②用離子方程式表示溶液pH不能超過10的原因__________________________________。
③若處理后的廢水中殘留的c(Fe3+)=2×10-13 mol/L,則殘留的Cr3+的濃度為___________。(已知:Ksp[Fe(OH)3]=4.0×10-38 Ksp[Cr(OH)3]=6.0×10-31)
(2)將含+6價鉻的廢水放入電解槽內,用鐵作陽極,加入適量的氯化鈉進行電解。陽極區生成的Fe2+和Cr2O72一發生反應,生成的Fe3+和Cr3+在陰極區與OH一結合成氫氧化物沉淀而除去。
①寫出陰極的電極反應式__________________________。
②電解法中加入氯化鈉的作用是______________________。
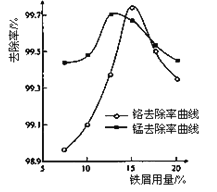
(3)某化學興趣小組以含+6價鉻和+2價錳的工業廢水為試樣,研究鐵屑用量和pH對廢水中鉻、錳去除率的影響。
①取100mL廢水于250 mL三角瓶中,調節pH到規定值,分別加入不同量的廢鐵屑.得到鐵屑用量對鉻和錳去除率的影響如下圖所示。則在pH一定時,廢水中鐵屑用量為____________時,錳、鉻去除率最好。
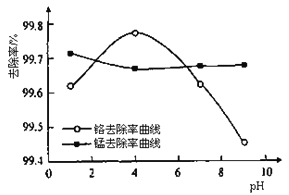
②取100mL廢水于250 mL三角瓶中,加入規定量鐵粉,調成不同的pH。得到pH對鉻和錳去除率的影響如下圖所示。則在鐵屑用量一定時,廢水pH=__________時錳、鉻去除率最好。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com