
有A、B、C、D、E、F六種物質,它們之間相互轉化關系如圖所示(條件及部分產物未標出)。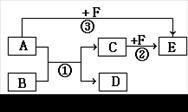
(1)若A、D為氣體,都能使澄清的石灰水變渾濁;B、F做焰色反應,透過藍色鈷玻璃觀察為紫色, B、C為正鹽,F的溶液為紫紅色。則C和F在酸性溶液中發生反應②的離子方程式為 。
(2)若1 mol A分子中含有3 mol極性共價鍵, B、C、F都是短周期元素組成的非金屬單質;常溫下,只有D為固體,其它為氣體。則反應③的化學方程式為 。
某同學設計了如圖所示裝置(夾持儀器省略)進行上述(2)中物質B的化學性質探究。
①你認為此裝置設計是否合理?若不合理如何改進: 。(若合理此問不答)
②Ⅱ中產生的現象是 。
③反應幾分鐘后,檢驗Ⅲ中可能含有的金屬陽離子的實驗操作是 。
④通過以上探究,氣體B的主要化學性質是 。
(12分)(1)5SO32-+2MnO4-+6H+=2Mn2++5SO42-+3H2O (2分)
(2)4NH3+5O2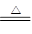 4NO + 6 H2O (2分)
4NO + 6 H2O (2分)
①不合理,應在Ⅰ、Ⅱ之間加上除去HCl的裝置。 (2分)
②石蕊溶液先變紅后褪色 (2分)
③取溶液少許分別加入兩支試管中,向其中一只滴加硫氰化鉀溶液,若溶液變紅,則含有Fe3+;
向另一只試管中滴加鐵氰化鉀溶液,若產生藍色沉淀,則含有Fe2+。(每個離子1分,共2分)
④強氧化性,能與水、與堿反應,水溶液具有酸性和氧化(漂白)性 (2分,對3個全分)
解析試題分析:(1)若A、D為氣體,都能使澄清的石灰水變渾濁,這說明二者是CO2和SO2;B、F做焰色反應,透過藍色鈷玻璃觀察為紫色,說明含有鉀元素。 F的溶液為紫紅色,這說明F是高錳酸鉀。由于F能和A反應,說明A是具有還原性的,所以A是SO2,D是CO2。B、C為正鹽,所以B是碳酸鉀,C是亞硫酸鉀。則C和F在酸性溶液中發生反應②的離子方程式為5SO32-+2MnO4-+6H+=2Mn2++5SO42-+3H2O。
(2)若1 mol A分子中含有3 mol極性共價鍵,因此A是氨氣。B、C、F都是短周期元素組成的非金屬單質;常溫下,只有D為固體,其它為氣體,這說明B應該是氯氣,C是氮氣,D是氯化銨,F是氧氣,E是NO,則反應③的化學方程式為4NH3+5O2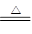 4NO + 6 H2O。
4NO + 6 H2O。
①由于在制備氯氣時,濃鹽酸具有揮發性,所以生成的氯氣中含有氯化氫,或干擾后續的實驗,因此是不合理,應在Ⅰ、Ⅱ之間加上除去HCl的裝置,可以用飽和的食鹽水除去氯化氫。
②氯氣溶于水生成鹽酸和次氯酸,具有酸性和強氧化性,所以Ⅱ中產生的現象是石蕊溶液先變紅后褪色。
③氯氣具有強氧化性,能把氯化亞鐵氧化生成氯化鐵,所以反應幾分鐘后,檢驗Ⅲ中可能含有的金屬陽離子的實驗操作是取溶液少許分別加入兩支試管中,向其中一只滴加硫氰化鉀溶液,若溶液變紅,則含有Fe3+;向另一只試管中滴加鐵氰化鉀溶液,若產生藍色沉淀,則含有Fe2+。
④根據以上分析可知,氯氣的主要性質是強氧化性,能與水、與堿反應,水溶液具有酸性和氧化(漂白)性。
考點:考查無機框圖題的判斷、氯氣制備以及性質的檢驗的實驗探究
點評:該題是中等難度的試題,試題綜合性強,對學生的思維能力要求高,有利于培養學生的邏輯推理能力和發散思維能力,也有助于培養學生規范、嚴謹的實驗設計能力。該題的難點是框圖題的判斷,需要注意的是化學推斷題是一類綜合性較強的試題,如元素及化合物性質和社會生活,環境保護,化學計算等知識,還可引入學科間綜合。它不僅可考察學生對化學知識的理解程度,更重要的是培養學生的綜合分析能力和思維方法。解框圖題的方法:最關鍵的是尋找“突破口”,“突破口”就是抓“特”字,例如特殊顏色、特殊狀態、特殊氣味、特殊反應、特殊現象、特殊制法、特殊用途等。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:單選題
下圖裝置可用于收集氣體并驗證其化學性質,下列對應關系完全正確的是
| | 氣體 | 試劑 | 現象 | 結論 |
| A | NO | 紫色石蕊試液 | 溶液變紅 | NO與水反應生成硝酸 |
| B | Cl2 | NaBr溶液 | 溶液呈橙黃色 | 氯的非金屬性大于溴 |
| C | SO2 | 酸性KMnO4溶液 | 溶液褪色 | SO2有漂白性 |
| D | NH3 | MgCl2溶液 | 產生白色沉淀 | NH3有堿性 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
碳酸鈣和硫酸鈣都是鈣的重要化合物,它們在生產生活中都有著廣泛的應用。甲、乙兩組同學分別對碳酸鈣的制備、硫酸鈣的性質進行了以下探究,請你參與并完成對有關問題的解答。
(1)甲組使用大理石(含少量的Fe2O3雜質)等物質制備碳酸鈣的實驗流程如下: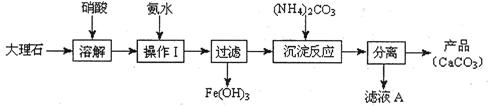
①溶解大理石時,用硝酸而不用硫酸的原因是 。
②上述流程中,“分離”得產品所包含的實驗操作依次為:過濾、 、 。
③“濾液A”中除H+離子外,還含有的陽離子是 ;檢驗該陽離子的實驗方法是:取少量濾液A與 在試管中混合、加熱充分反應,將濕潤的紅色石蕊試紙(或pH試紙)靠近試管口,觀察現象即可。
(2)乙組對某硫酸鈣晶體(xCaS04·yH20)加熱分解的有關反應進行探究。他們取6.52g該晶體進行加熱,加熱過程中,固體質量隨時間的變化情況如下圖所示。又知t5~t6時間段內固體質量減輕的原因是產生了兩種氣體,反應的化學方程式為:2CasO4 2CaO+2S02↑+O2↑。
2CaO+2S02↑+O2↑。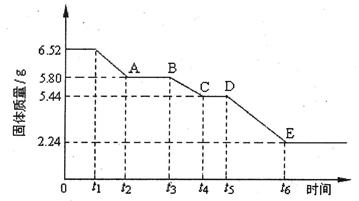
①加熱時,該晶體開始發生化學變化的時間是 (填“t1”、“t3”或“t5”)。
②t4~t5時間段固體的化學式為 。
③tl~t2時間段固體發生反應的化學方程式為 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
有幾個實驗小組的同學,利用下圖裝置進行“一器多用”的實驗探究(a中盛放的液體均勻慢速滴下;b中盛放的藥品足量;若在c、d中盛裝液體,則長導管均浸入液面以下),每組同學設想在a、b、c、d中分別盛放不同物質,來制取某種氣體并檢驗其性質。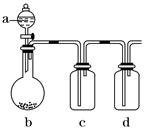
請你回答以下各組同學在交流實驗設計方案中提出的問題:
Ⅰ.(1)若a:濃鹽酸;b:高錳酸鉀(其氧化性比二氧化錳強很多);c:紅色鮮花瓣。在實驗過程中c中的現象_____________________________________________________________。
d裝置中盛放藥品的作用是______________________________,請寫出d中反應的離子方程式: ___________________________________________________________________。
(2)若a:稀鹽酸;b:貝殼粉;c:飽和碳酸鈉溶液;d:飽和Na2SiO3溶液。在實驗過
程中,c中出現的現象是____________________。d中現象是____________,這說明
________________________________________________________________________。
Ⅱ.你認為四組同學在制取氣體之前都應進行的操作是________________。你還可以利用此裝置的a和b兩部分制取的氣體有(只寫一種)_________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
以白云石(化學式表示為MgCO3·CaCO3)為原料制備Mg(OH)2的工藝流程如下圖所示。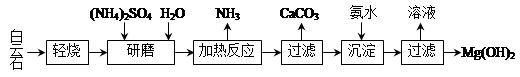
(1)研磨的作用是 。
(2)該工藝中可循環使用的物質是 、 (寫化學式)。
(3)白云石輕燒的主要產物是MgO·CaCO3,而傳統工藝是將白云石加熱分解為MgO和CaO后提取,白云石輕燒的優點是 。
(4)加熱反應的離子方程式為 。
(5)①加熱反應時,在323k和353k溶液中c(NH4+)與反應時間的關系如下圖所示,請在下圖畫出373k的曲線。
②由圖可知,隨著溫度升高: 。
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
為探索工業含鋁、鐵、銅合金廢料的再利用,甲同學設計的實驗方案如下:
請回答:
(1)綠礬的化學式為 。
(2)寫出反應①的化學方程式 ,
反應②生成沉淀的離子反應方程式 。
(3)為了檢測濾液D中含有的金屬離子,可設計實驗方案為(試劑自選): 。
(4)在濾渣B中滴加稀硫酸時,發現反應速率比一般的鐵粉反應要快,其原因是 。
(5)若考慮綠色化學工藝,在濾渣E中加入稀硫酸和試劑Y制膽礬晶體,試劑Y為無色液體,則反應④的總化學方程式為 ;若不考慮綠色化學工藝,所選試劑Y為1mol/L的硝酸,欲使3molCu全部溶解且溶液中含銅元素的溶質僅為CuSO4,則需該硝酸的體積 L。
堿石灰
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
鈦白粉(主要成分是TiO2),廣泛用于油漆、塑料、造紙等行業,還可用作乙醇脫水、脫氫的催化劑。下圖是以鈦鐵礦(主要成分FeTiO3,鈦酸亞鐵)為主要原料生產鈦白粉并獲得副產品FeSO4·7H2O的工藝流程圖。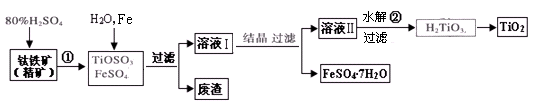
(1)鈦鐵礦與硫酸發生反應①的化學方程式為 ;在TiOSO4和FeSO4溶液中加入Fe的目的是 。
(2)溶液Ⅱ中TiOSO4在加熱條件下發生水解反應②的離子方程式為 ;可回收利用的物質是 。
(3)為測定溶液Ⅱ中TiOSO4的含量,首先取待測鈦液10 mL用水稀釋至100 mL,加過量鋁粉,充分振蕩,使其完全反應:3TiO2+ +Al+6H+=3Ti3++Al3++3H2O。過濾后,取出濾液20.00 mL,向其中滴加2~3滴KSCN溶液作指示劑,用 (填一種玻璃儀器的名稱)滴加0.1000mol·L-1 FeCl3溶液,當溶液出現紅色達到滴定終點,用去了30.00mL FeC13溶液。待測鈦液中TiOSO4的物質的量濃度是 。
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
[實驗化學]
對硝基苯甲酸在醫藥、感光材料等工業中應用廣泛。以對硝基甲苯等為原料制取對硝基苯甲酸(黃色結晶,熔點242 ℃,沸點約359 ℃,微溶于水,能升華。)的反應原理為: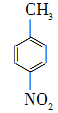 +Na2Cr2O7+4H2SO4―→
+Na2Cr2O7+4H2SO4―→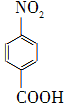 +Na2SO4+Cr2(SO4)3+5H2O
+Na2SO4+Cr2(SO4)3+5H2O
某小組以對硝基甲苯等物質為原料制取對硝基苯甲酸的實驗裝置如下圖所示(加熱和儀器固定裝置均已略去),實驗步驟如下:
步驟1:向250 mL三頸燒瓶中依次加入適量的對硝基甲苯、重鉻酸鈉粉末、水,并充分混合。在攪拌下,用滴液漏斗滴入適量濃硫酸后,加熱0.5 h至反應液呈黑色。
步驟2:待反應混合物冷卻后,和適量冰水充分混合,抽濾并用50 mL水分兩次洗滌。將洗滌后的固體放入盛有適量5%硫酸溶液中,水浴加熱10 min,冷卻后抽濾。
步驟3:將抽濾后的固體溶于適量5%NaOH溶液中,50 ℃溫熱后抽濾,在濾液中加入少量活性炭,煮沸后趁熱抽濾。將得到的濾液慢慢加入到盛有適量15%硫酸溶液的燒杯中,析出黃色沉淀,抽濾,冷水洗滌,干燥得粗產品。
(1) 在步驟1中“攪拌”是用電動攪拌器完成的,這樣操作的好處有________、________。
(2) 在三頸燒瓶中,隨著濃硫酸的加入,反應溫度迅速上升,為使反應溫度不致過高,必要時可采取的措施是________。
(3) 在步驟2中,抽濾所得固體的主要成分是________。抽濾裝置所包含的儀器除減壓系統外,還有________、________(填儀器名稱)。
(4) 步驟3用NaOH溶液進行處理的作用主要是____。
用NaOH溶液處理后,需50 ℃溫熱后抽濾的原因是____。
(5) 制得的粗產品需要進一步精制(純化),根據對硝基苯甲酸的有關性質可知,對其進行精制(純化)可以用乙醇溶液完成,也可以采用________法完成。
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
(15分)已知:BaSO4(s)+4C(s) 高溫4CO(g)+BaS(s)
工業上以重晶石礦(主要成分BaSO4,含雜質Fe2O3、SiO2)為原料,通過下列流程生產氯化鋇晶體(BaCl2·nH2O)。
(1)若按以上流程在實驗室焙燒重晶石礦,回收處理所產生的氣體,恰當的方法是 (填字母編號)。
a.用澄清石灰水吸收氣體 b.用濃硫酸吸收氣體 c.點燃氣體
(2)焙燒重晶石礦時,可能發生的副反應的化學方程式是 (寫兩個)。
(3)為測定產品氯化鋇晶體(BaCl2·nH2O)中的n值,設計下列實驗步驟,請補充完善空缺項的實驗步驟:①稱量樣品;②灼燒樣品;③置于 (填儀器名稱)中冷卻;④ ;⑤恒重操作。恒重操作的目的是 ;若最終測出的n值偏大,可能的實驗操作誤差原因是 (舉例一種情況)。
(4)用下列裝置組合也可完成(3)中實驗。請選擇下列恰當的裝置組合(稱量、加熱和夾持儀器省略),完成上述實驗: (用裝置代號以“A
 ……
…… ”形式表示,每套裝置不可重復使用)
”形式表示,每套裝置不可重復使用)
(5)將重晶石礦與碳、氯化鈣共同焙燒,可以直接得到氯化鋇,反應的化學方程式為:
BaSO4+4C+CaCl2高溫4CO +CaS+BaCl2。以下是從焙燒后的固體中分離得到氯化鋇晶體的實驗流程設計(已知硫化鈣不溶于水,易溶于鹽酸)。請在空格方框橫線上填寫操作名稱。
+CaS+BaCl2。以下是從焙燒后的固體中分離得到氯化鋇晶體的實驗流程設計(已知硫化鈣不溶于水,易溶于鹽酸)。請在空格方框橫線上填寫操作名稱。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com