
【題目】食鹽是日常生活的必需品,也是重要的化工原料。粗食鹽常含有少量CaCl2、MgCl2、Na2SO4等雜質(zhì),實驗室提供的試劑如下:飽和Na2CO3溶液、飽和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、75%乙醇、四氯化碳。實驗室提純NaCl的流程如下:

(1)欲除去溶液I中的雜質(zhì),寫出A所代表的多種試劑,按滴加順序依次為I. NaOH;II.____;III._________(填化學(xué)式)。
(2)請寫出下列試劑加入時發(fā)生反應(yīng)的化學(xué)方程式:
①加入試劑I:_______。 ②加入鹽酸:_______。
(3)操作a、b中均用到的玻璃儀器是______(填儀器名稱),操作c的名稱為_____。
(4)洗滌除去NaCl晶體表面附帶的少量KCl,選用的試劑為_____(從提供的試劑中選)。
(5)若上述流程中未進(jìn)行操作b,即直接向溶液I中加鹽酸到pH為4~5,過濾,得到沉淀X和溶液Y,則沉淀X為______(寫離子符號),溶液Y仍含有的雜質(zhì)金屬離子是_______(寫離子符號)。
【答案】 BaCl2溶液 飽和Na2CO3溶液 MgCl2+2NaOH=Mg(OH)2↓+2NaCl NaOH+HCl=NaCl+H2O、Na2CO3+2HCl=2NaCl+H2O+CO2↑ 燒杯、玻璃棒 蒸發(fā)濃縮 75%乙醇 BaSO4 Ca2+ 、Ba2+、Mg2+
【解析】試題分析:本題以粗鹽提純的流程為載體,考查流程的分析,物質(zhì)的分離提純和基本實驗操作。粗食鹽常含有少量CaCl2、MgCl2、Na2SO4等雜質(zhì),根據(jù)題目提供的試劑,選用飽和Na2CO3溶液除去CaCl2、NaOH溶液除去MgCl2、BaCl2溶液除去Na2SO4,由于所加除雜試劑過量,所以Na2CO3溶液必須在BaCl2溶液之后加入,即Na2CO3溶液不僅除去CaCl2還要除去過量的BaCl2,在此過程中發(fā)生的反應(yīng)有:2NaOH+MgCl2=Mg(OH)2↓+2NaCl、Na2SO4+BaCl2=BaSO4↓+2NaCl、CaCl2+Na2CO3=CaCO3↓+2NaCl、BaCl2+Na2CO3=BaCO3↓+2NaCl。過濾后獲得的濾液中含有過量NaOH和Na2CO3,加入鹽酸除去過量NaOH和Na2CO3,反應(yīng)的方程式為:NaOH+HCl=NaCl+H2O、Na2CO3+2HCl=2NaCl+H2O+CO2↑。將獲得的NaCl溶液經(jīng)過蒸發(fā)濃縮、冷卻獲得NaCl晶體。
(1)根據(jù)上述分析,A中試劑滴加順序依次為:I.NaOH,II.BaCl2溶液,III.飽和Na2CO3溶液。
(2)①加入NaOH除去MgCl2,反應(yīng)的化學(xué)方程式為2NaOH+MgCl2=Mg(OH)2↓+2NaCl。
②加入鹽酸除去過量的NaOH和Na2CO3,反應(yīng)的方程式為:NaOH+HCl=NaCl+H2O、Na2CO3+2HCl=2NaCl+H2O+CO2↑。
(3)操作a為溶解,用到的玻璃儀器為燒杯、玻璃棒;操作b為過濾,用到的玻璃儀器為燒杯、玻璃棒、漏斗;操作a、b都用到的玻璃儀器為燒杯、玻璃棒。操作c為將NaCl溶液變成糊狀物,操作c為蒸發(fā)濃縮。
(4)洗滌除去NaCl晶體表面附帶的少量KCl選用75%乙醇,不能選擇四氯化碳,因為KCl不溶于CCl4。
(5)若上述流程中未進(jìn)行操作b,直接加入鹽酸,Mg(OH)2溶于鹽酸轉(zhuǎn)化成可溶性的MgCl2,CaCO3、BaCO3溶于鹽酸分別轉(zhuǎn)化成可溶性的CaCl2、BaCl2,BaSO4不溶于鹽酸,則沉淀X為BaSO4,溶液Y中仍含有的雜質(zhì)金屬離子是Ca2+、Ba2+、Mg2+。


科目:高中化學(xué) 來源: 題型:
【題目】已知:還原性HSO3->I-,氧化性IO3->I2。在含3mol NaHSO3的溶液中逐滴加人KIO3溶液。加入KIO3和析出I2的物質(zhì)的量的關(guān)系曲線如圖所示。下列說法不正確的是
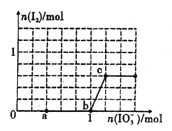
A. 0-a段發(fā)生反應(yīng):3HSO3-+IO3-=3SO42-+I-+3H+
B. a~b段共消耗NaHSO3的物質(zhì)的量為1.8mol
C. b~c段反應(yīng):氧化產(chǎn)物為I2
D. 當(dāng)溶液中I-與I2的物質(zhì)的量之比為5 : 1時,加入的KIO3為1.lmol
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】POC13常用作半導(dǎo)體摻雜劑及光導(dǎo)纖維原料,實驗室制備POC13并測定產(chǎn)品含量的實驗過程如下:
I.實驗室制備POC13。
采用氧氣氧化液態(tài)PCl3法制取POC13,實驗裝置(加熱及夾持儀器略)如圖:

資料:①Ag+SCN-==AgSCN↓:Ksp(AgCl)>Ksp(AgSCN);
②PCl3和POC13的相關(guān)信息如下表:
物質(zhì) | 熔點/℃ | 沸點/℃ | 相對分子質(zhì)量 | 其他 |
PCl3 | -112.0 | 76.0 | 137.5 | 兩者互溶,均為無色液體,遇水均劇烈反應(yīng)生成含氧酸和氯化氫 |
POC13 | 2.0 | 106.0 | 153.5 |
(1)B中所盛的試劑是________,干燥管的作用是_____________________。
(2)POC13遇水反應(yīng)的化學(xué)方程式為____________________________。
(3)裝置B的作用除干燥O2外,還有_____________________________。
(4)反應(yīng)溫度要控制在60~65℃,原因是:____________________________。
II.測定POC13產(chǎn)品的含量。
實驗步驟:
①制備POC13實驗結(jié)束后,待三頸瓶中的液體冷卻至室溫,準(zhǔn)確稱取30.7g POC13產(chǎn)品,置于盛有60.00 mL蒸餾水的水解瓶中搖動至完全水解,將水解液配成100. 00 mL溶液。
②取10. 00 mL溶液于錐形瓶中,加入10.00 mL 3.2mol/L AgNO3標(biāo)準(zhǔn)溶液。
③加入少許硝基苯用力搖動,使沉淀表面被有機(jī)物覆蓋。
④以X為指示劑,用0.2 mol/L KSCN溶液滴定過量的AgNO3溶液,達(dá)到滴定終點時共用去l0.00 mLKSCN溶液。
(5)步驟③中加入硝基苯的作用是__________________________。
(6)步驟④中X為____________________ 。
(7)反應(yīng)中POC13的百分含量為_________,通過__________(填操作)可以提高產(chǎn)品的純度。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】碳及其化合物在能源、材料等方面具有廣泛的用途。回答下列問題:
(1)天然氣是目前應(yīng)用較為廣泛的能源之一,天然氣中除含主要成分甲烷外,還含有乙烷、丙烷等,乙烷的電子式為 。
(2)碳酸和草酸均為二元弱酸,其電離均為分步電離,二者的電離常數(shù)如下表:
H2CO3 | H2C2O4 | |
K1 | 4.2×107 | 5.4×102 |
K2 | 5.6×1011 | 5.4×105 |
①向碳酸鈉溶液中滴加少量草酸溶液所發(fā)生反應(yīng)的離子方程式為 。
②濃度均為0.1 mol·L1的Na2CO3溶液、NaHCO3溶液、Na2C2O4溶液、NaHC2O4溶液,其溶液中H+濃度分別記作c1、c2、c3、c4。則四種溶液中H+濃度由大到小的順序為 。
(3)常溫時,C和CO的標(biāo)準(zhǔn)燃燒熱分別為394.0 kJ·mol1、283.0 kJ·mol1,該條件下C轉(zhuǎn)化為CO的熱化學(xué)方程式為 。
(4)氫氣和一氧化碳在一定條件下可合成甲醇,反應(yīng)如下:
2H2(g)+CO(g)![]() CH3OH(g) ΔH=Q kJ·mol1
CH3OH(g) ΔH=Q kJ·mol1
①該反應(yīng)在不同溫度下的化學(xué)平衡常數(shù)(K)如下表:
溫度/℃ | 250 | 300 | 350 |
K/L2·mol2 | 2.041 | 0.270 | 0.012 |
由此可判斷Q (選填“ >”或“<”)0。
②一定溫度下,將6 mol H2和2 mol CO充入體積為2 L的密閉容器中,10 min反應(yīng)達(dá)到平衡狀態(tài),此時測得c(CO)=0.2 mol·L1,該溫度下的平衡常數(shù)K= ,0~10 min內(nèi)反應(yīng)速率v(CH3OH)= 。
③在兩個密閉容器中分別都充入20 mol H2和10 mol CO,測得一氧化碳的平衡轉(zhuǎn)化率隨溫度(T)、壓強(qiáng)(p)的變化如圖所示:

A、B兩點的壓強(qiáng)大小關(guān)系:p1 (選填“ >”、“=”或“<”)p2。若A點對應(yīng)容器的容積為20 L,則B點對應(yīng)容器的容積為 L。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】污染物的有效去除和資源的充分利用是化學(xué)造福人類的重要研究課題。工業(yè)上以硫鐵礦為原料制硫酸所產(chǎn)生的尾氣除了含有N2、O2外,還含有SO2。為了保護(hù)環(huán)境,同時提高硫酸工業(yè)的綜合經(jīng)濟(jì)效益,應(yīng)盡可能將尾氣中的SO2轉(zhuǎn)化為有用的產(chǎn)品。
治理方案Ⅰ:
(1)將尾氣通入氨水中,能發(fā)生多個反應(yīng),寫出其中可能發(fā)生的兩個氧化還原反應(yīng)的化學(xué)方程式:_______________、_______________。
治理方案Ⅱ:
某研究小組利用軟錳礦(主要成分為MnO2,另含有少量鐵、鋁、銅、鎳等金屬化合物)作脫硫劑,通過如下流程既去除尾氣中的SO2,又制得電池材料MnO2 (反應(yīng)條件已省略)。

請回答下列問題:
(2)用MnCO3能除去溶液中Al3+和Fe3+其原因是___________________________,用MnS除去溶液中的Cu2+的離子方程式為_______________。
(3)流程圖④過程中發(fā)生的主要反應(yīng)的化學(xué)方程式為___________________。
(4)MnO2可作超級電容器材料。工業(yè)上用下圖所示裝置制備MnO2。接通電源后,A電極的電極反應(yīng)式為:_______________,當(dāng)制備lmol MnO2,則膜兩側(cè)電解液的質(zhì)量變化差(△m左-△m右)為_______________g。

查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】下列有關(guān)氫原子(用H表示)與氫分子的說法中錯誤的是( )
A. 化學(xué)能:2molH >1molH2 B. H原子間發(fā)生碰撞就能轉(zhuǎn)化為H2
C. 穩(wěn)定性:H<H2 D. H2→2H的過程是吸熱過程
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】下列敘述中正確的是( )
A. 向NaHCO3溶液中滴加澄清石灰水,不會產(chǎn)生沉淀
B. 等質(zhì)量NaHCO3和Na2CO3分別與足量鹽酸反應(yīng),生成的CO2在同溫同壓下體積相同
C. 向Na2CO3溶液中緩慢通入等物質(zhì)的量的HCl,生成的CO2與原Na2CO3的物質(zhì)的量之比為1:2
D. 向Na2CO3飽和溶液中通入CO2,有晶體析出
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com