
H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三種形態的粒子的分布分數δ隨溶液pH變化的關系如圖所示[已知Ksp(CaC2O4)=2.3×10-9].下列說法正確的是( )
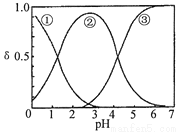
A.曲線①代表的粒子是HC2O4-
B.0.1 mol•L-1 NaHC2O4溶液中:c(C2O42-)>c(H2C2O4)
C.pH=5時,溶液中主要含碳物種濃度大小關系為:c(C2O42-)>c(H2C2O4)>c(HC2O4-)
D.一定溫度下,往CaC2O4飽和溶液中加入少量CaCl2固體,c(C2O42-)將減小,c(Ca2+)不變
 期末復習檢測系列答案
期末復習檢測系列答案 超能學典單元期中期末專題沖刺100分系列答案
超能學典單元期中期末專題沖刺100分系列答案 黃岡360度定制密卷系列答案
黃岡360度定制密卷系列答案 陽光考場單元測試卷系列答案
陽光考場單元測試卷系列答案科目:高中化學 來源:2016-2017學年河北省高二下學期3月月考化學試卷(解析版) 題型:選擇題
為了證明液溴與苯發生的反應是取代反應,有如下圖所示裝置.則裝置A中盛有的物質是

A. 水 B. NaOH溶液 C. CCl4 D. NaI溶液
查看答案和解析>>
科目:高中化學 來源:2016-2017學年江蘇省高一下學期期中考試化學試卷(解析版) 題型:選擇題
鋅-空氣電池(原理如圖)適宜用作城市電動車的動力電源。該電池放電時Zn轉化為ZnO轉化為ZnO。該電池工作時下列說法正確的是

A. 氧氣在石墨電極上發生氧化反應
B. 該電池的負極反應為Zn+H2O-2e-=ZnO+2H+
C. 電子由鋅電極經電解質溶液流向石墨電極
D. 電池工作時鋅電極不斷被消耗
查看答案和解析>>
科目:高中化學 來源:2016-2017學年江蘇省高一下學期期中考試化學試卷(解析版) 題型:選擇題
下列關于堿金屬性質的比較,不正確的是
A. 它們的原子核外電子層數隨核電荷數的增多而增加
B. 核電荷數大的可將核電荷數小的從其氫化物的水溶液中置換出來
C. 與鹽酸的反應隨核電荷數的增加而越來越劇烈
D. 熔、沸點隨核電荷數的增加而降低
查看答案和解析>>
科目:高中化學 來源:2017屆江蘇省南通市高三高考全真模擬(一)化學試卷(解析版) 題型:填空題
(1)本生(Bunsen)熱化學循環吸收SO2工藝由下列三個反應組成:
2H2(g)+O2(g)=2H2O(l) △H1=-572kJ·mol-1
2HI(g)=H2(g)+I2(g) △H2=+10kJ·mol-1
2H2SO4(l)=2SO2(g)+2H2O(l)+O2(g) △H3=+462kJ·mol-1
則得
SO2(g)+I2(g)+2H2O(I)=2HI (g)+H2SO4(I) △H=_______ kJ·mol-1
(2)氧化鋅吸收法。配制ZnO懸濁液,在吸收塔中封閉循環脫硫。測得pH、吸收效率η隨時間t的變化如圖1所示;溶液中部分微粒與PH的關系如圖2所示。
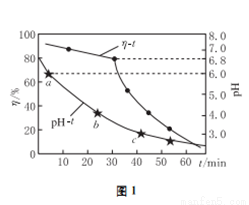
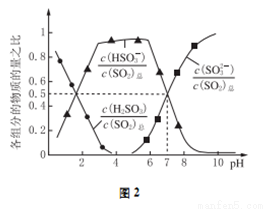
①為提高SO2的吸收效率η,可采取的措施有:增大懸濁液中ZnO的量、________________。
②圖1中的pH-t曲線ab段發生的主要化學方程式為___________________
③pH=7時,溶液中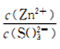 =________
=________
(3)如圖3所示,利用惰性電解電解含SO2的煙氣回收S及H2SO4,以實現廢物利用。
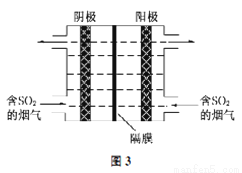
①陰極的電極反應式為_____________。
②每處理含19.2g SO2的煙氣,理論上回收S、H2SO4的物質的量分別為______、________。
查看答案和解析>>
科目:高中化學 來源:2017屆江蘇省南通市高三高考全真模擬(一)化學試卷(解析版) 題型:選擇題
右圖為1 mol SO2Cl2(g)和1 mol SCl2(g)反應生成SOCl2(g)的能量變化的示意圖,已知E1=xKJ/mol、E2=yKJ/mol,下列有關說法正確的是

A. 若在反應體系中加人催化劑,E1不變
B. 若在反應體系中加人催化劑, ΔH減小
C. 該反應的活化能等于ykJ/mol
D. 1 mol SO2Cl2 (g)和1mol SCl2(g)反應生成SOCl2(g)的ΔH=(x-y)kJ/mol
查看答案和解析>>
科目:高中化學 來源:2017屆北京市朝陽區高三第一次(3月)綜合練習理綜化學試卷(解析版) 題型:實驗題
某學生探究如下實驗(A):
實驗A | 條件 | 現象 |
| 加熱 | i.加熱后藍色褪去 ii.冷卻過程中,溶液恢復藍色 ⅲ.一段時間后,藍色重又褪去 |
(1)使淀粉變藍的物質是____。
(2)分析現象i、ii認為:在酸性條件下,加熱促進淀粉水解,冷卻后平衡逆向移動。
設計實驗如下,“現象a”證實該分析不合理:
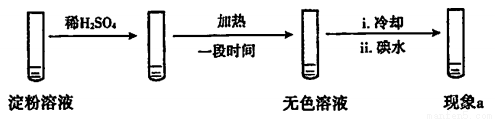
“現象a”是____。
(3)再次分析:加熱后單質碘發生了變化,實驗如下:
I:取少量碘水,加熱至褪色,用淀粉溶液檢驗揮發出的物質,變藍。
Ⅱ:向褪色后的溶液中滴加淀粉溶液,冷卻過程中一直未變藍;加入稀H2SO4,瞬間變藍。
對步驟Ⅱ中稀H2SO4的作用,結合離子方程式,提出一種合理的解釋:______________。
(4)探究碘水褪色后溶液的成分:
實驗1:測得溶液的pH≈5
實驗2:取褪色后的溶液,完成如下實驗:
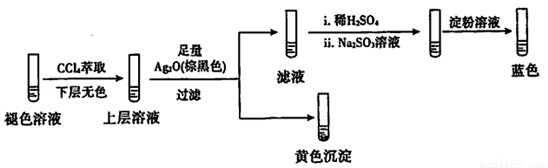
①產生黃色沉淀的離子方程式是____。
②Ag2O的作用是____________。
③依據上述實驗,推測濾液中含有的物質(或離子)可能是_________。
(5)結合化學反應速率解釋實驗A中現象i、現象iii藍色褪去的原因:_______________。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河南省南陽市高一下學期第一次月考(3月)化學試卷(解析版) 題型:選擇題
200 mL 1 mol/L的氯化鋁溶液中加入一定體積的2 mol/L的NaOH溶液,最終產生7.8 g沉淀,則加入的NaOH溶液的體積可能是( )
① 350 mL ② 90 mL ③ 150 mL ④200 mL
A. 只有① B. ①③ C. ②④ D. ②③
查看答案和解析>>
科目:高中化學 來源:四川省成都市北湖校區2016-2017學年高一3月月考化學試卷 題型:選擇題
元素周期表揭示了不同元素之間的內在聯系,是化學發展史上重要的里程碑。下列關于元素周期表的敘述中,正確的是( )
A. 元素周期表中每一橫行為一周期,每一縱列為一族
B. 原予最外層電子數相同的元素一定位于元素周期表中的同一主族
C. 在元素周期表的過渡元素區域中尋找制備耐高溫材料的元素
D. 第二周期元素的最高價態都等于其原子最外層電子數
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com