
| A. | 氯化氫與氫氧化鈉反應的中和熱△H=-57.3kJ/mol,則硫酸和氫氧化鋇反應的△H=-2×(-57.3)kJ/mol | |
| B. | CO(g)的燃燒熱是283.0KJ/mol,則表示一氧化碳的燃燒熱的熱化學方程式為CO(g)+1/2O2(g)=CO2(g)△H=-283.0kJ/mol | |
| C. | 需要加熱的反應一定是吸熱反應,常溫下能發生的反應一定是放熱反應 | |
| D. | 已知: Ⅰ:對于反應:H2(g)+Cl2(g)=2HCl(g)△H=-a kJ/mol Ⅱ:  且a、b、c均大于零,則斷開1摩爾H-Cl鍵所需的能量為(-a-b-c) kJ/mol 且a、b、c均大于零,則斷開1摩爾H-Cl鍵所需的能量為(-a-b-c) kJ/mol |
分析 A.硫酸和氫氧化鋇反應生成硫酸鋇沉淀的過程放熱;
B.燃燒熱是1mol可燃物完全燃燒生成穩定氧化物放出的熱量;
C.有些放熱反應也需要引發條件才能進行,吸熱反應常溫下也可以反應;
D.反應焓變=反應物鍵能總和-生成物鍵能總和計算.
解答 解:A.氯化氫與氫氧化鈉反應的中和熱△H=-57.3kJ/mol,硫酸和氫氧化鋇反應生成硫酸鋇沉淀,沉淀過程為放熱過程,焓變為負值,所以反應的△H<-2×(-57.3)kJ/mol,故A錯誤;
B.CO(g)的燃燒熱是283.0KJ/mol,則表示一氧化碳的燃燒熱的熱化學方程式為CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-283.0kJ/mol,故B正確;
C.有些放熱反應也需要引發條件才能進行,如氧氣和氫氣點燃才發生反應,吸熱反應常溫下也可以反應,如氯化銨和氫氧化鋇晶體混合常溫下反應,故C錯誤;
D.對于反應:H2(g)+Cl2(g)=2HCl(g)△H=-a kJ/mol,△H=-a kJ/mol=bKJ/mol+cKJ/mol-2H-Cl,得到斷開1摩爾H-Cl鍵所需的能量=$\frac{1}{2}$(a+b+c)KJ,故D錯誤;
故選B.
點評 本題從中和熱、燃燒熱和反應熱數值的計算角度對化學反應與能量進行了考查,主要是鍵能計算焓變的方法,注意把握中和熱和燃燒熱的定義要點,難度中等.


 每日10分鐘口算心算速算天天練系列答案
每日10分鐘口算心算速算天天練系列答案科目:高中化學 來源: 題型:選擇題
| A. | 除去氯化鈉溶液中的泥沙--蒸發結晶 | |
| B. | 分離水和乙醇--蒸餾 | |
| C. | 用四氯化碳提取溴水中的溴單質--萃取 | |
| D. | 分離汽油和水--分液 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用藍色石蕊試紙檢驗溶液的酸性 | |
| B. | 量筒可用于配制溶液,但不能作為反應容器使用 | |
| C. | 配制稀硫酸時,先向燒杯中注入濃硫酸,再加水稀釋 | |
| D. | 向燃著的酒精燈中加酒精 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 二氧化硅能與水反應 | |
| B. | 用二氧化硅制取單質硅,當生成2.24 L(標準狀況下)氣體時,得到2.8g硅 | |
| C. | 二氧化硅屬于傳統的無機非金屬材料 | |
| D. | 二氧化硅不能與碳酸鈉溶液發生反應,但在高溫下能與碳酸鈉固體發生反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在船舶的外殼裝上銅塊可防止其發生電化學腐蝕 | |
| B. | FeCl3溶液和Fe2(SO4)3溶液加熱蒸干、灼燒都得到Fe2O3 | |
| C. | MnO2、FeCl3和CuSO4都可加快H2O2的分解速率 | |
| D. | 用惰性電極分別電解CuCl2溶液和MgCl2溶液分別得到單質Cu和Mg |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
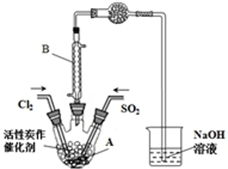 某學習小組依據反應:SO2(g)+Cl2(g)?SO2Cl2(g)△H<0,設計制備磺酰氯(SO2Cl2)的裝置如圖,有關信息如表所示.
某學習小組依據反應:SO2(g)+Cl2(g)?SO2Cl2(g)△H<0,設計制備磺酰氯(SO2Cl2)的裝置如圖,有關信息如表所示. | SO2Cl2 | Cl2 | SO2 | |
| 熔點/℃ | -54.1 | -101 | -72.4 |
| 沸點/℃ | 69.1 | -34.6 | -10 |
| 性質 | 遇水發生劇烈水解 | / | / |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | … |
| … | C2H6 | C5H12 | C8H18 | … | … | … | … |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com