
A.水解反應是典型的可逆反應,水解反應的化學平衡常數稱為水解常數(用Kh表示),Na2CO3第一步水解反應的水解常數的表示式 Kh≤ |
B.HS-電離的離子方程式:HS-+H2O H3O++S2- H3O++S2- |
C.N2(g)+3H2(g) 2NH3(g) △H<0,其他條件不變時升高溫度,反應速率V(H2)增大,氫氣的平衡轉化率變小 2NH3(g) △H<0,其他條件不變時升高溫度,反應速率V(H2)增大,氫氣的平衡轉化率變小 |
| D.CO(g)的燃燒熱是283.0 kJ·mol-1,則表示CO(g)的燃燒熱的熱化學方程式為: |
 O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1 HCO3-+OH-可知,第一步水解常數Kh=
HCO3-+OH-可知,第一步水解常數Kh= ,A不正確;B、氫硫酸是二元弱酸,則HS-電離的離子方程式為HS-+H2O
,A不正確;B、氫硫酸是二元弱酸,則HS-電離的離子方程式為HS-+H2O H3O++S2-,B正確;C、合成氨反應是體積減小的放熱的可逆反應,所以其他條件不變時升高溫度,反應速率V(H2)增大,平衡向逆反應方向移動,則氫氣的平衡轉化率變小,C正確;D、燃燒熱是在一定條件下,1mol可燃物完全燃燒生成穩定的氧化物時所放出的熱量,則根據CO(g)的燃燒熱是283.0 kJ·mol-1可知,表示CO(g)的燃燒熱的熱化學方程式為:CO(g)+
H3O++S2-,B正確;C、合成氨反應是體積減小的放熱的可逆反應,所以其他條件不變時升高溫度,反應速率V(H2)增大,平衡向逆反應方向移動,則氫氣的平衡轉化率變小,C正確;D、燃燒熱是在一定條件下,1mol可燃物完全燃燒生成穩定的氧化物時所放出的熱量,則根據CO(g)的燃燒熱是283.0 kJ·mol-1可知,表示CO(g)的燃燒熱的熱化學方程式為:CO(g)+ O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1,D正確,答案選A。
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1,D正確,答案選A。

科目:高中化學 來源:不詳 題型:實驗題
查看答案和解析>>
科目:高中化學 來源:不詳 題型:問答題
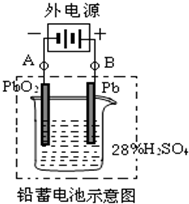
| 放電 |
| 充電 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
A.汽車尾氣的凈化反應2NO+2CO 2CO2+N2△H<0,則該反應一定能自發進行 2CO2+N2△H<0,則該反應一定能自發進行 |
| B.電解精煉銅時,陽極泥中含有Zn、Fe、Ag、Au等金屬 |
| C.由于Ksp(BaSO4)<Ksp(BaCO3),因此不可能使BaSO4沉淀轉化為BaCO3沉淀 |
D.對N2(g)+3H2(g) 2NH3(g),其他條件不變時充入N2,正逆反應速率均增大 2NH3(g),其他條件不變時充入N2,正逆反應速率均增大 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
A.對于反應2SO2(g)+O2(g)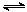 2SO3(g),壓縮氣體體積使壓強增大(其他條件不變),則SO2的轉化率增大,平衡常數K也增大 2SO3(g),壓縮氣體體積使壓強增大(其他條件不變),則SO2的轉化率增大,平衡常數K也增大 |
| B.電解法精煉銅時,精銅作陽極,粗銅作陰極 |
| C.在硫酸鋇懸濁液中加入足量飽和Na2CO3溶液處理,向所得沉淀中加入鹽酸有氣體產生,說明Ksp(BaSO4)>Ksp(BaCO3) |
D.CH3COOH溶液加水稀釋后,電離程度增大,溶液中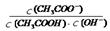 的值不變 的值不變 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.原子的核外電子排布----元素的金屬性強弱 |
| B.化合物的內在結構----電解質的相對強弱 |
| C.反應溫度的高低----化學平衡的移動程度 |
| D.反應物的化學性質----化學反應速率的快慢 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.合成氨生產過程中將NH3液化分離,可加快正反應速率,提高N2、H2的轉化率 |
| B.含1 mol Ba(OH)2的稀溶液和含1 mol H2SO4的稀溶液反應釋放熱量akJ,則表示該反應中和熱的熱化學反應方程式為: OH-(aq)+H+(aq)=H2O(l) ?H =" -a" kJ·mol-1 |
| C.電解精煉銅時,同一時間內陽極溶解銅的質量比陰極析出銅的質量小 |
D.對于2HI(g)  H2(g)+I2(g)平衡體系,增大平衡體系的壓強可使顏色變深,符合勒夏特列原理解釋。 H2(g)+I2(g)平衡體系,增大平衡體系的壓強可使顏色變深,符合勒夏特列原理解釋。 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
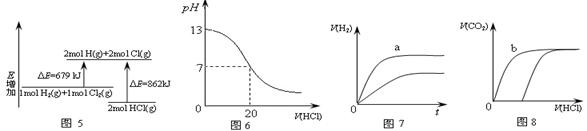
| A.圖5表示化學反應H2(g)+Cl2(g)=2HCl(g)的能量變化,則該反應的反應熱△H =183kJ·mol-1 |
| B.圖6表示室溫時用0.1mol·L-1鹽酸滴定20mL0.1mol·L-1NaOH溶液,溶液pH隨加入酸體積變化 |
| C.圖7表示體積和pH均相同的HCl和CH3COOH兩種溶液中,分別加入足量的鋅,產生H2的體積隨時間的變化,則a表示CH3COOH溶液 |
| D.圖8表示10mL0.1mol/LNa2CO3和NaHCO3兩種溶液中,分別滴加0.1mol/LHCl,產生CO2的體積隨鹽酸體積的變化,則b表示Na2CO3溶液 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com