
| A. | 6 | B. | 5 | C. | 4 | D. | 3 |
分析 強弱電解質的根本區別是電離程度,部分電離的電解質是弱電解質,要證明醋酸是弱電解質,只要證明醋酸部分電離即可,可以根據醋酸鈉溶液酸堿性、一定濃度的醋酸pH等方法判斷,據此分析解答.
解答 解:①常溫下某CH3COONa溶液的pH=8,說明醋酸鈉是強堿弱酸鹽,則醋酸為弱酸,故①正確;
②用CH3COOH溶液做導電實驗,燈泡很暗,說明醋酸溶液中離子濃度較小,不能說明醋酸部分電離,所以不能證明醋酸是弱電解質,故②錯誤;
③等pH等體積的鹽酸、CH3COOH溶液和足量鋅反應,CH3COOH放出的氫氣較多,說明醋酸中存在電離平衡,則醋酸部分電離為弱電解質,故③正確;
④0.1mol/L的CH3COOH溶液的pH=2.1,說明醋酸部分電離,為弱電解質,故④正確;
⑤CH3COONa和稀H3PO4反應生成CH3COOH,證明醋酸的酸性小于磷酸,而磷酸為弱電解質,則醋酸為弱電解質,故⑤正確;
⑥pH=1的CH3COOH溶液稀釋100倍,pH<3,說明醋酸中存在電離平衡,為弱電解質,故⑥正確;
根據分析可知,能夠證明醋酸為弱電解質的有5個,
故選B.
點評 本題考查強弱電解質判斷,為高頻考點,題目難度中等,明確強弱電解質根本區別是解本題關鍵,注意不能根據電解質溶液導電性強弱、電解質溶解性強弱等方法判斷,為易錯題.


科目:高中化學 來源: 題型:解答題

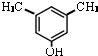 或
或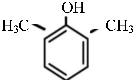 .
.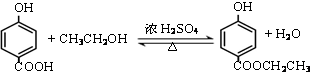 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在氧化還原反應中,非金屬單質一定是氧化劑 | |
| B. | 某元素從化合態變為游離態時,該元素一定被還原 | |
| C. | 金屬陽離子被還原不一定得到金屬單質 | |
| D. | 氧化還原反應中所有元素的化合價都發生變化 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
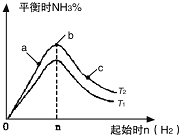 利用N2和H2可以實現NH3的工業合成,而氨又可以進一步制備硝酸.
利用N2和H2可以實現NH3的工業合成,而氨又可以進一步制備硝酸.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
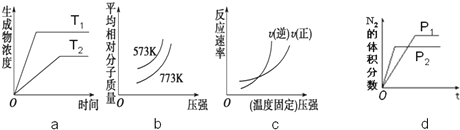
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
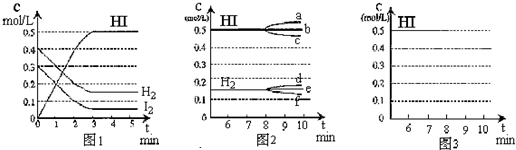
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 少量CO2通入漂白液中:CO2+ClO-+H2O═HClO+HCO3- | |
| B. | 向含K+、CO32-、OH-的溶液中通入少量CO2:2OH-+CO2═CO32-+H2O | |
| C. | 強堿溶液中NaClO與Fe(OH)3反應生成Na2FeO4:3ClO-+Fe(OH)3═FeO42-+3Cl-+H2O+4H+ | |
| D. | 3molCl2通入含4molFeI2的溶液中充分反應:2I-+Cl2═I2+2Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
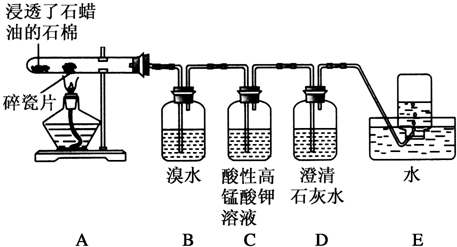
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 膠體能發生電泳現象 | B. | 膠體能產生丁達爾現象 | ||
| C. | 膠體粒子直徑在1~100nm之間 | D. | 膠體在一定條件下能聚沉 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com