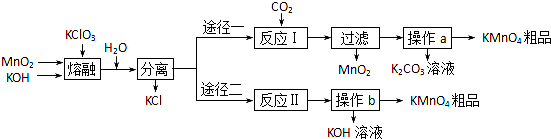
(2010?泰州三模)某化學研究性學習小組通過查閱資料,設計了如圖所示的方法來制備KMnO
4.
已知:①3MnO
2+KClO
3+6KOH
3K
2MnO
4+KCl+3H
2O
②幾種物質的溶解度:
| 溫度 |
溶解度/g |
| K2CO3 |
KOH |
KMnO4 |
| 20℃ |
111 |
112 |
6.38 |
| 60℃ |
127 |
154 |
22.1 |
請回答下列問題:
(1)第一步固體熔融時除三腳架、泥三角、細鐵棒、坩堝鉗外,還需下列儀器中的
CD
CD
.
A.蒸發皿 B.燒杯 C.酒精燈 D.鐵坩堝
(2)反應Ⅰ中氧化產物與還原產物的物質的量之比為
2:1
2:1
;該反應中可以循環利用的產物是
MnO2
MnO2
.
(3)反應Ⅱ的條件為電解,寫出反應Ⅱ的化學方程式
2K
2MnO
4+2H
2O
2KOH+2KMnO
4+H
2↑
2K
2MnO
4+2H
2O
2KOH+2KMnO
4+H
2↑
.
(4)途徑一、二中的操作a、b相同,均包括
蒸發濃縮、降溫結晶
蒸發濃縮、降溫結晶
、過濾等3步.
(5)通過用草酸滴定KMnO
4溶液的方法可測定KMnO
4粗品的純度(質量分數).
①實驗時要將草酸晶體(H
2C
2O
4?2H
2O)配成標準溶液,則配制100mL1.5mol?L
-1的草酸溶液,需要稱取草酸晶體的質量為
18.9g
18.9g
.
②該實驗中除草酸晶體的質量外,還需要采集的數據有
滴定時消耗草酸溶液的體積、KMnO4粗品的質量
滴定時消耗草酸溶液的體積、KMnO4粗品的質量
.



