
在一定溫度下,容器內某一反應中M、N的物質的量隨反應時間變化的曲線如圖所示,下列表述中正確的是
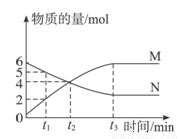
A.反應的化學方程式為N 2M
2M
B.t1時,正、逆反應速率相等,達平衡
C.t3時,正反應速率大于逆反應速率
D.t1時,N的濃度是M濃度的2倍
 孟建平錯題本系列答案
孟建平錯題本系列答案 超能學典應用題題卡系列答案
超能學典應用題題卡系列答案科目:高中化學 來源:2015-2016學年山西大學附中高一下期中化學試卷(解析版) 題型:填空題
有A、B、C、D、E 5種短周期元素,A與B可形成BA型化合物,A元素的單質常用于自來水消毒;金屬B的原子核內質子數比它前一周期同主族元素原子的質子數多8;C元素有3種同位素C1、C2、C3,自然界里含量最多的是C1,C3原子的質量數是C1的3倍,C2原子的質量數是C1的2倍;D的氣態氫化物的水溶液呈堿性,而其最高價氧化物對應的水化物為強酸;E元素原子的最外層電子數比次外層電子數多4。
(1)寫出下列元素的元素名稱:A________, B________。
(2)寫出C1、C3兩種原子的符號:C1________, C3________。
(3) A、B、E形成的一種化合物是某種家用消毒液的有效成分,其電子式是 。
(4)D的最高價氧化物的水化物與其氫化物反應形成化合物的化學式是____________,其所含化學鍵的類型是 。由最常見的E原子與C2原子形成的最簡單分子0.5mol中,所含中子的數目是________。
(5) C、E的單質在堿性(KOH溶液)條件下可設計成一種燃料電池,其電極反應式為(負極) (正極) 。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年青海師大附二中高一下期中化學試卷(解析版) 題型:選擇題
①②③④四種金屬片兩兩相連浸入稀硫酸中都可組成原電池,當①②相連時,外電路電流從②流向①;當①③相連時,溶液中的H+向③移動;當②④相連時,②上有氣泡逸出;當③④相連時,③的質量減少。據此判斷這四種金屬活動性由大到小的順序是( )
A.①③②④ B.③④②① C.①③④② D.③①②④
查看答案和解析>>
科目:高中化學 來源:2015-2016學年青海師大附二中高二下期中化學試卷(解析版) 題型:選擇題
下列說法正確的是
A.室溫下,在水中的溶解度:丙三醇>苯酚>1-氯丁烷
B.用核磁共振氫譜不能區分HCOOCH3和HCOOCH2CH3
C.用Na2CO3溶液不能區分CH3COOH和CH3COOCH2CH3
D.油脂在酸性或堿性條件下均能發生水解反應,且產物相同
查看答案和解析>>
科目:高中化學 來源:2015-2016學年江蘇省高一下期中化學試卷(解析版) 題型:填空題
將4molA氣體和2molB氣體在2L的密閉容器中混合,在一定條件下發生如下反應:2A(g)+B(g) 2C(g)若經過2秒后測得C的濃度為0.6mol/L。
2C(g)若經過2秒后測得C的濃度為0.6mol/L。
則:(1)2s內用B表示的反應速率 。
(2)2s時A的物質的量濃度為 。
(3)2s時B的物質的量為 。
(4)最終C的濃度 (填“能”或“不能”)達到2mol/L。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年江蘇省高一下期中化學試卷(解析版) 題型:選擇題
下列比較錯誤的是
A.原子半徑:N>O>F
B.酸性強弱:HNO3>H3PO4>H2SO4
C.堿性強弱:KOH >NaOH>Mg(OH)2
D.氫化物的穩定性:HF>HCl>H2S
查看答案和解析>>
科目:高中化學 來源:2015-2016學年江蘇省高一下期中化學試卷(解析版) 題型:選擇題
設 NA為阿伏加德羅常數,下列說法中錯誤的是
A. 在標準狀況下,22.4LSO3所含的硫原子數目為NA
B. 常溫常壓下,7.8g過氧化鈉含有的離子數為0.3NA
C. 18 g 水所含的電子數目為10 NA
D. 3.2g O2、O3混合物中所含氧原子一定是0.2NA
查看答案和解析>>
科目:高中化學 來源:2015-2016學年江蘇省高二下期中化學試卷(解析版) 題型:選擇題
反應3X(g)+Y(g) 2Z(g)+2W(g)在2L密閉容器中進行,5min后Y減少了0.5mol,則此反應的平均速率v為
2Z(g)+2W(g)在2L密閉容器中進行,5min后Y減少了0.5mol,則此反應的平均速率v為
A.v(X)=0.05mol·L-1·min-1 B.v(Z)= 0.10mol·L-1·min-1
C.v(Y)=0.10mol·L-1·min-1 D.v(W)=0.05mol·L-1·s-1
查看答案和解析>>
科目:高中化學 來源:2015-2016學年吉林長春外國語高一下期中文科化學試卷(解析版) 題型:選擇題
1994 年12月科學家發現了一種新元素,它的原子核內有161個中
年12月科學家發現了一種新元素,它的原子核內有161個中 子,質量數為272,該元素的核電荷數為( )
子,質量數為272,該元素的核電荷數為( )
A.111 B.272 C.161 D.433
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com