
【題目】某單質A經如下圖所示的過程,請回答下列問題:
![]()
(1)若A為淡黃色固體,B是有刺激性氣味的無色氣體。
①A、D的化學式分別為:A__________ D__________
②工業生產中大量排放的B氣體被雨水吸收后形成___________而污染環境。
③寫出B→C反應的化學方程式:__________________________________________
(2)若C為淡黃色固體。
①C的電子式為___________,C中陰陽離子數目比為_________
②寫出C→D反應的離子方程式:___________________________________________
【答案】 S H2SO4 酸雨 2SO2+O2![]() 2SO3
2SO3 ![]() 1:2 2Na2O2+2H2O=4Na++4OH-+O2↑
1:2 2Na2O2+2H2O=4Na++4OH-+O2↑
【解析】(1)若A為淡黃色固體,B是有刺激性氣味的無色氣體,則A是單質硫,B是二氧化硫,據此解答。
(2)若C為淡黃色固體,B與氧氣反應生成,因此C是過氧化鈉,據此解答。
(1)若A為淡黃色固體,B是有刺激性氣味的無色氣體,根據轉化關系圖可判斷A是S,B是SO2,C是SO3,D是H2SO4。則
①根據以上分析可知A、D的化學式分別為S、H2SO4;
②SO2溶于水生成亞硫酸,亞硫酸易被氧化為強酸硫酸從而形成酸雨而污染環境。
③B→C反應是二氧化硫的催化氧化,反應的化學方程式為2SO2+O2![]() 2SO3。
2SO3。
(2)若C為淡黃色固體,B與氧氣反應生成,因此C是過氧化鈉,所以A是鈉,B是氧化鈉,D是氫氧化鈉。則
①過氧化鈉含有離子鍵和極性鍵,電子式為![]() ,根據過氧化鈉的電子式可判斷C中陰陽離子數目比為1:2;
,根據過氧化鈉的電子式可判斷C中陰陽離子數目比為1:2;
②C→D反應是過氧化鈉與水反應生成氫氧化鈉和氧氣,反應的離子方程式為2Na2O2+2H2O=4Na++4OH-+O2↑。


 新活力總動員暑系列答案
新活力總動員暑系列答案 龍人圖書快樂假期暑假作業鄭州大學出版社系列答案
龍人圖書快樂假期暑假作業鄭州大學出版社系列答案科目:高中化學 來源: 題型:
【題目】某實驗小組設計的糖廠甘蔗渣利用方案如下圖所示:

其中:A能催熟水果,B是高分子化合物,D是有水果香味的物質。請回答以下問題:
(1)“C6H12O6” 所示物質的名稱是______; A的結構簡式為_____;C中官能團的名稱為______。
(2)寫出下列轉化的化學方程式并指出反應類型:
CH3CH2OH → CH3CHO:______, 反應類型為_______。
(3)下列說法正確的是______。
A.目前生產A的主要方法是石油的裂解,其產量是衡量一個國家化工水平的標志之一
B.分餾石油得到的各個餾分為純凈物
C.動物的脂肪在酸性條件下水解可以得到肥皂的主要成分
D.塑料、合成橡膠、合成纖維、淀粉都是高分子化合物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業上電解NO制備NH4NO3,其工作原理如圖所示(圖中電極均為石墨電極)。下列說法錯誤的是

A. a 極連接電源的負極
B. 陽極反應為NO+5e-+6H+=NH4++H2O
C. 總反應方程式為8NO+7H2O![]() 3NH4NO3+2HNO3
3NH4NO3+2HNO3
D. 為使電解產物全部轉化為NH4NO3,需補充物質A,A 是NH3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】H2X為二元弱酸,常溫下,將NaOH溶液加入到H2X溶液中,在不同pH環境下,不同形態的粒子(酸、酸式酸根、酸根離子)的組成分數如圖所示。下列說法正確的是

A. HX-的電離程度小于水解程度
B. 在pH=7的溶液中HX-和X2-能大量共存
C. 在pH=9時,H2X 與NaOH恰好完全中和
D. 1L.0.1 molL-1Na2X溶液中,n(HX-)+2n(X2-)+n(H2X)=0.1 mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】【題目】工業上用重鉻酸鈉(Na2Cr2O7)結晶后的母液(含少量雜質Fe3+)生產重鉻酸鉀 (K2Cr2O7),其工藝流程及相關物質溶解度曲線如下圖所示。
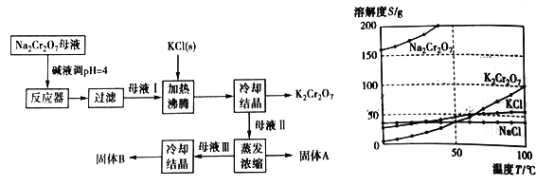
(1)向Na2Cr2O7母液中加堿液調pH的目的是_____________________。
(2)通過冷卻結晶析出大量K2Cr2O7的原因是________________________________。
(3)固體A的主要成分為__________(填化學式),用熱水洗滌固體A,回收的洗滌液轉移到母液___________(填“I”“Ⅱ”或“Ⅲ”)中,既能提高產率又可使能耗降低。固體B的主要成分為___________________(填化學式)。
(4)測定產品中K2Cr2O7含量的方法如下:稱取產品試樣2.500 g 配成250 mL溶液,用移液管取出25.00 mL于碘量瓶中,加入10 mL 2 mol·L-l H2SO4溶液和足量KI溶液(鉻的還原產物為Cr3+),放置于暗處5 min,然后加入100 mL蒸餾水、3 mL 淀粉指示劑,用0.1200 mol·L-l Na2S2O3標準溶液滴定(已知I2+ 2S2O32-=2I-+S4O62-)。
①酸性溶液中KI 與K2Cr2O7反應的離子方程式為_____________________________。
②若實驗中共用去Na2S2O3標準溶液40.00 mL,則所得產品中重鉻酸鉀的純度為__________%( 保留2 位小數,設整個過程中其他雜質不參與反應)。進一步提純產品的方法是___________________。
(5)+6價Cr的毒性很高,工業上用電解法來處理含Cr2O72-的廢水。下圖為電解裝置示意圖,電極材料分別為鐵和石墨。通電后,Cr2O72-在b極附近轉變為Cr3+,一段時間后Cr3+最終可在a 極附近變成Cr(OH)3沉淀而被除去。
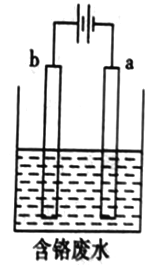
①在以上處理過程中,Cr2O72-轉化為毒性較低的Cr3+的離子方程式為________________________。
②a電極的電極反應式是是____________________;電解一段時間后在陰極區有Fe(OH)3和Gr(OH)3沉淀生成,若電解后的溶液中c(Cr3+)為3×10-5mol·L-1,則溶液中c(Fe3+)為____________ mol·L-1。已知:Ksp=[Fe(OH)3]=4.0×10-38,K[Cr(OH)3]=6.0×10-31。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】相同狀況下,1體積某氣態烴只能與1體積Cl2發生加成反應,生成氯代烷,1 mol此氯代烷可與4 mol Cl2發生完全取代反應,則該烴的結構簡式為( )
A. CH2===CH2 B. CH3CH===CH2
C. CH3CH3 D. CH2===CH—CH===CH2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃/101kPa時,1g甲醇完全燃燒生成CO2和液態H2O,同時放出22.68kJ熱量,下列表示該反應的熱化學方程式正確的是( )
A.CH4O(l)+ ![]() O2(g)=CO2(g)+2H2O(g)△H=﹣725.8kJmol﹣1
O2(g)=CO2(g)+2H2O(g)△H=﹣725.8kJmol﹣1
B.2CH4O(l)+3O2(g)=2CO2(g)+2H2O(l)△H=+1451.6kJmol﹣1
C.2CH4O(l)+3O2(g)=2CO2(g)+4H2O(l)△H=﹣22.68kJmol﹣1
D.CH4O(l)+ ![]() O2(g)=CO2(g)+2H2O(l)△H=﹣725.8kJmol﹣1
O2(g)=CO2(g)+2H2O(l)△H=﹣725.8kJmol﹣1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示,A、F為石墨電極,B、E為鐵片電極.按要求回答下列問題. 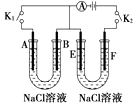
(1)打開K2 , 合并K1 . B為極,A的電極反應為 .
(2)打開K1 , 合并K2 . E為極,F極的電極反應為 , 檢驗F極產生氣體的方法是 .
(3)若往U型管中滴加酚酞,進行(1)(2)操作時,A、B、E、F電極周圍能變紅的是 , 原因是 .
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com