
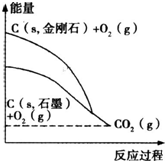
 根據右圖所示的各物質能量變化關系,判斷下列熱化學方程式正確的是( )
根據右圖所示的各物質能量變化關系,判斷下列熱化學方程式正確的是( )| A、C(金剛石,s)+O2(g)=CO2(g)△H1=a kJ?mol-1 (a<0) | B、C(石墨,s)+O2(g)=CO2(g);△H2=b kJ?mol-1 (b>0) | C、C+O2=CO2(g)△H3=c kJ?mol-1 (c<0) | D、C(s,金剛石)=C(s,石墨)△H4=d kJ?mol-1 (d>0) |


 黃岡經典趣味課堂系列答案
黃岡經典趣味課堂系列答案 啟東小題作業本系列答案
啟東小題作業本系列答案科目:高中化學 來源: 題型:
 (2011?焦作一模)化學-選修物質結構與性質:
(2011?焦作一模)化學-選修物質結構與性質:查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
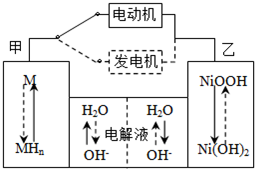
| 放電 | 充電 |
查看答案和解析>>
科目:高中化學 來源:2011-2012學年河南省平頂山市高二下學期期末考試理科綜合化學試卷(帶解析) 題型:填空題
[化學——選修物質結構與性質](30分)
Ⅰ.(18分)請選出下列各題中符合題意的選項:
(1)下列物質中,屬于含有共價鍵的離子晶體是
A.CsCl B.KOH C.H2O D.H2
(2)已知CsCl晶體的密度為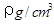 ,NA為阿伏加德羅常數,相鄰的兩個Cs+的核間距為a cm,如圖所示,則CsCl的摩爾質量可以表示為
,NA為阿伏加德羅常數,相鄰的兩個Cs+的核間距為a cm,如圖所示,則CsCl的摩爾質量可以表示為 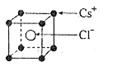
A.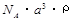 g/mol B.
g/mol B.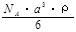 g/mol
g/mol
C.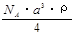 g/mol D.
g/mol D. g/mol
g/mol
(3)已知含氧酸可用通式XOm(OH)n來表示,如X是S,m=2,n=2,則這個式子就表示H2SO4。一般而言,該式中m的值越大,該含氧酸的酸性越強。下列各含氧酸中酸性最強的是
A.HMnO4 B.H2SeO3 C.H3BO3 D.H3PO4
Ⅱ.(12分)現有部分前四周期元素的性質或原子結構如下表:
| 元素編號 | 元素性質或原子結構 |
| A | 原子的電子排布圖為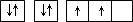 |
| B | 常溫下單質為雙原子分子,原子間形成三對共用電子對 |
| C | 原子的s軌道電子數等于p軌道電子數,元素的最低負價為-2價 |
| D | 二價陽離子與C的陰離子具有相同的電子層結構 |
| E | 原子序數是D兩倍, |

查看答案和解析>>
科目:高中化學 來源:2010年北京市高三上學期起點考試化學試題 題型:填空題
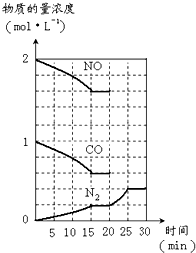
(10分)25°C時,在體積為2L的密閉容器中,氣態物質A、B、C的物質的量n(m ol)隨時間t的變化如右圖所示,已知達平衡后,降低溫度,A的轉化率將增大。
ol)隨時間t的變化如右圖所示,已知達平衡后,降低溫度,A的轉化率將增大。
(1)根據上圖數據,寫出該反應的化學方程式: ;此反應的平衡常數表達式K= ,從反應開始到達第一次平衡時的平均速率v(A)為 。
(2)在5—7min內,若K值不變,則此處曲線變化的原因是
(3)下圖表示此反應的反應速率v和時間t的關系圖: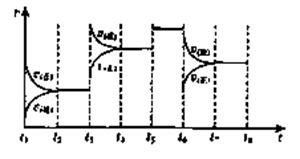
各階段的平衡常數如下表所示:
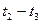 | 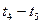 |  |  |
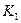 |  | 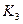 | 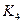 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com