
【題目】500 多年前,一艘載著天然蘇打晶體(Na2CO3·10H2O)的商船在航行中擱淺,船員們便在附近的沙灘上用幾塊蘇打晶體支鍋煮飯。之后他們驚奇地發現,在蘇打與沙粒接觸的地方出現了許多晶瑩發亮的珠子。回答下列問題:
(1)沙灘上沙粒的主要成分為_______(填化學式)。
(2)上述晶瑩發亮的珠子可能是______(填字母)。
A. 水晶顆粒 B.無水碳酸鈉 C.晶體硅 D.玻璃珠
(3)生成該珠子時發生反應的化學方程式為_____________。
(4)氫氟酸常用作玻璃的蝕刻劑,原因是______________(用化學方程式表示)。
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】下列說法正確的是(NA表示阿伏加德羅常數的量)( )
A. 在常溫常壓下, ![]() 氧氣和臭氧組成的混合氣體中所含氧原子數目為NA
氧氣和臭氧組成的混合氣體中所含氧原子數目為NA
B. 1mol![]() (碳正離子)中含電子數目為10NA
(碳正離子)中含電子數目為10NA
C. 標準狀況下,22.4LSO3中含有的氧原子數為3NA
D. 200mL 0.5mol/L硝酸銨溶液中含有![]() 0.1NA
0.1NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關能源與能量的說法正確的是( )
A.煤和石油是經過億萬年形成的,億萬年后煤和石油還會生成,故二者屬可再生能源
B.蒸汽屬于一次能源
C.凡經過加熱而發生的反應都是吸熱反應,常溫下進行的反應都是放熱反應
D.反應物和生成物的總能量決定反應是放熱還是吸熱
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】“千年大計、國家大事”,雄安新區無疑是今年最受矚目的地區。不過,近日媒體報道河北廊坊、天津等地存在超大規模的工業污水滲坑,給雄安新區的水環境帶來隱患,目前正采用多種方法對污水進行處理,改善水資源狀況。
(1)在微生物作用的條件下,廢水中的NH4+經過兩步反應氧化成NO3-,兩步反應的能量變化示意圖如下:
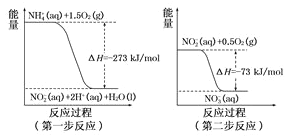
①第一步反應是______反應(選填“放熱”或“吸熱”),判新依據是_________。1mol NH4+ (aq)全部氧化成NO3- (aq)的熱化學方程式為_____________。
②一定條件下,向廢水中加入CH3OH,將HNO3還原成N2。若該過程中CH3OH反應生成CO2,則參加反應的還原劑和氧化劑的物質的量之比為______.
(2)二氧化氯(ClO2)是一種黃綠色到橙黃色的氣體,是國際上公認為安全、無毒的綠色消毒劑,可以投入廢水中清除污染物。
①二氧化氯可以將廢水中的氰化物(CN-)氧化成兩種無污染氣體.寫出離子方程式________。
②廢水中的重金屬離子的危害性很大,二氧化氯能夠在弱酸性溶液中把二價錳離子氧化成不溶于水的二氧化錳(MnO2),寫出反應的離子方程式_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用NA表示阿伏加德羅常數的值,下列敘述正確的是( )
A.0.1molCl2常溫下與過量稀NaOH溶液反應轉移電子總數為0.1NA
B.25℃時,pH=13的1.0L Ba(OH)2溶液中含有的OH﹣數目為0.2NA
C.標準狀況下,22.4LCHCl3含有的分子數為NA
D.1L 0.1molL﹣1的硫化鈉溶液中硫離子數目為0.1NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】黃鉀銨鐵礬[KNH4Fex(SO4)y(OH)z] 不溶于水和稀硫酸,制取流程如下:

請回答下列問題:
(1)溶液X是_______。
(2)在黃鉀銨鐵礬[KNH4Fex(SO4)y(OH)z] 中,x、y、z的代數關系式為_______。
(3)檢驗濾液中是否存 在K+的操作是_______。
(4)黃鉀銨鐵礬的化學式可通過下列實驗測定:
步驟1: 稱取一定質量的樣品加入稀硝酸充分溶解,將所得溶液轉移至容量瓶配制成100.00mL 溶液A。
步驟2: 最取25.00mL溶液A,加入鹽酸酸化的BaCl2溶液至沉淀完全,過濾、洗滌、干燥至恒重,得到白色固體9.32g。
步驟3: 量取25.00mL溶液A,加入足最NaOH溶液,加熱,收集到標準狀下氣體224mL,同時有紅褐色沉淀生成。
步驟4: 將步驟3所得沉淀過濾、洗滌、灼燒,最終得固體4.80g。
①步驟1配制溶液A所需的玻璃儀器除燒杯、玻璃棒、膠頭滴管外,還需_______。
②根據以上實驗數據計算黃鉀銨鐵礬中的n(OH-)∶n(SO42-)的比值為_______。(寫出必要的計算過程,否則不得分)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業上常以烴的含氧衍生物X為主要原料生產可降解塑料PCL{![]() }及阻燃劑四溴雙酚A.合成線路如下:
}及阻燃劑四溴雙酚A.合成線路如下:
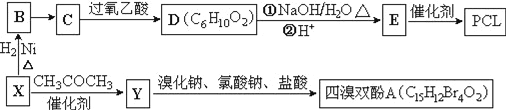
已知:①X的蒸汽密度是相同條件下H2的47倍,遇FeCl3溶液顯紫色;C為![]() 。
。
②![]() 。
。
③RCOCH2R′![]() RCOOCH2R′。
RCOOCH2R′。
(1)B的名稱是_________________。
(2)B→C還需要的反應試劑及條件是___________。C→D的反應類型是______________________。
(3)寫出X→Y的化學方程式:_______________________________。
(4)0.5mol四溴雙酚A在一定條件下與足量的NaOH溶液反應,最多消耗__molNaOH。
(5)符合以下條件的D的同分異構體有__種(不考慮空間異構)。
①含有兩個甲基和兩種官能團 ②能使溴的CCl4溶液褪色 ③能發生銀鏡反應
(6)已知由烯烴直接制備不飽和酯的新方法為:
![]()
利用乙烯為有機原料(無機物和反應條件自選)合成聚合物涂料![]() ,寫出合成該涂料的反應流程圖:________________________________。
,寫出合成該涂料的反應流程圖:________________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com