
【題目】下列關于原電池的說法正確的是( )
A.在正極上發生氧化反應
B.化學性質較活潑的金屬為負極
C.在外電路,電子流出正極
D.是由電能轉化為化學能的裝置
科目:高中化學 來源: 題型:
【題目】常見物質A~K之間存在如下圖所示的轉化關系,其中D、E為單質,請回答下列問題(圖中有些反應的產物和反應的條件沒有全部標出)。
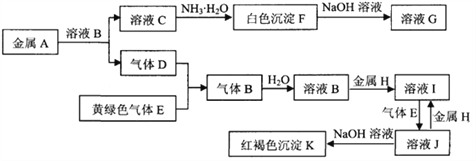
(1)寫出下列物質中溶質的名稱:B是 __________,G是____________
(2)反應“F→G”的化學方程式是_____________________________________________
(3)反應“J→I”的離子方程式是_____________________________________________
(4)溶液I中混有溶液J,除去J的方法是:________________________________________________________________
(5)檢驗溶液I中陽離子的方法是:__________________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】水的離子積常數KW與溫度t(℃)的關系如圖所示: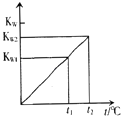
(1)若t1=25℃,則KW1=;若t2=100℃時,KW2=10﹣12 , 則0.05molL﹣1的Ba(OH)2溶液的pH= .
(2)已知25℃時,0.1L0.1molL﹣1的NaA溶液的pH=10,則NaA溶液中所存在的化學平衡有(用離子方程式表示): . 溶液中各離子的物質的量濃度由大到小的順序為 .
(3)25℃時,將pH=11的NaOH溶液與pH=4的硫酸溶液混合,若所得混合溶液pH=9,則NaOH溶液與硫酸溶液的體積比為 .
(4)100℃時,若10體積的某強酸溶液與1體積的某強堿溶液混合后溶液呈中性,則混合之前,該強酸的pH(pH酸)與強堿的pH(pH堿)之間應滿足的關系為:pH(酸)+pH(堿)= .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列物質的分離或提純,可選用蒸餾法的是
A. 除去石灰水中懸浮的碳酸鈣顆粒
B. 除去氯化鈉晶體中混有的碘單質
C. 分離汽油和煤油的混合物
D. 分離水和苯的混合物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某研究性學習小組設計了一組實驗,驗證元素周期律.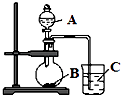
(1)甲同學在a、b、c、d四只燒杯里分別加入50mL冷水,再分別滴加幾滴酚酞溶液,依次加入大小相近的鈉(Na)、鎂(Mg)、鋁(Al)、鉀(K)金屬塊,觀察現象.①甲同學設計實驗的目的是驗證:同一主族,從上到下元素的元素金屬性逐漸增強;同一周期,從左到右,元素金屬性;
②反應最劇烈的燒杯里金屬是(填字母)
A、鈉 B、鎂 C、鋁 D、鉀;
③寫出a燒杯里發生反應的離子方程式 .
④實驗中發現b、c兩只燒杯中幾乎沒有什么現象,要想達到實驗的目的,請你幫助選擇下列合適的方法 .
A.把鎂、鋁的金屬塊換成金屬粉末
B.把燒杯中的冷水換成熱水
C.把燒杯中的冷水換成鹽酸
D.把燒杯中的冷水換成氫氧化鈉溶液
(2)乙同學設計實驗驗證:非金屬元素的非金屬性越強,其最高價含氧酸的酸性就越強.他設計了如圖裝置以驗證碳、氮、硅元素的非金屬性強弱.乙同學設計的實驗可直接證明三種酸的酸性強弱,已知A是強酸,其濃溶液在常溫下可與銅反應;B是塊狀固體;燒杯中盛放C的水溶液,打開分液漏斗的活塞后,C中可觀察到白色膠狀沉淀生成.①寫出所選用物質的化學式:A、; C、 .
②寫出燒瓶中發生反應的化學方程式: .
③碳、氮、硅三種元素的非金屬性由強到弱順序為 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據相應的圖象(圖象編號與答案一一對應),判斷下列相關說法正確的是( ) 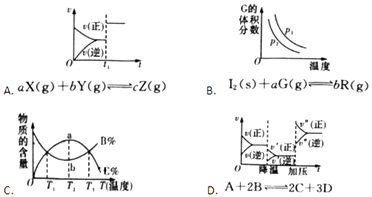
A.t1時改變某一條件有如圖所示變化,則改變的條件一定是加入催化劑
B.反應達到平衡時,外界條件對平衡影響關系如圖所示,若b=1,a為正整數,則P1<P2
C.從加入反應物開始,物質的百分含量與溫度關系如圖所示,則該反應的正反應為吸熱反應
D.反應速率和反應條件變化如圖所示,則該反應正反應為放熱反應,A,B一定是氣體,D一定不是氣體,C可能不是氣體
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一水合硫酸四氨合銅(Ⅱ)[Cu(NH3)4]SO4)H2O為深藍色晶體,在工業上用途廣泛,常用作殺蟲劑、媒染劑.某學習小組探究制備該晶體并測定其組成的實驗過程如下:(Ⅰ)晶體的制備原理及流程:
CuSO4+4NH3+H2O═[Cu(NH3)4]SO4)H2O
回答下列問題:
(1)無水乙醇的作用;烘干晶體的溫度性質60℃的原因是;
(2)實驗制得產物晶體中往往有Cu2(OH)2SO4雜質,分析產生該雜質的原因可能是;
(3)(Ⅱ)晶體中溶解于酸性溶液中,加入NaI溶液,Cu2+可與I作用產生I2和白色沉淀,該反應的離子方程式為 , 再用Na2S2O3溶液滴定I2 , 即可得Cu2+含量;
(4)(Ⅲ)晶體中氮含量的測定實驗裝置如圖所示,稱取0.9380g[Cu(NH3)x]SO4H2O晶體[M=(178+17x)g/mol]于錐形瓶a中,通過分液漏斗向錐形瓶a中滴加10%NaOH溶液,用1.000mol/L的NaOH標準滴定b中剩余的HCl.
滴定管讀數如圖所示,消耗標準液mL;[Cu(NH3)x]SO4H2O中x= , 推測測量值(x)比理論值偏小的原因是;
(5)(Ⅳ)SO42﹣含量的測定﹣﹣沉淀法稱取一定質量的試樣,加稀鹽酸溶解,將BaCl2加入溶液中,靜置得到BaSO4沉淀,檢驗沉淀已完全的操作為 .
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com