
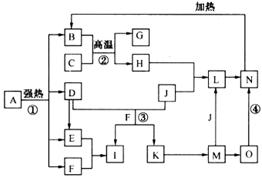
仔細閱讀下圖,已知B、D、E、F、G是氧化物,F、K是氫化物;C、H是日常生活中最為常見的金屬單質,J是氣態非金屬單質,O是白色沉淀,且B、H、L、M、N、O中含有同種元素(圖中部分反應物或產物已略去)。
請按要求回答:
(1)反應①既是分解反應,又是氧化還原反應,產物B、D、E、F的物質的量之比1:1:1:14。A強熱分解的化學反應方程式為 。
(2)寫出反應②在工業生產上的一種用途: 。
(3)反應③的離子方程式為 ;
反應④的化學方程式為 。
(4)常以C或H制成容器盛裝和運輸I的濃溶液,其原理是
。
(1)2FeSO4·7H2O![]() Fe2O3+SO2↑+SO3↑+14H2O
Fe2O3+SO2↑+SO3↑+14H2O
(2)野外焊接鋼軌
(3)Cl2+SO2+2H2O==4H++SO![]() +2Cl
+2Cl![]() 4Fe(OH)2+O2+2H2O==4Fe(OH)3
4Fe(OH)2+O2+2H2O==4Fe(OH)3
(4)冷的濃硫酸與鐵或鋁制容器接觸時,在表面生成一層致密的氧化膜,阻止金屬繼續與酸反應而使金屬“鈍化”,所以可用鐵或鋁制容器儲運濃硫酸
暫無解析(1)2FeSO4·7H2O![]() Fe2O3+SO2↑+SO3↑+14H2O
Fe2O3+SO2↑+SO3↑+14H2O
(2)野外焊接鋼軌
(3)Cl2+SO2+2H2O==4H++SO![]() +2Cl
+2Cl![]() 4Fe(OH)2+O2+2H2O==4Fe(OH)3
4Fe(OH)2+O2+2H2O==4Fe(OH)3
(4)冷的濃硫酸與鐵或鋁制容器接觸時,在表面生成一層致密的氧化膜,阻止金屬繼續與酸反應而使金屬“鈍化”,所以可用鐵或鋁制容器儲運濃硫酸


 舉一反三單元同步過關卷系列答案
舉一反三單元同步過關卷系列答案科目:高中化學 來源: 題型:閱讀理解
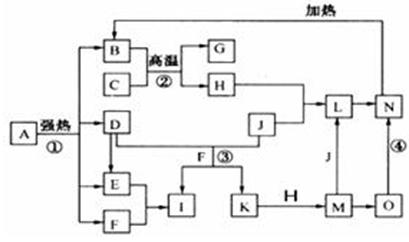
仔細閱讀下圖,已知B、D、E、F、G是氧化物,其中D是形成酸雨的主要污染物,F、K是氫化物,且F在常溫下為液態;C、H是日常生活中最為常見的金屬單質,J是氣態非金屬單質,O是白色沉淀,且B、H、L、M、N、O中含有同種元素(圖中部分反應物或產物已略去)。請按要求回答:
(1)反應①既是分解反應,又是氧化還原反應,產物B、D、E、F的物質的量之比1:1:1:14。A強熱分解的化學反應方程式為 ▲ 。
(2)寫出反應②在工業生產上的一種用途: ▲ 。
(3)反應③的離子方程式為 ▲ ;
反應④的化學方程式為 ▲ 。
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
仔細閱讀下圖,已知B、D、E、F、G是氧化物,其中D是形成酸雨的主要污染物,F、K是氫化物,且F在常溫下為液態;C、H是日常生活中最為常見的金屬單質,J是氣態非金屬單質,O是白色沉淀,且B、H、L、M、N、O中含有同種元素(圖中部分反應物或產物已略去)。請按要求回答:
(1)反應①既是分解反應,又是氧化還原反應,產物B、D、E、F的物質的量之比1:1:1:14。A強熱分解的化學反應方程式為 ▲ 。
(2)寫出反應②在工業生產上的一種用途: ▲ 。
(3)反應③的離子方程式為 ▲ ;
反應④的化學方程式為 ▲ 。
查看答案和解析>>
科目:高中化學 來源:2011屆浙江省嵊州二中高三12月月考化學試卷 題型:實驗題
仔細閱讀下圖,已知B、D、E、F、G是氧化物,其中D是形成酸雨的主要污染物,F、K是氫化物,且F在常溫下為液態;C、H是日常生活中最為常見的金屬單質,J是氣態非金屬單質,O是白色沉淀,且B、H、L、M、N、O中含有同種元素(圖中部分反應物或產物已略去)。請按要求回答:
(1)反應①既是分解反應,又是氧化還原反應,產物B、D、E、F的物質的量之比1:1:1:14。A強熱分解的化學反應方程式為 ▲ 。
(2)寫出反應②在工業生產上的一種用途: ▲ 。
(3)反應③的離子方程式為  ▲ ;
▲ ;
反應④的化學方程式為 ▲ 。
查看答案和解析>>
科目:高中化學 來源:2010-2011學年浙江省高三12月月考化學試卷 題型:實驗題
仔細閱讀下圖,已知B、D、E、F、G是氧化物,其中D是形成酸雨的主要污染物,F、K是氫化物,且F在常溫下為液態;C、H是日常生活中最為常見的金屬單質,J是氣態非金屬單質,O是白色沉淀,且B、H、L、M、N、O中含有同種元素(圖中部分反應物或產物已略去)。請按要求回答:
(1)反應①既是分解反應,又是氧化還原反應,產物B、D、E、F的物質的量之比1:1:1:14。A強熱分解的化學反應方程式為 ▲ 。
(2)寫出反應②在工業生產上的一種用途: ▲ 。
(3)反應③的離子方程式為 ▲ ;
反應④的化學方程式為 ▲ 。

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com