實驗室可有軟錳礦(主要成分為MnO2)制備KMnO4,方法如下:軟錳礦與過量固體KOH和KClO3在高溫下反應,生成錳酸鉀(K2MnO4)和KCl;用水溶解,濾去殘渣,濾液酸化后,K2MnO4轉變為MnO2和KMnO4;濾去MnO2沉淀,濃縮濾液,結晶得到深紫色的針狀KMnO4.請回答:
(1)軟錳礦制備K2MnO4的化學方程式是______ 3K2MnO4+KCl+3H2O
【答案】
分析:(1)根據反應物與生成物來書寫反應方程式;
(2)根據反應物與生成物來書寫反應方程式;
(3)利用化學反應方程式及二氧化錳的質量代入計算;
(4)根據KMnO
4能與熱的經硫酸化的Na
2C
2O
4反應生成Mn
2+和CO
2,并利用質量守恒定律來書寫反應方程式;
(5)利用(4)中的化學反應方程式及恰好與0.335g純Na
2C
2O
4反應完全來計算.
解答:解:(1)由軟錳礦與過量固體KOH和KClO
3在高溫下反應,生成錳酸鉀(K
2MnO
4)和KCl,則反應為3MnO
2+6KOH+KClO
3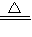
3K
2MnO
4+KCl+3H
2O,
故答案為:3MnO
2+6KOH+KClO
3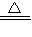
3K
2MnO
4+KCl+3H
2O;
(2)由濾液酸化后,K
2MnO
4轉變為MnO
2和KMnO
4,則反應為3MnO
42-+4H
+═MnO
2↓+2MnO
4-+2H
2O,
故答案為:3MnO
42-+4H
+═MnO
2↓+2MnO
4-+2H
2O;
(3)由3MnO
2+6KOH+KClO
3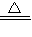
3K
2MnO
4+KCl+3H
2O、3MnO
42-+4H
+═MnO
2↓+2MnO
4-+2H
2O可知,反應物和生成物間的計量關系為:
MnO
2→K
2MnO
4→KMnO
4 87 158×

2.5×80% x
x=
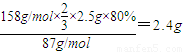
,
答:KMnO
4的理論產量是2.4g;
(4)由KMnO
4能與熱的經硫酸化的Na
2C
2O
4反應生成Mn
2+和CO
2,則反應為2KMnO
4+5Na
2C
2O
4+8H
2SO
4 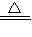
K
2SO
4+2MnSO
4+5Na
2SO
4+10CO
2+8H
2O,
故答案為:2KMnO
4+5Na
2C
2O
4+8H
2SO
4 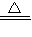
K
2SO
4+2MnSO
4+5Na
2SO
4+10CO
2+8H
2O;
(5)設該KMnO
4的純度為y,根據2KMnO
4+5Na
2C
2O
4+8H
2SO
4 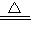
K
2SO
4+2MnSO
4+5Na
2SO
4+10CO
2+8H
2O可知,
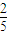
KMnO
4---Na
2C
2O
4 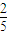
×158 134
0.165×y 0.335
y=
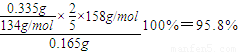
,
答:該KMnO
4的純度為95.8%.
點評:本題考查化學反應方程式的書寫及有關氧化還原反應的計算,明確反應物與生成物及物質之間的關系是解答的關鍵,難度不大.

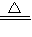 3K2MnO4+KCl+3H2O,
3K2MnO4+KCl+3H2O, 3K2MnO4+KCl+3H2O;
3K2MnO4+KCl+3H2O; 3K2MnO4+KCl+3H2O、3MnO42-+4H+═MnO2↓+2MnO4-+2H2O可知,反應物和生成物間的計量關系為:
3K2MnO4+KCl+3H2O、3MnO42-+4H+═MnO2↓+2MnO4-+2H2O可知,反應物和生成物間的計量關系為:
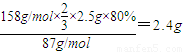 ,
, K2SO4+2MnSO4+5Na2SO4+10CO2+8H2O,
K2SO4+2MnSO4+5Na2SO4+10CO2+8H2O, K2SO4+2MnSO4+5Na2SO4+10CO2+8H2O;
K2SO4+2MnSO4+5Na2SO4+10CO2+8H2O;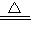 K2SO4+2MnSO4+5Na2SO4+10CO2+8H2O可知,
K2SO4+2MnSO4+5Na2SO4+10CO2+8H2O可知,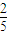 KMnO4---Na2C2O4
KMnO4---Na2C2O4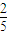 ×158 134
×158 134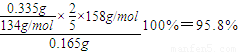 ,
,
