
���}Ŀ��(1)һ���ض��£�Ksp[Mg3(PO4)2]=6.0��10-29,Ksp[Ca3(PO4)2]=6.0��10-26�����Ⱦ��� 0.20mol��L-1�� MgCl2 �� CaCl2 �����Һ����μ��� Na3PO4�������ɳ���________(��W(xu��)ʽ)����(d��ng)�y(c��)����Һ����һ�N�����(y��ng)�x�ӳ�����ȫ(���С��10-5mol��L-1)�r(sh��)����Һ�е���һ�N�����(y��ng)�x�ӵ����|(zh��)�������c________��
(2)����ʯ����Ҫ�ɷ�BaCO3(��Ca2+��Mg2+��Fe3+���s�|(zh��))����(sh��)�(y��n)�����ö���ʯ�Ƃ�BaCl2��2H2O���������£�

��֪�� Ksp(BaC2O4)=1.6��10-7, Ksp(CaC2O4)=2.3��10-9
Ca2+ | Mg2+ | Fe3+ | |
�_(k��i)ʼ����r(sh��)��pH | 11.9 | 9.1 | 1.9 |
��ȫ����r(sh��)��pH | 13.9 | 11.1 | 3.7 |
�ٶ���ʯ���}���ȡǰ������ĥ��Ŀ����________��
�ڼ���NH3��H2O�{(di��o)��(ji��)pH=8 �ɳ�ȥ________(���x�ӷ�̖(h��o))���V�����к�________(��W(xu��)ʽ)������H2C2O4�r(sh��)��(y��ng)�����^(gu��)����ԭ����________________��
���𰸡� Mg3(PO4)2 <10-4mol��L-1 ��������(y��ng)��Ľ��|��e������(y��ng)���� Fe3+ Mg(OH)2��Ca(OH)2 ��(hu��)��(d��o)������BaC2O4�������a(ch��n)Ʒ�a(ch��n)����(hu��)�p��
��������(1)�y�����ܶȷe����(sh��)С���ȳ���������(j��)�ܶȷe����(sh��)����(du��)��С֪��Mg3(PO4)2�����ɳ�������(d��ng)��Һ��c(Mg2+)��10-5 mol/L�r(sh��)���J(r��n)���V�x����ȫ�������t��Һ�е��������Ȟ�c2(PO43-)��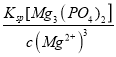 =
=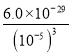 =6.0��10-14 mol2��L-2������c(Ca2+)��
=6.0��10-14 mol2��L-2������c(Ca2+)��![]() =10-4 mol��L-1���ʴ𰸞飺Mg3(PO4)2����10-4 mol��L-1��
=10-4 mol��L-1���ʴ𰸞飺Mg3(PO4)2����10-4 mol��L-1��
(2)�Ƃ�BaCl22H2O�����̣�����ʯ����Ҫ�ɷ�BaCO3(��Ca2+��Mg2+��Fe3+���s�|(zh��))�����}���ܽ⣬̼���^���}�ᷴ��(y��ng)��BaCO3+2H+=Ba2++CO2��+H2O�����백ˮ���{(di��o)pH��8��Fe3+��ȫ����r(sh��)��pH��3.2��ֻ��Fe3+��ȫ�������V��1��Fe(OH)3����Һ����Ҫ��Ca2+��Mg2+��Ba2+������������c�{(di��o)��(ji��)PH=12.5��Ca2+��ȫ����r(sh��)��pH��13.9��Mg2+��ȫ����r(sh��)��pH��11.1��Mg2+��ȫ������Ca2+���ֳ������V�����к�Mg(OH)2��Ca(OH)2����Һ����Ҫ��Ca2+��Ba2+������H2C2O4���õ�CaC2O4������ȥCa2+�����l(f��)��s��s�Y(ji��)���õ�BaCl22H2O��
�ٻ��W(xu��)����(y��ng)�������c����(y��ng)��Ľ��|��e���P(gu��n)������ʯ���}���ȡǰ������ĥ����������(y��ng)��Ľ��|��e������(y��ng)���ʣ��ʴ𰸞飺������|��e�Ķ�ʹ����(y��ng)���ʼӿ죻
�ڸ���(j��)���̈D�ͱ��Д�(sh��)��(j��)��֪��Fe3+��ȫ����r(sh��)��pH��3.2�����백ˮ���{(di��o)pH��8��Fe3++3NH3H2O=Fe(OH)3��+3NH4+��Fe3+��ȫ�������V��1��Fe(OH)3������������c�{(di��o)��(ji��)PH=12.5��Ca2+��ȫ����r(sh��)��pH��13.9��Mg2+��ȫ����r(sh��)��pH��11.1��Mg2+��ȫ������Ca2+���ֳ������V�����к�Mg(OH)2��Ca(OH)2����Һ����Ҫ��Ca2+��Ba2+��Ksp(BaC2O4)=1.6��10-7��Ksp(CaC2O4)=2.3��10-9�����γ�CaC2O4����������H2C2O4�r(sh��)��(y��ng)�����^(gu��)������ֹCaC2O4������ȫ���^(gu��)����H2C2O4��(hu��)��(d��o)������BaC2O4�������a(ch��n)Ʒ�Įa(ch��n)���p�٣��ʴ𰸞飺Fe3+��Mg(OH)2��Ca(OH)2��H2C2O4�^(gu��)����(hu��)��(d��o)������BaC2O4�������a(ch��n)Ʒ�Įa(ch��n)���p�١�


 ��У�n��ϵ�д�
��У�n��ϵ�д�
| �꼉(j��) | �����n�� | �꼉(j��) | �����n�� |
| ��һ | ��һ���M(f��i)�n�����]�� | ��һ | ��һ���M(f��i)�n�����]�� |
| �߶� | �߶����M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
| ���� | �������M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�
���}Ŀ����֪�������|(zh��)��һ���l��������KI�r(sh��)�������l(f��)������׃����Fe3+��Fe2+��Cl2 ��Cl��MnO4��Mn2+��HNO3��NO2������քe�����|(zh��)�����������@Щ���|(zh��)�c������KI����(y��ng)�õ�������
A.Fe3+B.Cl2C.MnO4D.HNO3
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�
���}Ŀ����֪����1��Zn��s��+1/2O2��g��==ZnO��s������H= -348.3kJ/mol ��2�� 2Ag��s��+1/2 O2��g��== Ag2O��s������H= -31.0kJ/mol �tZnO��s��+ 2Ag��s��== Zn��s��+ Ag2O��s������H����( )
A. -317.3kJ/molB. -379.3kJ/molC. -332.8 kJ/molD. 317.3 kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�
���}Ŀ��W��M��X��Y��Z��ԭ����(sh��)���������ǰ������Ԫ�أ��ǽ���Ԫ��W�������ڔ�(sh��)��������(sh��)��M�������Ӕ�(sh��)����ӌӔ�(sh��)�ăɱ���X�cMͬ�壬X���|(zh��)�cO2����(y��ng)���ɻ�����XO2��Y �ǵ�������ԭ�Ӱ돽��С��Ԫ�أ�Z�������г�Ҋ(ji��n)���٣��Ȳ��������壬Ҳ�����ڸ��塣�ش����І�(w��n)�}��
(1) W�cM�����γɶ�N��������������(ji��n)�λ���������ʽ_____________��
(2) ��֪����X�Ć��|(zh��)�Y(ji��)��(g��u)��( ��ÿ��(g��)Xԭ���܇����c4��(g��)X���I�γɵ�����Y(ji��)��(g��u))��������XO2�Y(ji��)��(g��u)��(
��ÿ��(g��)Xԭ���܇����c4��(g��)X���I�γɵ�����Y(ji��)��(g��u))��������XO2�Y(ji��)��(g��u)��( ��ÿ��(g��)X�c4��(g��)O���I��ÿ��(g��)O���c2��(g��)X���I�γɵ�����Y(ji��)��(g��u))��
��ÿ��(g��)X�c4��(g��)O���I��ÿ��(g��)O���c2��(g��)X���I�γɵ�����Y(ji��)��(g��u))��
�����P(gu��n)�I�ܵĔ�(sh��)��(j��)���±���
���W(xu��)�I | X-O | O=O | X-X |
�I��(kJ/mol) | 460 | 498.8 | 176 |
�������|(zh��)X ��O2��ȼ���ğữ�W(xu��)����ʽ________________________��(�þ��wԪ�ط�̖(h��o)��������ʽ)
(3) ����Z�Ć��|(zh��)�cH2O����(y��ng)�Ļ��W(xu��)����ʽ_____________________________________��
(4)Y��Z�γɵĻ������ˮ��Һ�����Ե�ԭ��_______________________________(���x�ӷ���ʽ���)��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�
���}Ŀ��(1) ���B(t��i)Siԭ���У����ռ��(j��)������܌ӷ�̖(h��o)��________��ԓ�܌Ӿ��е�ԭ��܉����(sh��)��_________��
(2) CH3COOH��Cԭ��܉���s����͞�_________��1molCH3COOH���Ӻ��Ц��I�Ĕ�(sh��)Ŀ��_________��
(3) ��(f��)����(BN)���w�ж�N��Y(ji��)��(g��u)�������൪������ͨ�����ڵķ�(w��n)���࣬�cʯī���ƣ����ЌӠ�Y(ji��)��(g��u)�������ߜ؝�(r��n)�����������൪�����dz�Ӳ���ϣ��Ѓ�(y��u)������ĥ�ԡ������ľ��w�Y(ji��)��(g��u)��D��ʾ��

�ٻ��B(t��i)��ԭ�ӵ�����Ų�ʽ��__________��
�������൪�����w�Ӄ�(n��i)һ��(g��)��ԭ���c������ԭ�Ә�(g��u)�ɵĿ��g��(g��u)�͞�__________��������Y(ji��)��(g��u)���cʯī���ƅs����(d��o)늣�ԭ����__________��
��NH4BF4 (�������@)�Ǻϳɵ�����{��ԭ��֮һ��1mol NH4BF4 ����__________mol ��λ�I��
(4) Ge�ξ����н���ʯ�ͽY(ji��)��(g��u)������Geԭ�ӵ��s����ʽ��_______����֮�g���ڵ���������__________��
(5) �����Ѓɂ�(g��)����Ҫ�أ�
��ԭ������(bi��o)����(sh��)����ʾ������(n��i)����ԭ�ӵ�����(du��)λ�ã��D�����ʯ�ľ���������ԭ������(bi��o)����(sh��)A��(0,0 ,0);B��(![]() ,0,
,0, ![]() );C��(
);C��(![]() ,
,![]() ,0)���tDԭ�ӵ�����(bi��o)����(sh��)��__________��
,0)���tDԭ�ӵ�����(bi��o)����(sh��)��__________��
�ھ�������(sh��)�����������Ĵ�С���Π��֪����ʯ��������(sh��)acm�����ܶȞ�__________g��cm-3(�г�Ӌ(j��)��ʽ����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�
���}Ŀ�������¹�̎���������_����
A.늾���·ʧ��r(sh��)���ô�����ˮ���
B.NaOH����Һ�R��Ƥ�w��������ˮ�_ϴ��Ȼ��Ϳ��ϡ������Һ
C.������R��Ƥ�w�ϣ�������ϡ NaOH ��Һϴ��
D.�c����r(sh��)��������ˮ���
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�
���}Ŀ������(j��)���ټ��仯��������W(xu��)֪�R(sh��)�ش����І�(w��n)�}��
(1)�����£��ڛ](m��i)��������ڕr(sh��)���F�cˮ��������(y��ng)�����ڸߜؕr(sh��)���F���cˮ���ⷴ��(y��ng)���������W(xu��)����(y��ng)����ʽ��_______________________________��
(2)��(1)�з���(y��ng)��ȫ������(y��ng)�a(ch��n)����FeԪ�ػ��σr(ji��)��_________��ԓ�a(ch��n)���c�}�ᷴ��(y��ng)���x�ӷ���ʽ�飺__________________________________��
(3)���F��Ͷ�뵽ʢ��Cu2����Fe3������Һ�У�����(y��ng)�ꮅ�r(sh��)���������ײ��й��wʣ�࣬�����漰�Ľ���Ԫ��(n��i)��Һ��һ�������еĽ����x����________(���x�ӷ�̖(h��o))�������C����Һ�в�����ԓ�x�ӵČ�(sh��)�(y��n)������______________________��
(4)ijͬ�W(xu��)���F���~��Ϸ�ĩ14.8 g���뵽100 mL 4.0 mol/L FeCl3��Һ�У���ַ���(y��ng)�����ײ�߀��ʣ����w�����|(zh��)����2.8 g���tԭ���w��������~���|(zh��)����______g������(y��ng)������Һ�е�Fe2�����|(zh��)������_____mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�
���}Ŀ�����Ќ�(sh��)�(y��n)�b�������_(d��)����(sh��)�(y��n)?z��i)��ĵ��?/span>
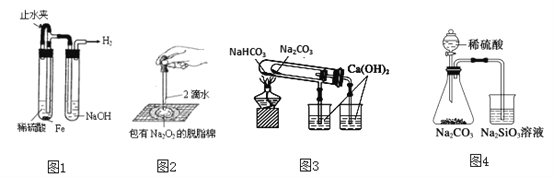
A. �D1���Ƃ䲢�^����������F
B. �D2���C���^(gu��)�����c�cˮ����(y��ng)�ş�
C. �D3���(y��n)�CNaHCO3��Na2CO3�ğ᷀(w��n)����
D. �D4���(y��n)�C���ԏ�(qi��ng)��H2SO4>H2CO3>H2SiO3
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�
���}Ŀ��ij��(sh��)�(y��n)С�Mͬ�W(xu��)�O(sh��)Ӌ(j��)��(sh��)�(y��n)�������![]() ��
��![]() ��Һ�ķ���(y��ng)���ڙz�(y��n)����(y��ng)�����Һ���Ƿ����Fe3+�r(sh��)�l(f��)�F(xi��n)��(sh��)�(y��n)�F(xi��n)������A(y��)�ϣ���ͨ�^(gu��)��(sh��)�(y��n)�M(j��n)��̽����
��Һ�ķ���(y��ng)���ڙz�(y��n)����(y��ng)�����Һ���Ƿ����Fe3+�r(sh��)�l(f��)�F(xi��n)��(sh��)�(y��n)�F(xi��n)������A(y��)�ϣ���ͨ�^(gu��)��(sh��)�(y��n)�M(j��n)��̽����
��(sh��)�(y��n)I��
| ��(sh��)�(y��n)�F(xi��n)�� |
i������ ii��ȡ����i����Һ��ԇ���У��μ�2��1 mol/L |
��֪��i��![]()
ii��![]() �����|(zh��)�c�u�؆��|(zh��)���ƣ��������ԣ�
�����|(zh��)�c�u�؆��|(zh��)���ƣ��������ԣ�![]()
��1��![]() ��
��![]() ��Һ����(y��ng)���x�ӷ���ʽ��______��
��Һ����(y��ng)���x�ӷ���ʽ��______��
��2���F(xi��n)��ii����Һ��K�ʼtɫ��һ�N����ԭ���ǣ�![]() ��
��![]() ����(SCN)2���M(j��n)��ʹ��Һ�е�
����(SCN)2���M(j��n)��ʹ��Һ�е�![]() ������
������![]() ���O(sh��)Ӌ(j��)����(sh��)�(y��n)II�M(j��n)���(y��n)�C��
���O(sh��)Ӌ(j��)����(sh��)�(y��n)II�M(j��n)���(y��n)�C��

�� �J(r��n)��ԭ���C��(sh��)�ĬF(xi��n)��iii��________��
�� ����CuCl2��Һ��(y��ng)���x�ӷ���ʽ��_________��
��3���е�ͬ�W(xu��)�J(r��n)�錍(sh��)�(y��n)II������(y��n)֔(j��n)�������C��(sh��)��2���в��룬���M(j��n)�Č�(sh��)�(y��n)III���£�

�� ��(du��)�Ȍ�(sh��)�(y��n)II���f(shu��)����(sh��)�(y��n)III���Ӈ�(y��n)֔(j��n)?sh��)�ԭ��?/span>________��
�� ���M(j��n)��Č�(sh��)�(y��n)�����C��(sh��)��2���в��룬����(j��)�������F(xi��n)����______��
��4����׃��(sh��)�(y��n)I��ԇ����������������O(sh��)Ӌ(j��)��(sh��)�(y��n)IV��
��(sh��)�(y��n)IV | �F(xi��n)�� |
��2 mL 1 mol/L | �����ʎ����Һ�tɫ��ȥ���а�ɫ�������� |
�� ��(sh��)�(y��n)IV����Һ�tɫ��ȥ�������f(shu��)��![]() ����(y��ng)��ȫ���Y(ji��)�ό�(sh��)�(y��n)II��III���f(shu��)�����ɣ�_______��
����(y��ng)��ȫ���Y(ji��)�ό�(sh��)�(y��n)II��III���f(shu��)�����ɣ�_______��
�ڌ�(sh��)�(y��n)С�Mͬ�W(xu��)�M(j��n)��ӑՓ���O(sh��)Ӌ(j��)�����Ќ�(sh��)�(y��n)�������܉�z�y(c��)�tɫ��ȥ�����Һ�Ƿ���![]() ����_______������̖(h��o)����
����_______������̖(h��o)����
a���ų���Һ�е�![]() ���ټ�������
���ټ�������![]() ��Һ�M(j��n)�Йz�y(c��)
��Һ�M(j��n)�Йz�y(c��)
b���ų���Һ�е�![]() ���ټ�������
���ټ�������![]() ��Һ�M(j��n)�Йz�y(c��)
��Һ�M(j��n)�Йz�y(c��)
c���x��һ�Nֻ�c![]() ����(y��ng)��ԇ�����^���Ƿ���F(xi��n)�����F(xi��n)��
����(y��ng)��ԇ�����^���Ƿ���F(xi��n)�����F(xi��n)��
�鿴�𰸺ͽ���>>
�ٶ����� - ����(x��)��(c��)�б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��(b��o)ƽ�_(t��i) | �W(w��ng)���к���Ϣ�e��(b��o)���^(q��) | ����p�_�e��(b��o)���^(q��) | ��vʷ̓�o(w��)���x�к���Ϣ�e��(b��o)���^(q��) | �����֙�(qu��n)�e��(b��o)���^(q��)
�`���Ͳ�����Ϣ�e��(b��o)�Ԓ��027-86699610 �e��(b��o)�]�䣺58377363@163.com