
| A. | 標準狀況下134.4LCl2 | B. | 55gCO2 | ||
| C. | 標準狀況下90g H2O | D. | 6.02×1023個H2 |
分析 依據n=$\frac{V}{Vm}$=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$計算,物質的量越多則分子數越多,據此計算解答.
解答 解:標準狀況下134.4LCl2物質的量n=$\frac{134.4L}{22.4L/mol}$=6mol;55gCO2物質的量為$\frac{55g}{44g/mol}$=1.25g;標準狀況下90g H2O物質的量為$\frac{90g}{18g/mol}$=5mol;6.02×1023個H2物質的量為1mol,所以標準狀況下134.4LCl2物質的量最多,含分子數最多,
故選:A.
點評 本題考查物質的量的相關計算,熟悉以物質的量為核心的計算公式是解題關鍵,題目難度不大.


科目:高中化學 來源: 題型:選擇題
| 項 | ① | ② | ③ | 實驗結論 | 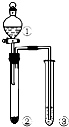 |
| A | 稀鹽酸 | Na2SO3 | Na2SiO3溶液 | 非金屬性:Cl>C>Si | |
| B | 稀硫酸 | Na2S | 滴加少量AgNO3的KI溶液 | Ksp(AgI)>Ksp(Ag2S) | |
| C | 濃鹽酸 | KMnO4 | AgNO3和稀硝酸混合溶液 | Cl2溶于水有Cl-生成 | |
| D | 濃硫酸 | 蔗糖 | Ba(OH)2溶液 | SO2能與堿溶液反應 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 膠體粒子的大小在1~100nm之間 | |
| B. | 用光束照射CuSO4溶液能觀察到丁達爾效應 | |
| C. | 明礬在水中能生成氫氧化鋁膠體,故可作凈水劑 | |
| D. | 向沸水中逐滴加入少量飽和FeCl3溶液,可制得Fe(OH)3膠體 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 17.6g | B. | 18.4g | ||
| C. | 24.0g | D. | 條件不足無法計算 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com